ASFV基因组由一个170~190 kb的双链DNA分子组成,病毒粒子呈现对称的二十面体结构,成熟病毒粒子包含多达68种结构蛋白和100多种非结构蛋白,其中结构蛋白对病毒感染研究及疫苗、诊断试剂研制的意义重大[4]。病毒粒子自外而内包括外囊膜、衣壳、内膜、核衣壳和基因组5个部分[5],外囊膜由EP402R基因编码的CD2v蛋白组成。CD2v是一种与T淋巴细胞表面黏附受体CD2相似的蛋白,由信号肽(1~16个氨基酸)、胞外区(17~207个氨基酸)、跨膜区(208~228个氨基酸)和胞内区(229~375个氨基酸)4部分组成[6],CD2v参与ASFV宿主免疫应答、免疫逃逸和病毒复制等生理生化过程,是病毒诊断和疫苗研发的重要靶点蛋白[7]。用杆状病毒表达的CD2v蛋白免疫可保护猪免于致死性感染[8],而且用CD2v蛋白免疫还可诱导猪产生特异性T细胞免疫反应[9]。
真核细胞和原核细胞均可用于外源基因的表达。真核表达系统表达的重组蛋白在结构和功能上更接近天然蛋白[10]。已有研究利用昆虫杆状病毒及CHO等真核表达系统对CD2v蛋白进行表达[11-13],其纯化蛋白能与临床ASFV抗体阳性血清反应。大肠埃希菌原核表达系统具有操作简单方便、表达周期短且成本低、蛋白表达水平高等优点,缺点在于所表达蛋白大多为包涵体,无法形成正确的三维结构,往往无生物学活性[14-16]。多个研究小组尝试利用原核表达系统来表达CD2v蛋白,但表达蛋白主要以包涵体形式存在[17-20],对包涵体进行溶解及镍柱亲和层析后,CD2v纯化蛋白与ASFV抗体阳性血清的免疫反应性较差[19];而纯化的CD2v可溶性蛋白能够被ASFV抗体阳性血清识别,具有良好的反应原性[18];蛋白质印迹法分析结果表明,表达的可溶性CD2v胞外区蛋白与ASFV抗体阳性血清具有良好的免疫反应性[17]。
综上所述,原核表达系统主要以包涵体形式表达CD2v蛋白,包涵体蛋白的免疫反应性较差且纯化、复性难度较大,不利于蛋白的功能研究及应用。因此,把CD2v蛋白与适宜的标签蛋白进行融合表达,筛选促进蛋白可溶性表达的载体,对CD2v蛋白的可溶性表达具有重要意义[21]。本研究基于5种不同的原核表达载体,筛选能促进CD2v蛋白可溶性表达的最佳表达载体,通过临床ASFV抗体阳性血清检测并比较可溶性CD2v蛋白和包涵体CD2v蛋白的免疫反应性,为原核表达可溶性CD2v蛋白及探究其免疫原性奠定基础。
1 材料与方法
1.1 材料
高保真酶(货号P510-01)购自南京诺唯赞生物科技股份有限公司;异丙基硫代-β-D-半乳糖苷[isopropylthio-β-D-galactoside(IPTG),货号15529019]、DNA标志物(货号01112376)购自赛默飞世尔科技(中国)有限公司;聚合酶链反应(polymerase chain reaction, PCR)产物清洁回收试剂盒(货号2101050)、DNA凝胶回收试剂盒(货号2003050)购自杭州新景生物试剂开发有限公司;DH5α和BL21(DE3)大肠埃希菌感受态细胞由本实验室制备;原核表达载体pET-28a、pET32a、pGEX-4T-1、pMAL-C6T和pCold-TF由本实验室保存;二辛可酸(bicinchoninic acid, BCA)蛋白浓度测定试剂盒(货号C503021-0500)购自生工生物工程(上海)股份有限公司;镍-氨三乙酸(nickel-nitrilotriacetic acid, Ni-NTA)琼脂糖(货号30210)购自德国QIAGEN公司;辣根过氧化物酶(horseradish peroxidase, HRP)标记的羊抗鼠IgG(货号074-1806)、HRP标记的羊抗猪IgG(货号14-14-06)购自美国KPL公司;质粒小提试剂盒(货号DP103-02)购自天根生化科技(北京)有限公司;其他生化试剂均为国产分析纯。临床ASFV抗体阳性血清(病毒被灭活)和标准阴性血清由本实验室保存。
1.2 方法
1.2.1 原核表达质粒的构建与鉴定
根据GenBank数据库中公布的非洲猪瘟病毒HLJ-2018株(登录号MK333180.1)的序列信息,由杭州尚亚科技有限公司合成去除信号肽和跨膜区的非洲猪瘟病毒CD2v蛋白(CD2vΔSP-TM)序列。将序列插入原核表达载体pET-28a,构建原核表达质粒pET28a-CD2vΔSP-TM。根据不同的原核表达载体设计引物,以pET28a-CD2vΔSP-TM原核表达质粒为模板,通过PCR扩增CD2v序列后,将目的片段分别插入pCold-TF、pMAL-C6T、pGEX-4T-1和pET-32a原核表达载体,得到原核表达质粒pCold-TF-CD2vΔSP-TM、pMAL-C6T-CD2vΔSP-TM、pGEX-4T-1-CD2vΔSP-TM和pET32a-CD2vΔSP-TM。将上述原核表达质粒转化至DH5α大肠埃希菌感受态细胞中,涂板并挑选单克隆菌落,将PCR鉴定为阳性的菌液送至杭州尚亚科技有限公司进行测序,对测序正确的阳性菌液进行质粒抽提,用于后续原核表达实验。
1.2.2 CD2v蛋白的原核表达与鉴定
将鉴定正确的质粒转化至BL21(DE3)大肠埃希菌感受态细胞中,涂板培养后,挑取单克隆菌落接种至LB培养基中,于37 ℃活化,将活化后的菌液按照体积比1∶100转接至含抗生素(100 μg/mL)的LB液体培养基中,于37 ℃、200 r/min条件下培养约4 h,待菌液在600 nm处的吸光度值达0.6时,向菌液中加入终浓度为1.0 mmol/L的IPTG,于16 ℃、120 r/min条件下培养16 h,诱导结束后离心收集菌液,在冰浴条件下超声破碎,离心后分别吸取上清液并保留沉淀,制备样品,经十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(sodium dodecyl sulfate-polyacrylamide gel electrophoresis, SDS-PAGE)后,用考马斯亮蓝R250进行染色,以检测重组蛋白的表达情况及存在形式。各载体标签及CD2v重组蛋白分子量如表1所示。
表1 不同原核表达载体标签及重组蛋白分子量
Table 1
表达载体 Expression vector | 标签 Tag | 重组蛋白分子量 Molecular weight of recombinant protein/kDa |
|---|---|---|
| pET28a | His | |
| pET32a | Trx | |
| pGEX-4T-1 | GST | |
| pMAL-C6T | MBP | |
| pCold-TF | TF |
1.2.3 CD2v蛋白的纯化与鉴定
离心收集经低温诱导后的pCold-TF-CD2vΔSP-TM菌体沉淀,用磷酸盐缓冲液(phosphate buffer solution, PBS)重悬后,在冰浴条件下超声破碎,离心收集上清液。将上清液与Ni-NTA琼脂糖混合,以4 ℃低温翻转孵育4 h,随后用20 mmol/L咪唑去除杂蛋白,用50 mmol/L咪唑洗脱CD2v-TF重组蛋白。同样,离心收集经低温诱导后的pET28a-CD2vΔSP-TM菌体沉淀,用尿素溶液(8 mol/L尿素,20 mmol/L NaH2PO4·2H2O,300 mmol/L NaCl,pH 8.0)重悬后,在冰浴条件下超声破碎,离心收集上清液。将上清液与Ni-NTA琼脂糖混合,以4 ℃低温翻转孵育4 h,随后用缓冲液A(8 mol/L尿素,20 mmol/L NaH2PO4·2H2O,300 mmol/L NaCl,10 mmol/L咪唑,pH 8.0)、缓冲液B(8 mol/L尿素,20 mmol/L NaH2PO4·2H2O,300 mmol/L NaCl,10 mmol/L咪唑,pH 6.3)、缓冲液C(8 mol/L尿素,20 mmol/L NaH2PO4·2H2O,300 mmol/L NaCl,pH 5.9)依次去除杂蛋白,用缓冲液D(8 mol/L尿素,20 mmol/L NaH2PO4·2H2O,300 mmol/L NaCl,pH 4.5)洗脱CD2v-His重组蛋白。收集每次被洗脱的样品,用BCA法测定CD2v-TF和CD2v-His重组蛋白浓度,并将这2种重组蛋白保存于-40 ℃冰箱中。
纯化蛋白通过考马斯亮蓝R250染色和蛋白质印迹法(Western blotting)进行鉴定。在蛋白质印迹法中,将经过SDS-PAGE后的纯化蛋白分别转印至硝酸纤维素膜上,用5%脱脂奶粉封闭1 h(37 ℃),加入按体积比1∶1 000稀释的多聚组氨酸标签(His-Tag)的鼠源单抗作为一抗,37 ℃孵育1 h后,用含吐温-20的磷酸盐缓冲液(phosphate buffer solution with Tween-20, PBST)洗涤3次,每次5 min,然后加入按体积比1∶5 000稀释的HRP标记的羊抗鼠二抗,37 ℃孵育1 h,用PBST洗涤后,利用增强型化学发光(enhanced chemiluminescence, ECL)试剂进行显色。
1.2.4 2种CD2v重组蛋白的免疫反应性比较
采用间接酶联免疫吸附测定(enzyme-linked immunosorbent assay, ELISA)方法比较2种CD2v重组蛋白的免疫反应性。将纯化后的2种CD2v重组蛋白用0.05 mmol/L PBS(pH 9.6)稀释至2 μg/mL,然后以100 μL/孔包被96孔酶标板,每块96孔酶标板于4 ℃过夜包被12 h,弃包被液,用200 μL/孔PBST清洗3次后,每孔加入200 μL 5%脱脂奶粉,37 ℃封闭1 h,然后用200 μL/孔PBST重复清洗3次。临床ASFV抗体阳性血清(n=5)和标准阴性血清(n=5)分别用5%脱脂奶粉按体积比1∶200、1∶400、1∶800、1∶1 600、1∶3 200、1∶6 400、1∶12 800、1∶25 600稀释后,每孔加入100 μL稀释后的溶液,37 ℃孵育1 h,每个稀释度设3个重复。用PBST洗涤3次后,按100 μL/孔加入经1∶2 000稀释的HRP标记的羊抗猪IgG,37 ℃孵育45 min,再用PBST洗涤3次后,每孔加入100 μL 3,3
2 结果与分析
2.1 原核表达质粒的构建与鉴定结果
以合成CD2v基因的质粒为模板,通过PCR扩增得到去除信号肽和跨膜区的CD2v序列片段,将其分别构建到pET-28a、pET32a、pGEX-4T-1、pMAL-C6T、pCold-TF 5个原核表达载体中,获得原核表达质粒,然后将这些质粒转化到DH5α大肠埃希菌感受态细胞中,经过对应抗性的LB平板筛选,挑取单克隆菌落接种于对应抗性的LB液体培养基中进行培养。以特异性引物(上游引物CD2v-F,5
图1
图1
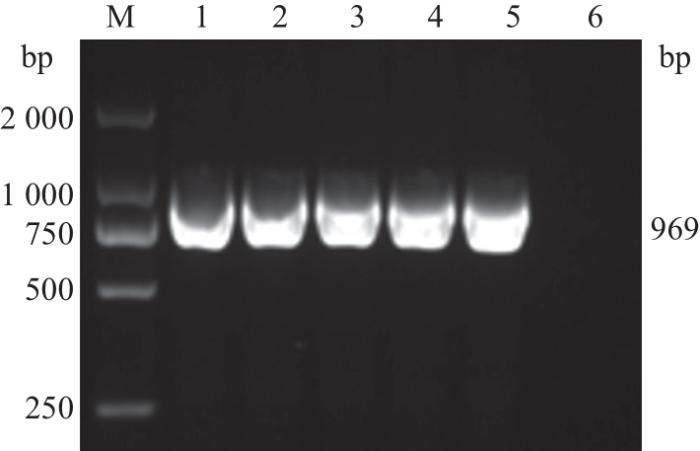
重组质粒的PCR鉴定结果
M:DNA分子标志物;1~5:pET-28a-CD2vΔSP-TM、pET32a-CD2vΔSP-TM、pGEX-4T-1-CD2vΔSP-TM、pMAL-C6T-CD2vΔSP-TM和pCold-TF-CD2vΔSP-TM重组质粒的PCR扩增产物;6:阴性对照。
Fig. 1
PCR identification results of recombinant plasmids
M: DNA marker; 1-5: Amplification products of pET-28a-CD2vΔSP-TM, pET32a-CD2vΔSP-TM, pGEX-4T-1-CD2vΔSP-TM, pMAL-C6T-CD2vΔSP-TM and pCold-TF-CD2vΔSP-TM recombinant plasmids, respectively; 6: Negative control.
2.2 CD2v蛋白的原核表达与鉴定结果
图2
图2
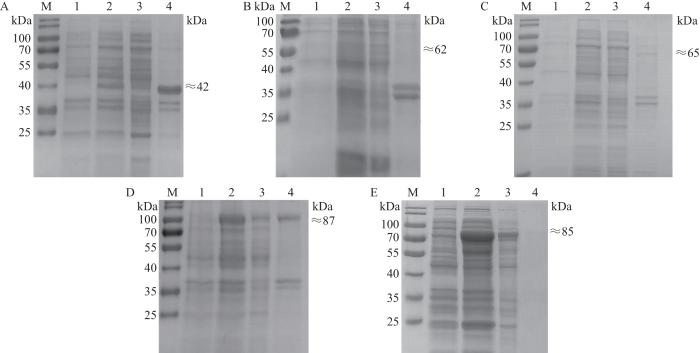
5种不同原核表达载体对CD2v重组蛋白表达的SDS-PAGE分析
A~E.分别为pET-28a-CD2vΔSP-TM、pET32a-CD2vΔSP-TM、pGEX-4T-1-CD2vΔSP-TM、pMAL-C6T-CD2vΔSP-TM、pCold-TF-CD2vΔSP-TM重组质粒。M:蛋白质相对分子质量;1:未诱导菌体;2:诱导后菌体;3:诱导后菌体超声裂解上清液;4:诱导后菌体超声裂解沉淀。
Fig. 2
SDS-PAGE analysis of CD2v recombinant protein expression by five different prokaryotic expression vectors
A-E. pET28a-CD2vΔSP-TM, pET32a-CD2vΔSP-TM, pGEX-4T-1-CD2vΔSP-TM, pMAL-C6T-CD2vΔSP-TM and pCold-TF-CD2vΔSP-TM recombinant plasmids, respectively. M: Relative molecular weight of protein; 1: Uninduced bacteria; 2: Induced bacteria; 3: Bacterial supernatant by ultrasonic lysis after induction; 4: Bacterial precipitation by ultrasonic lysis after induction.
2.3 CD2v蛋白的纯化与鉴定结果
图3
图3
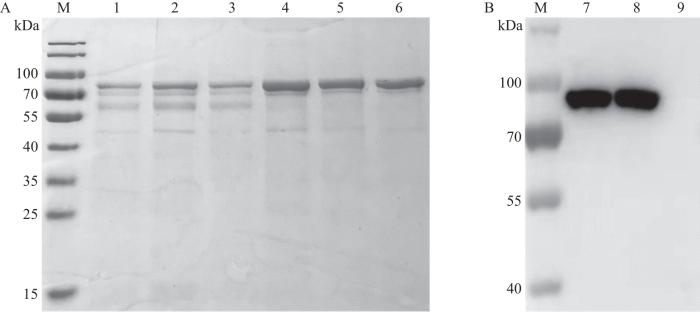
CD2v-TF重组蛋白纯化结果
A. SDS-PAGE分析;B.蛋白质印迹法分析。M:蛋白质相对分子质量;1~3:用20 mmol/L咪唑洗脱的杂蛋白;4~6:用50 mmol/L咪唑洗脱的目的蛋白CD2v-TF;7:纯化的目的蛋白CD2v-TF;8:诱导后菌体;9:未诱导菌体(对照)。
Fig. 3
Purification results of CD2v-TF recombinant protein
A. SDS-PAGE analysis; B. Western blotting analysis. M: Relative molecular weight of protein; 1-3: Heterologous proteins eluted with 20 mmol/L imidazole; 4-6: Target protein CD2v-TF eluted with 50 mmol/L imidazole; 7: Purified target protein CD2v-TF; 8: Induced bacteria; 9: Uninduced bacteria (control).
图4
图4
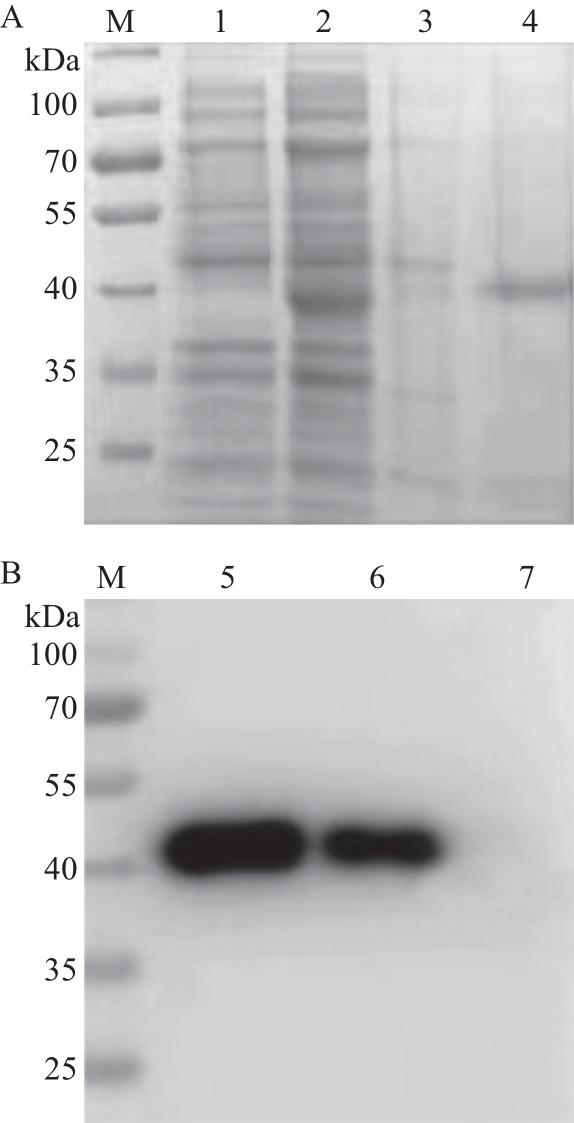
CD2v-His重组蛋白纯化结果
A. SDS-PAGE分析;B.蛋白质印迹法分析。M:蛋白质相对分子质量;1、7:未诱导菌体(对照);2、6:诱导后菌体;3:洗脱的杂蛋白;4:洗脱的目的蛋白CD2v-His;5:纯化的目的蛋白CD2v-His。
Fig. 4
Purification results of CD2v-His recombinant protein
A. SDS-PAGE analysis; B. Western blotting analysis. M: Relative molecular weight of protein; 1, 7: Uninduced bacteria (control); 2, 6: Induced bacteria; 3: Eluted heterologous protein; 4: Eluted target protein CD2v-His; 5: Purified target protein CD2v-His.
2.4 2种CD2v重组蛋白的免疫反应性比较分析
图5
图5
利用间接ELISA方法检测2种CD2v重组蛋白的免疫反应性
*表示与CD2v-His重组蛋白组相比在P<0.05水平差异有统计学意义;n=3。
Fig. 5
Immunoreactivity of two CD2v recombinant proteins detected by indirect ELISA
Single asterisk (*) indicates significant differences compared with the CD2v-His recombinant protein group at the 0.05 probability level, and n=3.
3 讨论
大肠埃希菌原核表达系统具有操作简单方便、表达量高、周期短、成本低等优点,但其表达的CD2v蛋白多以包涵体的形式存在,经尿素溶解后,蛋白空间结构被破坏而呈变性状态,空间表位丢失,导致免疫原性较差[11,26-27],影响了其在低成本疫苗研制中的应用。本研究系统比较了5种原核表达载体不同重组标签对CD2v蛋白可溶性表达的影响。结果表明:作为被广泛应用的pET表达系统中的2个代表性载体,pET28a和pET32a均未能促进CD2v的可溶性表达;pGEX-4T-1载体虽然具有促进蛋白可溶性表达的谷胱甘肽-S-转移酶(glutathione S-transferase, GST)标签[28],但其仍表达以包涵体形式为主的CD2v重组蛋白;pMAL-C6T载体具有麦芽糖结合蛋白(maltose binding protein, MBP)标签,该标签不仅能提高重组蛋白表达量,而且能减少蛋白降解并促进其可溶性表达[29],在本研究中该标签虽然可提高CD2v蛋白的可溶性表达,但在非变性亲和纯化过程中杂蛋白较多,影响了CD2v蛋白的纯度;而pCold-TF载体表达的CD2v重组蛋白均以可溶性的方式存在,且可纯化获得纯度较高的可溶性重组蛋白。pCold-TF是一种冷休克载体,带有触发因子(trigger factor, TF)标签,而TF是原核细胞中与核糖体相关的分子伴侣蛋白,可促进多肽进行共翻译折叠表达,并通过提高蛋白的正确折叠来促进可溶性表达[30]。
4 结论
本研究构建了5种原核表达重组质粒,比较了CD2v蛋白的可溶性表达情况,并利用临床ASFV抗体阳性血清比较了在可溶性和包涵体形式下CD2v蛋白的免疫反应性。结果表明,TF标签可有效促进CD2v蛋白的可溶性表达,且可溶性CD2v蛋白的免疫反应性显著高于包涵体蛋白,表明蛋白的可溶性表达可能在空间表位层面影响蛋白的免疫反应性。因此,选择合适的表达载体是CD2v蛋白在原核表达系统中实现正确折叠和可溶性表达的一种有效策略。本研究为ASFV CD2v蛋白的可溶性表达提供了参考载体,为CD2v蛋白功能与免疫原性研究及亚单位疫苗研制奠定了基础。
参考文献
Emergence of African swine fever in China, 2018
[J].
An update on African swine fever virology
[J].
Structure of African swine fever virus and associated molecular mechanisms underlying infection and immunosuppression: a review
[J].
Architecture of African swine fever virus and implications for viral assembly
[J].
The CD2v protein of African swine fever virus interacts with the actin-binding adaptor protein SH3P7
[J].
非洲猪瘟病毒跨膜蛋白CD2v的结构与功能研究进展
[J].
Research advances in structure and function of transmembrane protein CD2v of African swine fever virus
[J].DOI:10.13242/j.cnki.bingduxuebao.004023 [本文引用: 1]
Functional and immunological properties of the baculovirus-expressed hemagglutinin of African swine fever virus
[J].
Immunization of pigs by DNA prime and recombinant vaccinia virus boost to identify and rank African swine fever virus immunogenic and protective proteins
[J].
Protein expression and purification
[J].
非洲猪瘟病毒CD2v蛋白杆状病毒表达及其单克隆抗体制备
[D].
Expression of African swine fever CD2v protein by baculovirus system and preparation of monoclonal antibody
[D].DOI:10.17660/ejhs.2022/005 [本文引用: 2]
Development of a dual ELISA for the detection of CD2v-unexpressed lower-virulence mutational ASFV
[J].
基于CHO-K1细胞稳定表达的非洲猪瘟病毒CD2v蛋白的间接ELISA抗体检测方法的建立
[J].
Development of an indirect ELISA based on African swine fever virus CD2v protein stably expressed in CHO-K1 cells
[J].DOI:10.16656/j.issn.1673-4696.2022.0029 [本文引用: 1]
Industrial production of recombinant therapeutics in Escherichia coli and its recent advancements
[J].
Advances in recombinant protein expression for use in pharmaceutical research
[J].
Recombinant protein expression in Escherichia coli: advances and challenges
[J].
非洲猪瘟CD2v截短蛋白的原核表达及间接ELISA方法的建立
[J].
Prokaryotic expression of CD2v truncated protein of African swine fever virus and establishment of an indirect CD2v-ELISA
[J].DOI:10.16303/j.cnki.1005-4545.2022.06.01 [本文引用: 2]
非洲猪瘟病毒Georgia 2007/1株CD2v蛋白的原核表达及多克隆抗体制备
[J].
Prokaryotic expression and polyclonal antibody preparation of African swine fever virus Georgia 2007/1 strain CD2v protein
[J].DOI:10.16431/j.cnki.1671-7236.2019.12.029 [本文引用: 1]
非洲猪瘟CD2v胞外区基因片段的真核表达及其多克隆抗体的制备
[J].
Eukaryotic expression the CD2v extracellular gene fragment of African swine fever virus and characterization of its polyclonal antibodies
[J].DOI:10.16656/j.issn.1673-4696.2021.0012 [本文引用: 1]
非洲猪瘟病毒外膜蛋白CD2v的原核表达及其免疫特性的研究
[J].
Prokaryotic expression and immunological characterization of African swine fever virus out membrane CD2v protein
[J].DOI:10.16656/j.issn.1673-4696.2020.0089 [本文引用: 1]
Fusion tags for protein solubility, purification and immunogenicity in Escherichia coli: the novel Fh8 system
[J].
非洲猪瘟病原学与传播特点及防控方法的研究进展
[J].
Advancement in etiology, transmission and prevention and control of African swine fever
[J].DOI:10.16656/j.issn.1673-4696.2022.0138 [本文引用: 1]
Deletion of CD2-like (CD2v) and C-type lectin-like (EP153R) genes from African swine fever virus Georgia-∆9GL abrogates its effectiveness as an experimental vaccine
[J].
BA71ΔCD2: a new recombinant live attenuated African swine fever virus with cross-protective capabilities
[J].
The recombinant pseudorabies virus expressing African swine fever virus CD2v protein is safe and effective in mice
[J].
Practical considerations in refolding proteins from inclusion bodies
[J].
Protein production and purification of a codon-optimized human NGN3 transcription factor from E. coli
[J].
Single-step purification of polypeptides expressed in Escherichia coli as fusions with glutathione S-transferase
[J].
通过使用MBP标签高水平原核表达纯化死亡结构域家族蛋白及炎症小体NLRP1与ASC的结构生物学研究
[D].
High-level prokaryotic expression and purification of death domain superfamily with MBP tag and structural basis of NLRP1 and ASC inflammasome
[D].DOI:10.7754/clin.lab.2017.170922 [本文引用: 1]
鸡氨肽酶N的高效可溶性表达及生物学功能分析
[J].
Expression and biological function analysis of chicken aminopeptidase N
[J].DOI:10.13345/j.cjb.2010.04.014 [本文引用: 1]