我国臭氧污染问题日益突出,已成为许多区域大气污染的首要因子,“十四五”期间大气污染防治任务仍十分艰巨[1]. 氮氧化物(NOx)与挥发性有机物(VOCs)在大气环境中的二次化学反应是造成臭氧污染的重要原因,因此有效控制NOx对于遏制臭氧污染有十分重要的作用. 以V2O5-WO3/TiO2为催化剂、NH3为还原剂的选择性催化还原脱硝技术(NH3-SCR),因其具有高效、成熟、稳定等优点被广泛应用于燃煤电厂烟气脱硝[2]. V2O5-WO3/TiO2催化剂的最佳运行温度窗口为350~450 ℃,对于水泥、玻璃类的非电行业工业炉窑,其烟气温度往往低于300 ℃,无法直接移用V2O5-WO3/TiO2催化剂[3-4]. 烟气再热技术虽然可以将烟气提升至V2O5-WO3/TiO2催化剂高效运行所需温度区间,但会造成大量的能量消耗. 由于适用于非电行业工业炉窑烟气脱硝的中低温SCR催化剂可以节省大量的运行成本,其研究开发受到广泛关注[5-7].
尖晶石氧化物是具有特殊空间结构的功能材料,其化学式可以表示为AB2O4,其中A2+离子与O2-之间为四配位,B3+离子与O2-之间为六配位. 不同金属间的协同作用以及A2+和B3+离子间的电子传递效应,使尖晶石氧化物往往具有良好的催化活性和稳定性[8-9]. Gao等[10-11]制备的含Cr离子的复合尖晶石氧化物具有优异的低温SCR脱硝性能. 此外,以Cu为主要活性组分的SCR催化剂,如Cu-SSZ-13、Cu-SAPO-34分子筛催化剂[12],Cu/TiO2、Cr/TiO2金属氧化物催化剂也具有良好的脱硝活性[13]. 尖晶石A2+位点的离子选择对催化剂的活性有显著影响,Cu离子作为活性位占据A2+位点是构筑高活性低温SCR催化剂的理想选择. 然而,Cu-Cr复合尖晶石催化剂的脱硝性能如何,仍有待进一步探究.
催化剂的形貌特征与其催化活性间存在密切关系,本研究采用溶胶凝胶法制备普通颗粒状的CuCr2O4催化剂,采用溶剂热法制备球状和多面体状的CuCr2O4催化剂. 测试对比不同形貌CuCr2O4催化剂的SCR脱硝活性,分析形貌对于CuCr2O4催化剂脱硝活性的影响,并通过相关表征技术揭示催化剂形貌特征与催化性能的构−效关系.
1. 实验材料和方法
1.1. 催化剂制备
不同形貌CuCr2O4催化剂样品的制备方法如下[14]. 1)多面体CuCr2O4:将2 mmol Cu(NO3)2-3H2O、4 mmol Cr(NO3)3-9H2O、0.3 g聚乙烯吡咯烷酮(PVP)先后溶于30 mL无水乙醇中充分搅拌. 配制30 mL浓度为10 mol/L的 NaOH溶液,逐滴滴入混合溶液,将混合溶液在150 ℃下水热反应12 h. 反应结束后将样品离心洗涤、干燥,干燥后的样品粉末在600 ℃下煅烧4 h,所得催化剂样品记为CuCr2O4-P. 2)球状CuCr2O4:将2 mmol Cu(NO3)2-3H2O、4 mmol Cr(NO3)3-9H2O溶于30 mL无水乙醇中充分搅拌,配制30 mL浓度为10 mol/L的NaOH溶液,逐滴滴入混合溶液. 将混合溶液在200 ℃下水热反应反应12 h. 反应结束后进行离心洗涤、干燥,干燥后的样品粉末在600 ℃下煅烧4 h,所得样品记为CuCr2O4-S. 3)颗粒状CuCr2O4:将2 mmol Cu(NO3)2-3H2O、4 mmol Cr(NO3)3-9H2O、1.512 g柠檬酸溶于30 mL去离子水充分搅拌. 将混合溶液在90 ℃的磁力搅拌水浴中搅拌至水分完全蒸发,将得到的凝胶状固体置于200 ℃烘箱中1 h,使柠檬酸分解. 干燥后的样品粉末在600 ℃下煅烧4 h,所得样品记为CuCr2O4-G.
1.2. 催化剂活性评价
催化剂活性评价在固定床石英反应器(内径为6 mm)内进行. 催化剂每次填充量为150 mg,并筛分至40~60目. 每组催化剂在测试前均在400 ℃条件下置于N2气氛中活化1 h,管式炉降温至室温后进行活性评价实验. 模拟反应气的体积分数分别为5.00×10−4 NOx、5.00×10−4 NH3、5% O2,N2作为载气,各组分用质量流量计混合控制. 模拟反应气总流速为280 mL/min,质量空速为1.12×105 h−1. 反应前后NOx体积分数由在线氮氧化物分析仪(Thermo Scientific 42i-HL)实时监测,NH3与N2O体积分数由红外光谱(Nicolet 6700)测定,CuCr2O4催化剂的脱硝效率X、N2选择性s分别用以下公式计算。
式中:
1.3. 催化剂表征
催化剂微观形貌使用Zeiss SIGMA HD扫描电子显微镜拍摄分析.催化剂晶型使用Ultima XRD多晶衍射仪测试,扫描速率为5°/min,扫描范围为10°~90°. 催化剂比表面积及孔道结构由N2吸附脱附所测得(Micromeritics ASAP2460),催化剂测试前在400 ℃ N2气氛下预处理0.5 h. 比表面积由BET方法测得,孔径和孔容积由BJH方法测得. 催化剂表面元素分布情况由X射线光电子能谱仪(Thermo ESCALAB 250XI)测得,并用污染碳C 1s (248.8 eV)校正,分峰拟合软件为XPSPEAK41. 催化剂酸性位特征以NH3-程序升温脱附(TPD)测定分析,催化剂氧化还原性由H2-程序升温还原(TPR)测定,测试仪器均为Micromeritics AutoChem II 2920,测试前催化剂在300 ℃ N2气氛下预处理0.5 h.
2. 实验结果与讨论
2.1. 催化剂脱硝性能
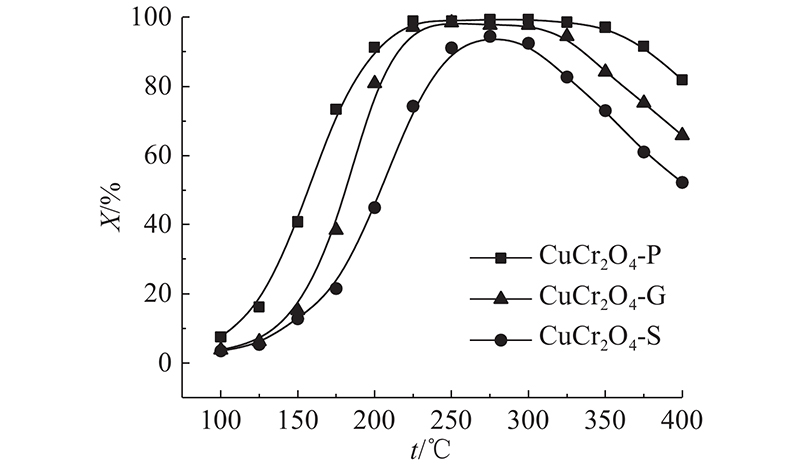
催化剂样品NH3-SCR脱硝活性测试结果如图1所示. 图中,t为反应温度,X为脱硝效率. 在
图 1
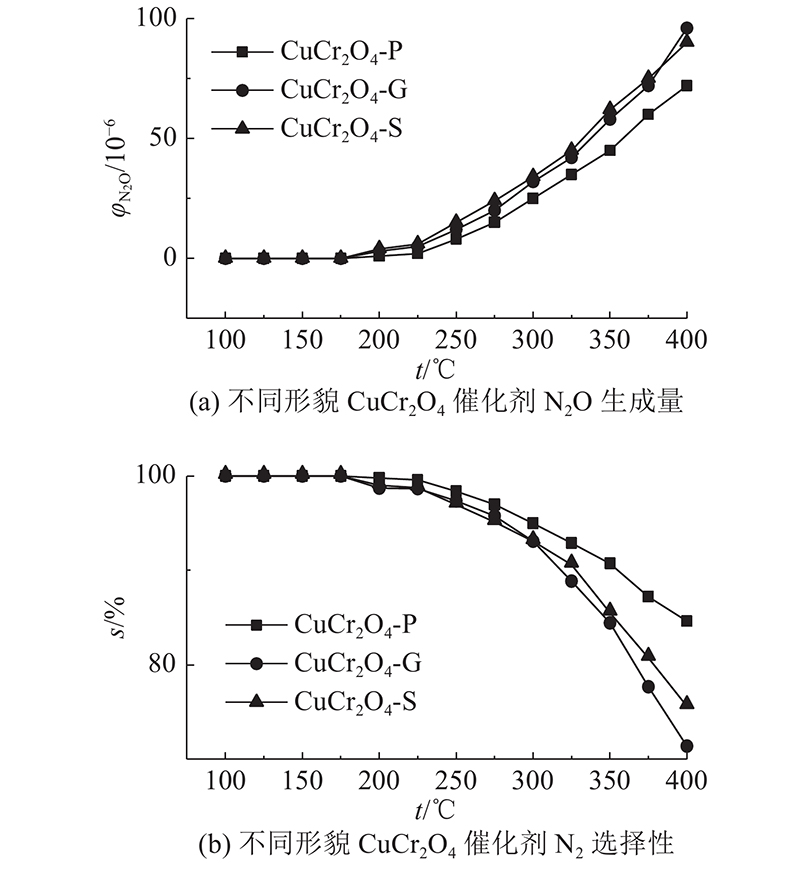
不同形貌CuCr2O4催化剂的N2O的生成量与N2选择性如图2所示. 图中,
图 2
图 2 CuCr2O4催化剂生成N2O体积分数与N2选择性
Fig.2 N2O volume fraction and N2 selectivity over CuCr2O4 catalysts
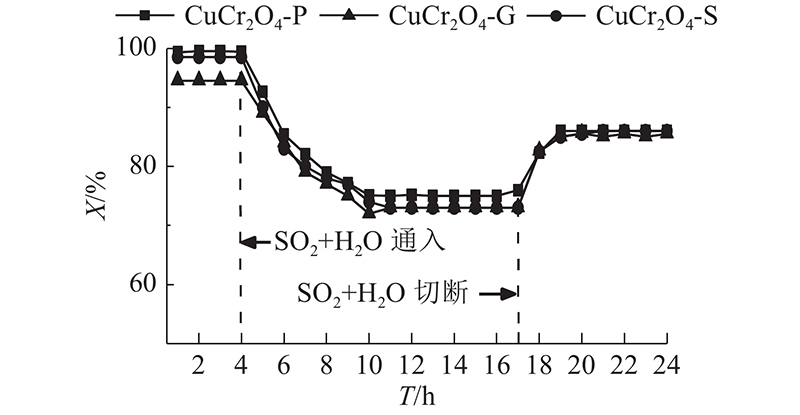
除催化剂的脱硝活性之外,其对烟气中的SO2+H2O耐受性也是实际应用中须考虑的重要因素. 因此测试在275 ℃时同时通入体积分数为5.0×10−5 SO2与5% H2O后CuCr2O4催化剂脱硝效率的变化趋势. 如图3所示,在T=4 h通入SO2+H2O后,脱硝活性皆受到显著影响并开始下降,在T=10 h时稳定在72%~75%. 在T=17 h切断SO2+H2O,CuCr2O4催化剂的脱硝效率回升,最终恢复至85%~87%. 结果表明,烟气中存在SO2+H2O会对CuCr2O4催化剂的脱硝活性产生不利影响,但CuCr2O4展现出一定的抗水抗硫性能. 脱硝活性未完全恢复的原因可能是反应过程中生成的硫酸盐覆盖催化剂活性位点所致.
图 3
图 3 SO2+H2O对CuCr2O4催化剂脱硝效率的影响
Fig.3 Effects of SO2+H2O on denitrification activity for CuCr2O4 catalysts
2.2. 微观形貌分析
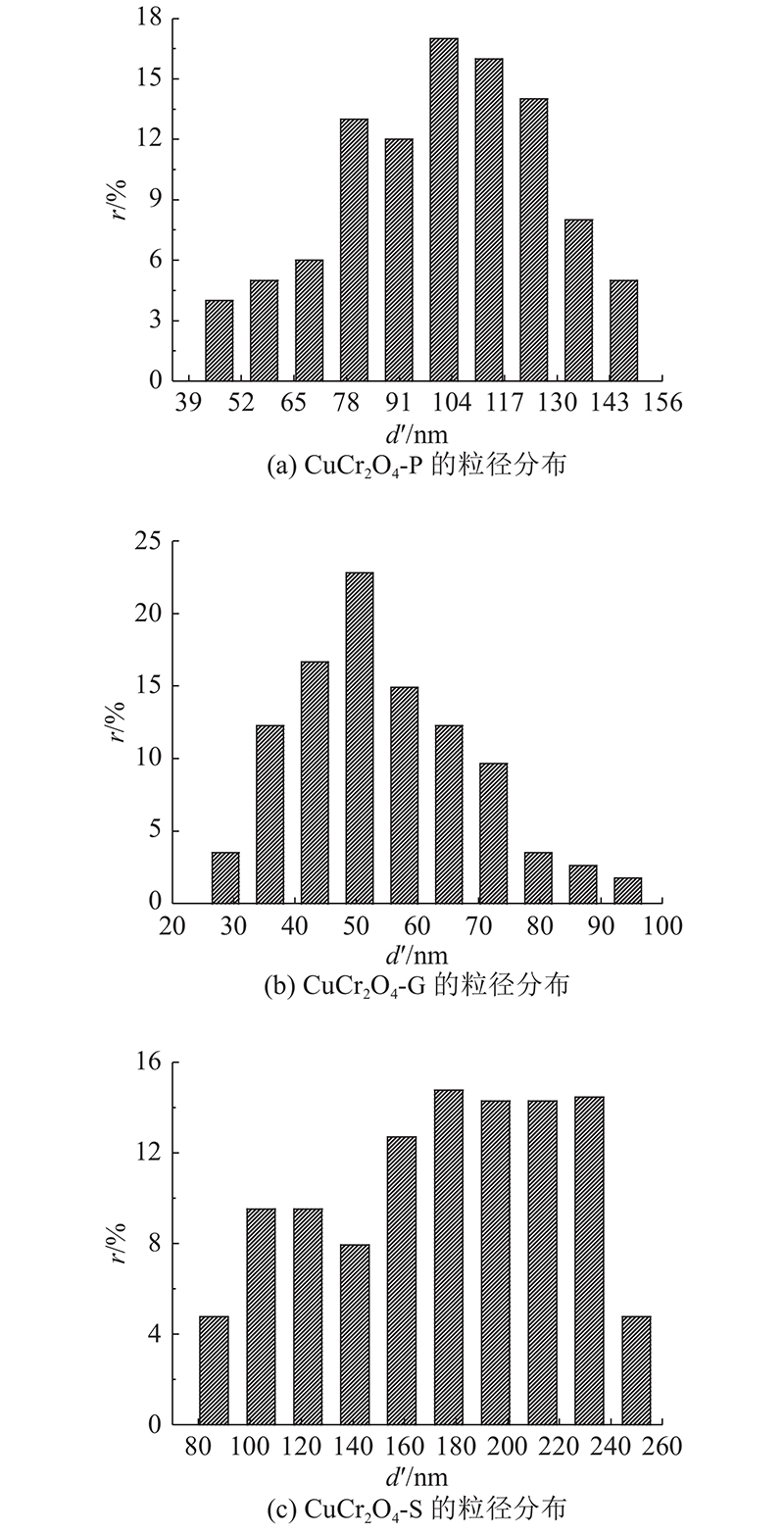
采用扫描电子显微镜(SEM)观察催化剂样品的微观形貌,如图4所示分别为3种催化剂样品在不同放大倍数下的照片. CuCr2O4-P、CuCr2O4-G和CuCr2O4-S分别呈现明显的多面体状、颗粒状和球状形貌,催化剂颗粒的粒径大小略有差别. 用r表示催化剂颗粒粒径的相对占比,d'表示催化剂颗粒的粒径,如图5所示,CuCr2O4-P催化剂的颗粒粒径主要分布于80~120 nm,CuCr2O4-G催化剂的颗粒粒径主要分布于35~70 nm,CuCr2O4-S催化剂的颗粒粒径主要分布于100~220 nm. 即球状CuCr2O4的粒径最大,多面体状CuCr2O4的粒径次之,颗粒状CuCr2O4的粒径最小. 此外,不同催化剂形貌还会使其暴露不同的反应晶面,影响其理化性质,从而影响其脱硝活性.
图 4
图 4 CuCr2O4催化剂的微观形貌特征
Fig.4 Micro-morphology characteristics of CuCr2O4 catalysts
图 5
2.3. 孔道结构分析
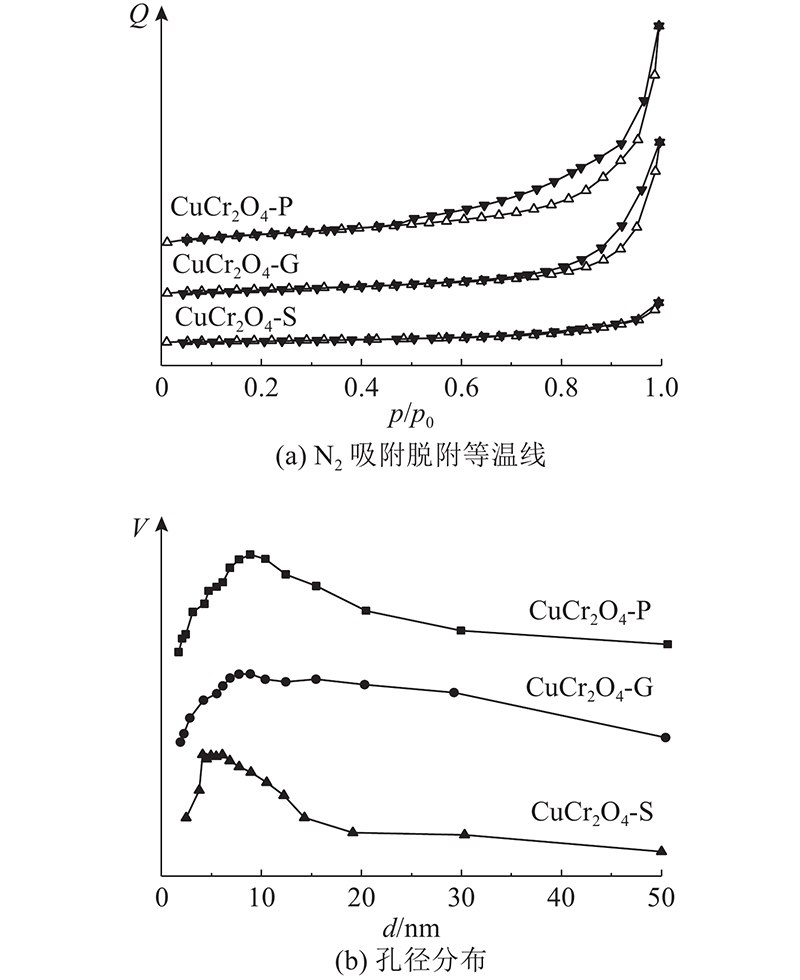
如图6所示为CuCr2O4催化剂的N2吸附脱附等温线与孔径分布图. 图中,p/p0为相对压力,Q为N2吸附量,d为孔径,V为孔体积. 可以看出,CuCr2O4-P、CuCr2O4-G均为IV型吸附等温线,同时具有明显的H3型回滞环,相较之下CuCr2O4-S回滞环较小. 结果表明,CuCr2O4-S的孔道结构不同于CuCr2O4-P、CuCr2O4-G,且它的比表面积也更小. CuCr2O4-P、CuCr2O4-G和CuCr2O4-S的孔道均为介孔. CuCr2O4-S的孔径分布窄于CuCr2O4-P、CuCr2O4-G. CuCr2O4-P的孔道尺寸均匀分布于2~30 nm,且其介孔数量在三者中最多.
图 6
图 6 CuCr2O4催化剂的N2吸附脱附等温线与BJH孔径分布
Fig.6 N2 adsorption-desorption isotherms and BJH pore diameter distribution of CuCr2O4 catalysts
CuCr2O4-P、CuCr2O4-G和CuCr2O4-S催化剂的比表面积与孔结构分析结果如表1所示. 表中,S为BET比表面积. 可以看出,3种形貌CuCr2O4催化剂的比表面积、孔径与孔容存在显著差异. CuCr2O4-P拥有最大的比表面积与最大的孔容积,大幅高于CuCr2O4-S. 这与SEM的测试结果对应,球状CuCr2O4的粒径较大,其比表面积与孔容积较低. 三者平均孔径较为接近. 比表面积与孔容积顺序为CuCr2O4-P>CuCr2O4-G>CuCr2O4-S. 较大的比表面积往往暴露更多活性位点,更有益于催化反应的进行.
表 1 CuCr2O4催化剂的比表面积、孔径与孔容
Tab.1
| 催化剂 | S/(m2·g−1) | d/nm | V/(cm3·g−1) |
| CuCr2O4-P | 25.5 | 10.9 | 0.154 |
| CuCr2O4-G | 21.8 | 11.5 | 0.146 |
| CuCr2O4-S | 16.7 | 10.4 | 0.098 |
2.4. 物相组成分析
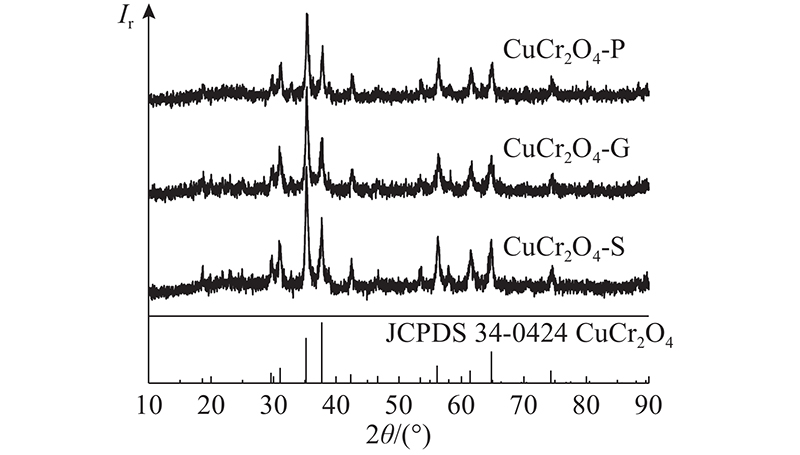
通过XRD分析所制备催化剂样品的物相组成,其结果如图7所示. 与粉末衍射标准联合会(JCPDS) CuCr2O4标准卡片比对结果表明,3种形貌的催化剂样品主要成分均为纯度较高的CuCr2O4尖晶石,杂质较少. CuCr2O4-S和CuCr2O4-G催化剂在2θ = 35.2°、37.7°、56.2°、61.4°、64.8°和74.4°处的衍射峰较CuCr2O4-P尖锐,说明球状和颗粒状CuCr2O4样品的结晶度较多面体状CuCr2O4-P更好. 结果表明,CuCr2O4-P、CuCr2O4-S和CuCr2O4-G催化剂的结晶度由于制备方法不同略有差别,这与SEM观测到CuCr2O4-S粒径较大的结论一致.
图 7
2.5. 元素组成与价态分析
通过XPS分析不同形貌催化剂表面的元素组成和化学状态. 催化剂的O 1s和Cu 2p3/2轨道电子结合能谱及其分峰拟合结果如图8所示,据此计算的催化剂表面原子摩尔分数和不同价态离子间相对比例列于表2. 催化剂表面Cu原子摩尔分数顺序为CuCr2O4-S>CuCr2O4-P>CuCr2O4-G. 催化剂表面Cr原子摩尔分数顺序为CuCr2O4-S≈CuCr2O4-G>CuCr2O4-P. 催化剂表面O原子摩尔分数顺序为CuCr2O4-G>CuCr2O4-P>CuCr2O4-S. 结果表明,不同形貌的CuCr2O4催化剂样品表面原子摩尔分数存在显著差别. 多面体状CuCr2O4-P催化剂表面有更多的Cu、O物种聚集,Cr物种分布较少.
表 2 CuCr2O4催化剂的表面元素摩尔分数
Tab.2
| 催化剂 | x/% | ||||
| Cu | O | Cr | Oα/(Oα+Oβ) | Cu+/(Cu++Cu2+) | |
| CuCr2O4-P | 12.82 | 66.07 | 21.11 | 49.5 | 16.2 |
| CuCr2O4-G | 9.57 | 66.39 | 24.04 | 39.4 | 7.6 |
| CuCr2O4-S | 13.40 | 63.21 | 24.44 | 40.8 | 10.7 |
图 8
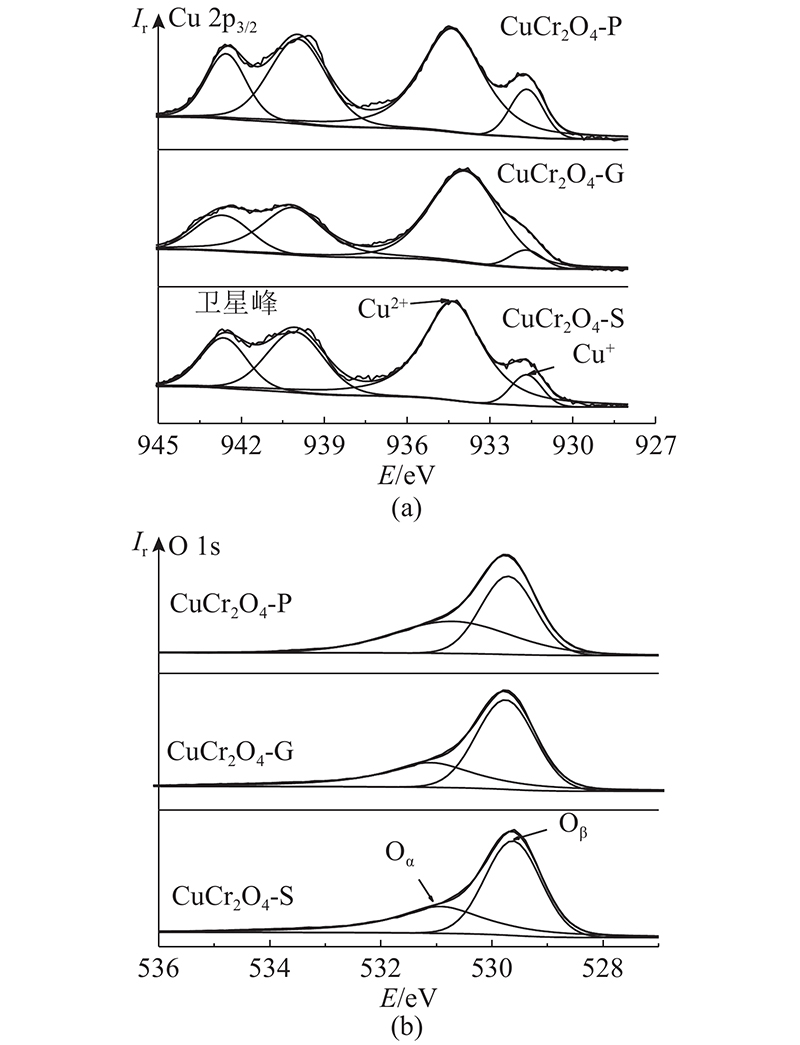
图 8 CuCr2O4催化剂O 1s与Cu 2p3/2分峰拟合结果
Fig.8 XPS spectra fitting results of O 1s and Cu 2p3/2 of CuCr2O4 catalysts
图8中的O 1s谱可以拟合为2个峰,较高结合能(531.1 eV)的峰归属于化学吸附氧(如O−、O22−和羟基),用Oα表示;较低结合能(529.7 eV)的峰归属于晶格氧物种,用Oβ表示. 分峰结果如表2所示,CuCr2O4-P催化剂Oα的摩尔分数最高,为49.5%;CuCr2O4-G与CuCr2O4-S的Oα摩尔分数值相近. Oα的活性往往高于Oβ,丰富的Oα可以促进NO氧化为NO2,参与"快速SCR"反应,显著提高低温段脱硝活性[15]. Cu 2p3/2能谱分别在934.3、931.6 eV处出现2个峰,其结合能分别对应Cu2+、Cu+物种[16],位于940、945 eV处的2个峰为它们的卫星峰. Xiong等[17]研究表明,更高比例的Cu+有益于提高SCR反应活性. 三者中CuCr2O4-P催化剂的Cu+与Oα摩尔分数最高,与其最佳的脱硝效率有较好对应.
2.6. 酸性分析
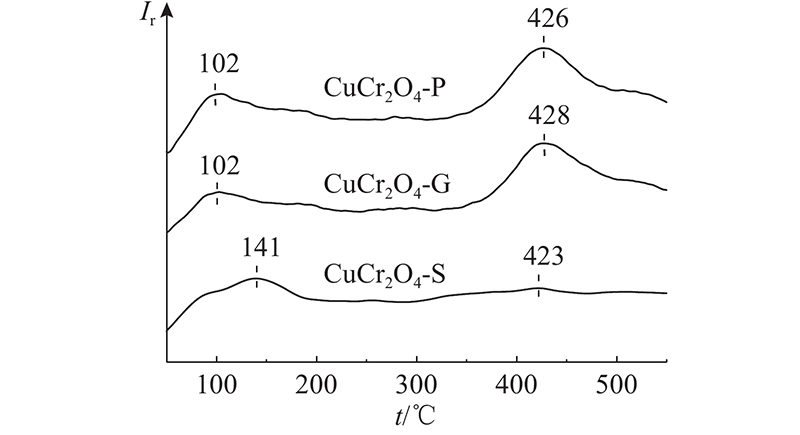
催化剂的表面酸性在NH3-SCR反应中起着非常重要的作用,酸性位提供了NH3吸附与活化的关键位点[18]. NH3-TPD分析的催化剂酸性如图9所示. 在
图 9
2.7. 氧化还原性分析
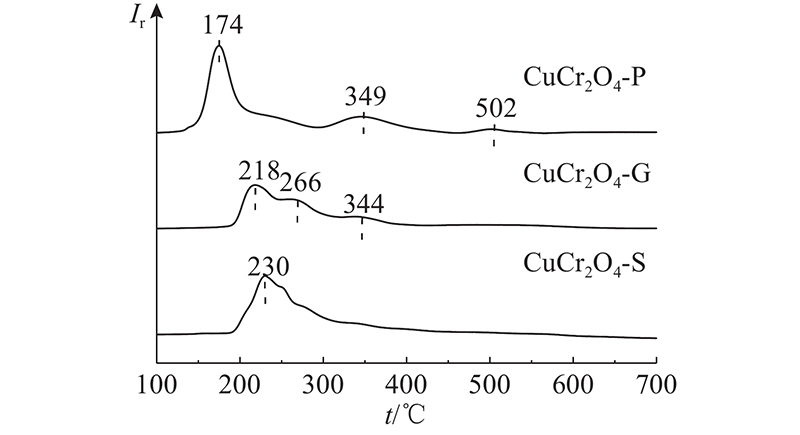
通过H2-TPR实验研究催化剂SCR性能的另一关键因素:氧化还原性,结果如图10所示. CuCr2O4-P、CuCr2O4-S和CuCr2O4-G的最大低温还原峰对应的温度分别为174、218、230 ℃,顺序为CuCr2O4-P<CuCr2O4-G<CuCr2O4-S. 位于200~300 ℃的还原峰可以归于Cu2+→Cu+与Cr6+→Cr3+在此处的重叠[17, 20],且CuCr2O4-P的还原峰温度低至174 ℃. 这表明,多面体CuCr2O4-P表面的氧物种最容易被还原,活性最高. CuCr2O4-P、CuCr2O4-G分别在349 ℃和344 ℃检测到归属于Cr3+→Cr2+还原峰[20-21],在该温度附近CuCr2O4-S未检测到还原峰,这意味着CuCr2O4-P、CuCr2O4-G表面的Cr物种较在CuCr2O4-S上更易被还原. CuCr2O4-P在502 ℃时检测到1个弱还原峰,该峰可能是Cu+→Cu0还原峰. 催化剂的总H2消耗量顺序为CuCr2O4-P(3.69 mmol·g−1) > CuCr 2O4-S(3.28 mmol·g−1) > CuCr 2O4-G(2.86 mmol·g−1). 结果表明,多面体CuCr2O4-P催化剂拥有最为丰富的可还原性物种且其可还原性最强.
图 10
3. 结 论
(1)通过调整水热法条件可制备形貌规整且纯度较高的多面体状和球状CuCr2O4催化剂. 催化剂形貌与其脱硝性能密切相关,多面体状CuCr2O4的脱硝性能显著优于常规颗粒状CuCr2O4的.
(2)脱硝活性顺序为CuCr2O4-P>CuCr2O4-G>CuCr2O4-S. 多面体状CuCr2O4催化剂具有较高的中低温活性,N2O生成量较普通颗粒状CuCr2O4低,同时具有一定的抗水抗硫性能,展现了一定的应用前景.
(3)不同的微观形貌对催化剂的理化性质有显著影响,进而影响催化性能. 多面体状CuCr2O4拥有更多的表面酸性位与更强的氧化还原性,更大的比表面积为其提供了更多的活性位点. 因此,多面体状CuCr2O4的SCR脱硝性能最优.
(4)本研究揭示了不同形貌CuCr2O4脱硝反应的构效关系,为低温SCR催化剂开发提供了新思路,也可为尖晶石型氧化物形貌控制策略研究借鉴. 今后将进一步探究CuCr2O4形貌对脱硝反应机理的影响.
参考文献
A perspective on the selective catalytic reduction (SCR) of NO with NH3 by supported V2O5-WO3/TiO2 catalysts
[J].DOI:10.1021/acscatal.8b01357 [本文引用: 1]
水泥炉窑中低温催化脱硝技术中试性能研究
[J].DOI:10.3969/j.issn.1000-6923.2021.07.019 [本文引用: 1]
A pilot scale study of low-temperature De-NOx in cement furnace
[J].DOI:10.3969/j.issn.1000-6923.2021.07.019 [本文引用: 1]
Impacts of Pb and SO2 poisoning on CeO2–WO3/TiO2–SiO2 SCR catalyst
[J].DOI:10.1021/acs.est.7b03309 [本文引用: 1]
A review of low temperature NH3-SCR for removal of NOx
[J].DOI:10.3390/catal9040349 [本文引用: 1]
Insights into the structure-activity relationships of highly efficient CoMn oxides for the low temperature NH3-SCR of NOx
[J].DOI:10.1016/j.apcatb.2020.119215
Controlled synthesis of spinel-type mesoporous Mn-Co rods for SCR of NOx with NH3 at low temperature
[J].DOI:10.1021/acs.iecr.8b05223 [本文引用: 1]
An overview of the structure and magnetism of spinel ferrite nanoparticles and their synthesis in microemulsions
[J].
Cu-Co synergism in Cu1-xCoxFe2O4 catalysis and XPS aspects
[J].DOI:10.1006/jcat.2002.3712 [本文引用: 1]
Surface lattice oxygen activation via Zr4+ cations substituting on A2+ sites of MnCr2O4 forming ZrxMn1-xCr2O4 catalysts for enhanced NH3-SCR performance
[J].DOI:10.1016/j.cej.2019.122397 [本文引用: 1]
Understanding the co-effects of manganese and cobalt on the enhanced SCR performance for MnxCo1-xCr2O4 spinel-type catalysts
[J].DOI:10.1039/D0CY00872A [本文引用: 1]
A comparison of hydrothermal aging effects on NH3-SCR of NOx over Cu-SSZ-13 and Cu-SAPO-34 catalysts
[J].DOI:10.1016/j.apcatb.2014.10.020 [本文引用: 1]
Low ‐temperature selective catalytic reduction (SCR) of NO with NH3 by using Mn, Cr, and Cu oxides supported on Hombikat TiO2
[J].DOI:10.1002/1521-3773(20010702)40:13<2479::AID-ANIE2479>3.0.CO;2-7 [本文引用: 1]
Different exposed facets VOx/CeO2 catalysts for the selective catalytic reduction of NO with NH3
[J].DOI:10.1016/j.cej.2018.05.049 [本文引用: 1]
Reaction mechanism of selective catalytic reduction of NO with NH3 over Fe-ZSM-5 catalyst
[J].DOI:10.1006/jcat.2002.3528 [本文引用: 1]
Effect of Si/Al ratio on catalytic performance of hydrothermally aged Cu-SSZ-13 for the NH3-SCR of NO in simulated diesel exhaust
[J].DOI:10.1016/j.apsusc.2017.04.198 [本文引用: 1]
The role of the Cu dopant on a Mn3O4 spinel SCR catalyst: improvement of low-temperature activity and sulfur resistance
[J].DOI:10.1016/j.cej.2020.124090 [本文引用: 2]
Ni-Mn bi-metal oxide catalysts for the low temperature SCR removal of NO with NH3
[J].DOI:10.1016/j.apcatb.2013.10.049 [本文引用: 1]
TiO2-supported metal oxide catalysts for low-temperature selective catalytic reduction of NO with NH3: I. Evaluation and characterization of first row transition metals
[J].DOI:10.1016/j.jcat.2003.09.003 [本文引用: 1]
NH3-SCR performance improvement of mesoporous Sn modified Cr-MnOx catalysts at low temperatures
[J].DOI:10.1016/j.cattod.2015.03.049 [本文引用: 2]
Cr-MnOx mixed-oxide catalysts for selective catalytic reduction of NOx with NH3 at low temperature
[J].DOI:10.1016/j.jcat.2010.08.016 [本文引用: 1]