固氮反应,即空气中游离态的氮分子转化为工农业可利用的含氮化合物(如氨、铵盐、硝酸盐等)的转化过程,维系着自然界的氮循环,是全球最重要的工业反应之一. 作为工业主流固氮技术,哈伯法合成氨生产物超过全球90%的人工固氮产品,养活了全世界40%的人口[1],被誉为“20世纪最重要的发明”. 但是哈伯法合成氨工艺需要高温高压的反应条件(350~550 ℃、15.19~35.46 MPa)和集中型、规模化的庞大设施,引发的能源和环境问题日益凸显. 哈伯法所用高纯氢通常来自工业的甲烷重整反应,每年约消耗全球天然气产能的2%,电力能源的1%~2%. 据研究统计,哈伯法每生产1 t
电催化固氮[3]、光催化固氮[4]、生物固氮[5]和低温等离子体固氮逐渐成为研究热点. 低温等离子体具有不平衡态的特性、优良的反应活性、更高比重的能量,可用于氮气的激发和活化,实现更高的能量利用率[6]. 根据反应器结构和激发方式,低温等离子体技术包含介质阻挡放电等离子体、微波放电等离子体、电晕放电等离子体和滑动弧等离子体等[7]. 与常用的介质阻挡放电等离子体相比,滑动弧等离子体处理量更大和能量密度更高,被广泛应用于惰性小分子的活化过程[8]. 相比传统的滑动弧反应器结构,旋转滑动弧等离子体(简称磁旋滑动弧)改进了电极样式、进气方式和外加磁场. 切向旋流进气和磁场加速保证了滑动弧的高速旋转,促进了电弧的非平衡态,提高了活性粒子的密度[9],催化剂的引入可进一步提升转化产率和选择性. 活性氧化铝(γ-Al2O3)由于其多孔结构、高比表面积性质,常被用作催化剂或催化剂的载体,如Patil等[10]研究发现,γ-Al2O3对于介质阻挡放电氧化固氮
1. 实验方法及装置
1.1. MoO3/Al2O3催化剂制备
选取MoO3/Al2O3作为催化剂进行等离子体耦合催化,利用过量浸渍法制备质量分数分别为5%、7.5% 和10%的催化剂. 使用粒径为3~5 mm的γ-Al2O3(Macklin)作为催化剂载体. 采用钼酸铵(99%,九鼎化学)和二水合乙二酸(GR,国药集团)作为MoO3的前驱物. 制备时,将一定量的前驱物溶于适量去离子水,将载体氧化铝小球置于前驱物溶液中,静置12 h,80 ℃水浴加热蒸干溶液水分,马弗炉110 ℃进一步干燥样品,干燥12 h后,在空气气氛下400 ℃煅烧6 h.
1.2. 催化剂表征方法
X射线衍射(X-ray diffraction,XRD)图谱可以用于分析催化剂的物相组成. 本研究采用XRD(D/max-2550,日本理学)扫描催化剂,扫描角度范围10°~80°(2θ). 扫描电子显微镜(scanning electron microscope,SEM)使用电子束轰击样品表面并捕捉散射电子,二次成像构建立体图像以获得高分辨的样品形貌信息. 本研究采用SEM(Quanta 650,美国FEI)扫描催化剂,分辨率为300 nm~10 μm. 透射电子显微镜(transmission electron microscope,TEM)使用电子束透射样品表面,由透过样品的电子束成像,获得样品表面形态,其分辨率高于SEM. 本研究采用TEM(Tecnai F30,美国FEI)扫描催化剂,分辨率为5~200 nm. 离子色谱检测用于测试固氮离子浓度,由自动进样器(Dionex AS-AP,赛默飞)、离子色谱仪(Dionex Integrion HPIC,赛默飞)和色谱分析数据软件Chromeleon组成,根据出峰时间和峰面积对样品中的离子进行定性定量检测,可以精确检测质量分数
1.3. 催化固氮实验系统
图 1
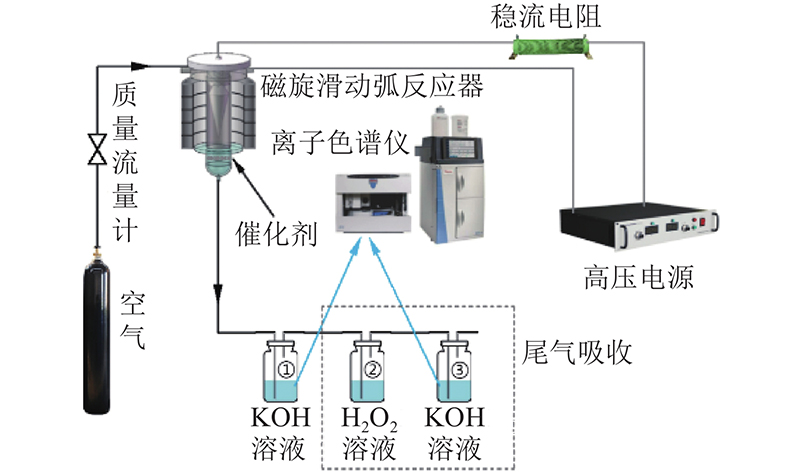
图 1 磁旋滑动弧耦合催化实验系统
Fig.1 Magnetic rotating sliding arc coupling catalytic experiment system
图 2
滑动弧放电时,由等离子体区域流出的气体流经催化床,气体中的活性物质在催化剂表面参与反应后,随气流进入洗气瓶①,与瓶中用于吸收NOx气体的溶液(简称吸收液)反应,形成含有
洗气瓶①中置100 mL KOH溶液,制取等离子体活化水的尾气先通入40 mL H2O2溶液(30%)氧化气相中的NO,再通入装有100 mL KOH溶液(0.1 mol/L)的洗气瓶③进行吸收处理.
每次实验放置5 g催化剂,每次使用磁旋滑动弧放电5 min,电源输出电压10 kV. 放电气体为空气(99.99%,杭州今工),放电气流量控制为6 L/min. 放电结束后,收集洗气瓶①中的等离子体活化水,采用离子色谱检测
1.4. 固氮效果检测
式中:
式中:
式中:
固氮能耗(MJ/mol
式中;E为每生成1 mol
2. 结果与讨论
2.1. 催化剂表征
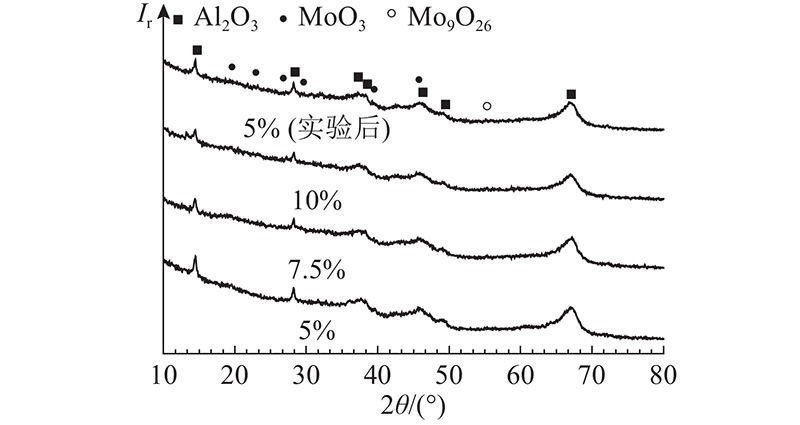
如图3所示为不同质量分数的MoO3/Al2O3的XRD图. 图中除明显的Al2O3衍射峰外,还可以观察到部分MoO3的衍射峰. 其中较为清晰的有19.45°、29.35°对应的(200)和(300)MoO3晶面(PDF#21-0569),23.33°、27.44°对应的(110)和(021)MoO3晶面(钼华,molybdite,PDF#05-0508). 结果显示MoO3/Al2O3质量分数高的样品中molybdite的峰强度高,表明molybdite数量多. 反应之后的样品中,molybdite的峰强度也较高,而低质量百分比、反应前的样品则有较强的MoO3(300)衍射峰. 这可能是在催化反应中MoO3的晶型发生转化造成的.
图 3
图 3 不同质量分数的MoO3/Al2O3 XRD图
Fig.3 XRD patterns of MoO3/Al2O3 with different mass fractions
图 4
如图5所示为透射电子显微镜(transmission electron microscope,TEM)观察到的MoO3/Al2O3表面微观结构. 可以观察到,催化剂表面分布较为均匀,虽有堆叠但片层较薄,颗粒明显. 晶格条纹呈无规则排列和堆叠状态,各区域晶格条纹间距不相同. 表明MoO3与载体混合存在且结构较为松散,颗粒可以清晰分辨. 良好的分散状态和均匀的表面分布有利于催化反应的进行.
图 5
2.2. 等离子体耦合催化实验固氮效果
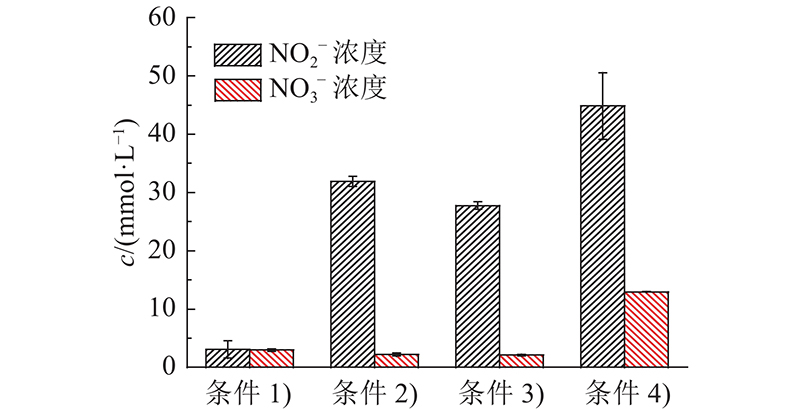
不同实验条件下的固氮效果如图6所示. 图中,c为催化反应后溶液中的离子浓度. 在使用去离子水作为吸收液并且不加入催化剂的条件1)中,生成的
图 6
图 6
不同实验条件下等离子体活化水中的
Fig.6
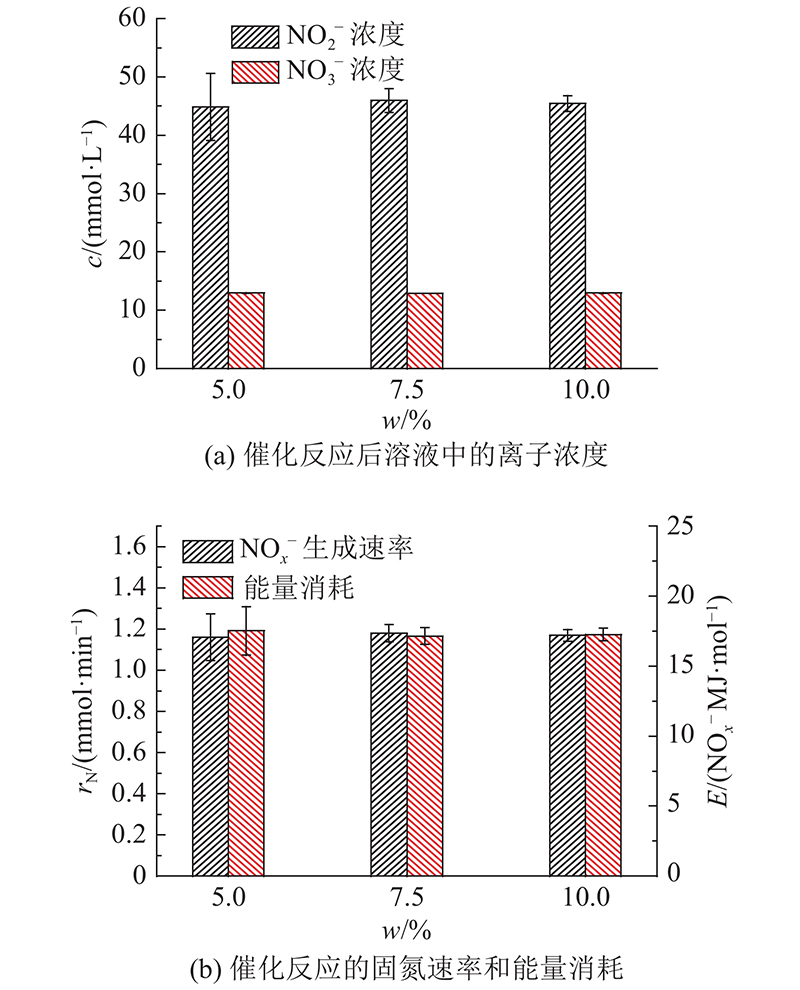
采用不同质量分数的MoO3/Al2O3作为催化剂,固氮效果如图7所示。图中w为MoO3/Al2O3的质量分数,
图 7
图 7 不同质量分数MoO3/Al2O3的等离子体耦合催化固氮效果
Fig.7 Effect of plasma coupled catalytic nitrogen fixation with different mass fractions of MoO3/Al2O3
在MoO3/Al2O3的催化下,
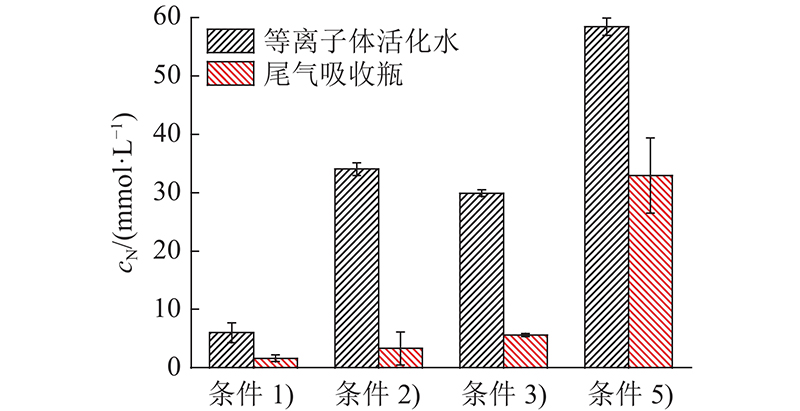
如图8所示为在不同反应条件下,检测等离子体活化水和尾气吸收瓶中的
图 8
图 8
不同反应条件下等离子体活化水和尾气吸收瓶中的
Fig.8
3. 结 论
(1)以γ-Al2O3作为催化剂基底,采用过量浸渍法制取MoO3/Al2O3作为催化剂. 研究结果表明,在MoO3/Al2O3中,MoO3与Al2O3的分离度较好,MoO3呈团簇状覆盖于载体表面,分散良好,且催化实验前后表面形貌无差异.
(2)MoO3/Al2O3拥有优良的催化效果. 一方面,MoO3的存在促进N2氧化,使产物中
(3)检测尾气吸收瓶中
(4)尾气吸收瓶中检测到浓度可观的
参考文献
A review of the existing and alternative methods for greener nitrogen fixation
[J].DOI:10.1016/j.cep.2015.02.004 [本文引用: 1]
Beyond fossil fuel–driven nitrogen transformations
[J].DOI:10.1126/science.aar6611 [本文引用: 1]
Efficient electrochemical N2 reduction to NH3 on MoN nanosheets array under ambient conditions
[J].DOI:10.1021/acssuschemeng.8b01438 [本文引用: 1]
Photocatalytic nitrogen fixation: an attractive approach for artificial photocatalysis
[J].DOI:10.1016/S1872-2067(18)63104-3 [本文引用: 1]
Regulation of biological nitrogen fixation
[J].DOI:10.1093/jn/130.5.1081 [本文引用: 1]
Ammonia synthesis on wool-like Au, Pt, Pd, Ag, or Cu electrode catalysts in nonthermal atmospheric-pressure plasma of N2 and H2
[J].DOI:10.1021/acscatal.7b01624 [本文引用: 1]
Nitrogen fixation by gliding arc plasma: better insight by chemical kinetics modelling
[J].DOI:10.1002/cssc.201700095 [本文引用: 1]
On-board plasma-assisted conversion of heavy hydrocarbons into synthesis gas
[J].DOI:10.1016/j.fuel.2009.11.039 [本文引用: 1]
Low temperature plasma-catalytic NOx synthesis in a packed DBD reactor: effect of support materials and supported active metal oxides
[J].DOI:10.1016/j.apcatb.2016.04.055 [本文引用: 1]
MoO3 nanosheets for efficient electrocatalytic N2 fixation to NH3
[J].DOI:10.1039/C8TA03974G [本文引用: 1]
Facile h-MoO3 synthesis for NH3 gas sensing application at moderate operating temperature
[J].
Plasmon-driven N2 photofixation in pure water over MoO3-x nanosheets under visible to NIR excitation
[J].
Energy cost improvement of the nitrogen oxides synthesis in a low pressure plasma
[J].
A novel preparation method of ZnO/MCM-41 for hydrogenation of methyl benzoate
[J].DOI:10.1016/S1381-1169(02)00335-7 [本文引用: 1]
MoO3-based sensor for NO, NO2 and CH4 detection
[J].DOI:10.1016/j.snb.2006.01.026 [本文引用: 1]
Nitrogen fixation in water using air phase gliding arc plasma
[J].DOI:10.1149/2.0221610jes [本文引用: 1]
In situ plasma-assisted atmospheric nitrogen fixation using water and spray-type jet plasma
[J].DOI:10.1039/C8CC00697K [本文引用: 1]
Plasma in situ gas–liquid nitrogen fixation using concentrated high-intensity electric field
[J].
Fertilization of radishes, tomatoes, and marigolds using a large-volume atmospheric glow discharge
[J].DOI:10.1007/s11090-014-9573-x [本文引用: 1]