与N、S元素相比,B的电负性更低(比碳还低). B掺杂将在石墨烯中形成p型载流子,从而改变石墨烯表面的某些物理和化学性质,使其更适合在电催化和电化学储能方面的应用[10-15]. 与未掺杂石墨烯相比,B掺杂石墨烯具有更好的多孔骨架结构和更高的导电性,作为电催化剂或电化学储锂电极材料,表现出更好的电化学性能,以及较低的电极反应电子转移阻抗. B掺杂石墨烯及其相关纳米结构对氧还原反应具有高效和较稳定的电催化活性[12-13]. 尽管B掺杂石墨烯对HER表现出较好的电催化活性,但是其Tafel斜率依然较高(99 mV/dec)[15]. B掺杂石墨烯也表现出较高的电化学储锂比容量(700~800 mA·h/g),但是在1 000 mA/g的大电流密度下,其高倍率性能只有255 mA·h/g[14].
本研究在氧化石墨烯和硼酸存在下,通过Na2MoO4与L-半胱氨酸的水热反应,制备MoS2/B掺杂石墨烯(MoS2/BG)复合纳米材料,并研究其作为HER电催化剂和电化学储锂电极材料的电化学性能.
1. 实验部分
1.1. 材料的合成
通过改进的Hummers方法制备氧化石墨烯纳米片(GOS)[5]. 复合材料的制备过程如下:将20 mL 硼酸溶液在搅拌下滴加到20 mL的GOS (3.0 mmol)悬浮液中;继续搅拌12 h后,将25mL混合溶液(含1.5 mmol Na2MoO4和7.5 mmol L-半胱氨酸)在搅拌下加入到上述混合悬浮液中;将该混合物转移到100 mL水热反应釜中,在180 °C下保温24 h;在反应完成后,将反应釜自然冷却到室温;在用去离子水洗涤5~6次后,采用离心分离得到黑色沉淀物;将其冷冻干燥48 h,得到MoS2/BG复合材料. 在水热反应混合溶液中,添加硼酸的物质的量分别为1.0、2.0、5.0 mmol,所制得的复合材料分别命名为MoS2/BG-1、MoS2/BG-2、MoS2/BG-3. 作为对比,在不添加硼酸的情况下,水热合成MoS2/G复合材料;在既没有氧化石墨烯也没有硼酸的条件下,水热制备MoS2.
1.2. 材料的表征
样品的晶体结构用X-射线衍射(X-ray diffraction,XRD)表征(UltimaIV X-射线衍射仪,Cu Kα靶, λ=0.154 056 nm). 样品的形貌用SU-8010型场发射扫描电镜表征. 采用JEM 2100F型高分辨透射电镜表征样品的微观形貌. 样品的元素及其化学态用X-射线光电子能谱表征(ESCALAB 250Xi型).
1.3. 电催化析氢性能测试
电催化HER测试采用三电极系统. Pt作为对电极,参比电极为饱和甘汞电极,电解液为0.5 mol/L的H2SO4溶液. 工作电极的制备:将4.0 mg催化剂分散在80 μL的质量分数为5%的 Nafion溶液和1.0 mL水/乙醇混合液(水/乙醇体积比为4∶1)中,超声1 h,得到均匀的催化剂浆料; 移取5.0 μL催化剂浆料涂抹在直径为3.0 mm的玻碳电极上,在60 °C下干燥后,即得到工作电极. 在CHI660E电化学工作站上,用线性扫描伏安法、循环伏安法和电化学阻抗技术测试比较催化剂的电催化析氢性能. HER的电势E均为相对于可逆氢电极(reversible hydrogen electrode, RHE)的电势(即在相对于饱和甘汞电极的电势上再加0.272 V).
1.4. 电化学储锂性能测试
以N-甲基吡咯烷酮为溶剂或分散剂,将活性物质、导电剂乙炔黑和黏合剂聚偏氟乙烯按质量比为80∶10∶10混合后研磨均匀,制得电极浆料. 将浆料涂布在铜箔上,在120 °C下真空干燥12 h后压制成工作电极. 在充满氩气的手套箱中组装成LIR 2025扣式电池进行电化学性能测试. Li片作为对电极和参比电极,聚丙烯膜(Celgard-2300)用作隔膜,电解液是1 mol/L的LiPF6的碳酸二乙酯与碳酸二甲酯(体积比为1∶1)溶液. 在室温下,恒电流充放电循环在LAND CT2001A型电池测试仪上进行.
2. 结果与讨论
2.1. 复合材料的微观结构和形貌表征
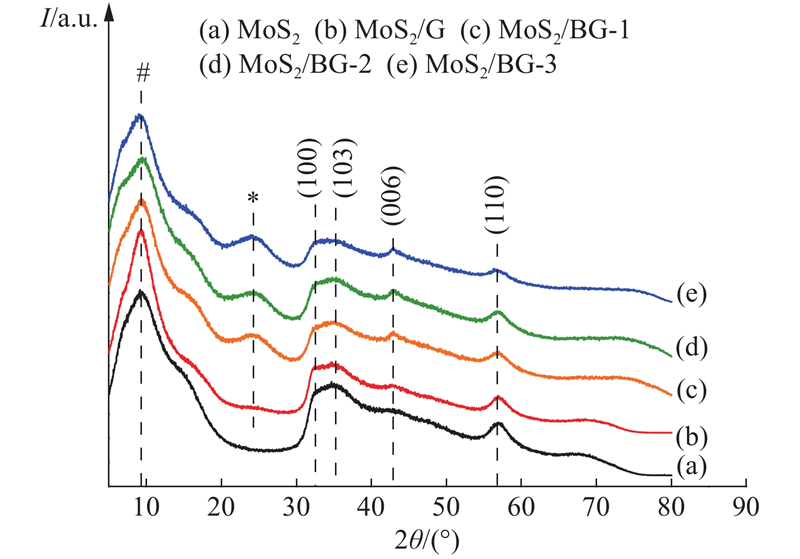
如图1所示为所制得样品的XRD图. 图中,I为衍射强度,2θ为衍射角度。可以看出,所有样品在2θ=32.8°、35.3°、43.0°、56.8°出现4个衍射峰,分别对应2H-MoS2的(100), (103), (006)和(110)晶面(JPCDS No.37-1492). 对应于MoS2的(002)面的在2θ=14.4°的衍射峰没有出现,在2θ=9.3°却出现较明显的宽化衍射峰(#标记),该峰对应的层间距为0.95 nm,明显大于MoS2 (002)面的层间距(0.62 nm). 层间距扩大主要是由于石墨烯或者其他离子的加入导致MoS2在(002)晶面的弱堆积[5, 10]. 另外,3个MoS2/BG样品在2θ=24.5°处出现弱的衍射峰,对应于石墨烯的(002)面. 这是由于B掺杂石墨烯的层与层之间π-π堆叠在一定程度上的增强[8]. Sathe等[15]认为B原子在碳晶格中形成sp2杂化,水热还原氧化石墨烯中sp2共轭结构部分恢复,改善了石墨烯片的π-π堆积或交联叠加程度.
图 1
图 2
如图3所示,用透射电子显微镜/高分辨率透射电子显微镜(transmission electron microscope/high resolution transmission electron microscope,TEM/HRTEM)进一步表征复合材料的微观结构. 如图3(a)、(b)所示,MoS2样品由MoS2纳米片交错组成,具有少层数的结构[9]. 如图3(c)、(d)所示,对于MoS2/G复合材料,MoS2纳米片能均匀地分散在石墨烯上. 如图3(e)~(j)所示,与MoS2/G和MoS2相比,MoS2/BG复合材料中MoS2纳米片具有更短的长度和更多的暴露边缘,并均匀地分散在B掺杂石墨烯上. 在水热反应溶液中添加2.0 mmol H3BO3制得的MoS2/BG-2样品,其中的MoS2的晶格条纹出现较多的无序结构或缺陷,暴露出更多的边缘或缺陷位点. 由图3还可以看出,全部样品中MoS2的层间距为0.92~0.96 nm,与其XRD分析结果一致. 对于MoS2/BG-2样品,用扫描透射电镜和电子衍射能谱进行进一步的表征. 结果表明,MoS2/BG-2样品的Mo、S、C、O和B元素的分布是均匀的.
图 3
用光电子能谱(X-ray photoelectron spectroscopy, XPS)进一步分析表征MoS2/BG-2复合材料的元素组成及其化学态. 如图4(a)所示,MoS2/BG-2样品含有Mo、S、C、B、O元素,其中O元素主要来源于石墨烯上残留的含氧官能团. 图中,EB为结合能. 对于MoS2/BG-2样品,石墨烯中B所占的原子百分比约为6.6%, Mo、S的物质的量之比为1∶2.1,符合MoS2的化学计量比.
图 4
如图4(b)所示为Mo 3d和S 2s谱,可以分解为3个峰,其中在229.2、232.1 eV的峰分别归属于Mo (IV)的3d5/2、3d3/2[6],在226.2 eV的峰归属于S 2s[6]。如图4(c)所示为S 2p的XPS谱,可以分解成5个峰,其中在161.7、162.3 eV的峰分别归属于MoS2中S2−的2p3/2、2p1/2;在163.3、164.4 eV的峰分别归属于尖端S2−配体和(或)桥接双硫S22−中的S 2p3/2、S 2p1/2;在168.6 eV处的峰归属于SO32−的S[1]. 关于MoS2的XPS表征结果和MoS2/未掺杂石墨烯复合材料中MoS2的XPS表征分析一致,说明B没有掺杂到MoS2中[16]. 如图4(d)所示为C 1s的XPS谱,可以分解成4个峰,其中在284.5、284.9、285.9、288.8 eV的峰分别对应于C=C,C—O,C=O和O—C—B/O—C=O[14]. 如图4(e)所示为B 1s的XPS图,可以分解成3个峰,在189.2、191.4、193.3 eV的峰分别对应于BC3、BC2O、BCO2[14-15, 17-18]. XPS分析较好地证明了B原子掺杂到了石墨烯的晶格中[14-15, 17-18]. 在水热过程中,B原子掺杂进石墨烯晶格的反应主要包括,当温度高于80 °C时,H3BO3经历脱水形成B2O3,B2O3在水热条件下进一步扩散到石墨烯的晶格中,相应的反应可以表示[14-15]为
2.2. 电催化HER性能
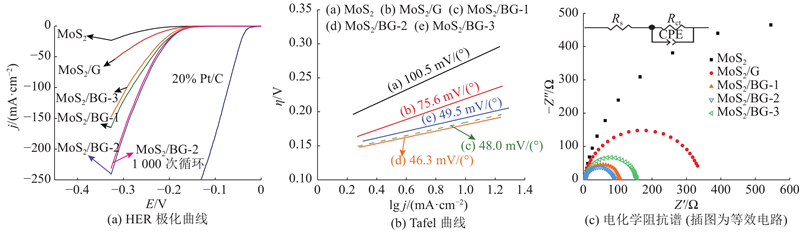
如图5(a)所示为不同催化剂修饰的玻碳电极上HER的极化曲线. 图中,j为电流密度. 商业化的Pt/C (Pt质量分数为20%)催化剂对HER有较高的电催化活性,显示了最高的HER电流密度,起始电位接近于零. MoS2催化剂表现了较高的起始过电位(185 mV),即使在300 mV的高过电位下,其电流密度仅为16 mA/cm2. 与MoS2相比,在MoS2/G催化剂上HER起始过电位降低为153 mV,电流密度也有较明显的增加,这是由于MoS2/G具有较好的导电性,并且石墨烯复合能减少MoS2纳米片的堆积,增加MoS2对HER的活性位点[4, 9]. 与MoS2/G相比,MoS2/BG的电催化HER活性有更显著的提高. 尤其是MoS2/BG-2, 其HER的起始过电位降低到130 mV,在300 mV的过电位下,其电流密度为180 mA/cm2,高于已报道的MoS2/N掺杂石墨烯的电流密度(136.3 mA/cm2)[10]. MoS2/BG的高电催化HER活性主要是由于石墨烯中B元素的掺杂. 掺杂B可以有效地调整或改变石墨烯的电子结构和表面物理化学特性,并在石墨烯表面诱导形成大量的活性(富电子)还原中心,为H+还原转化为H2提供能垒更低的途径[15]. B掺杂还增加了p型载流子的数量,改善了石墨烯中π共轭体系与孤对电子间的联系,提高了石墨烯的导电能力[14-15]. 与未掺杂石墨烯相比,B掺杂石墨烯具有更多的褶皱和更好的开放多孔骨架结构[14],在水热条件下原位生长的MoS2层能均匀地分散在这些B掺杂石墨烯上,并形成具有更多HER催化活性位的MoS2/BG复合材料. 因此,MoS2/BG复合材料比MoS2/G显示出更高的电催化HER活性. 稳定性也是评价催化剂性能的重要因素. 在0.5 mol/L H2SO4电解液中,以5 mV/s扫速用循环伏安法对MoS2/BG-2进行1 000次循环测试. 如图5(a)所示,1 000次循环后得到的HER极化曲线和初始的极化曲线几乎重合,表明在酸性电解质中MoS2/BG-2对HER的电催化性能是稳定的.
图 5
图 5 不同催化剂电极上HER的极化曲线、Tafel斜率分析以及HER电化学阻抗谱
Fig.5 Polarization curves, Tafel slopes and EIS plots of HER on different catalyst electrodes
电催化剂的活性与其电化学活性表面积(electrochemical active surface area,ECSA)密切相关,而ECSA与电催化剂的双电层电容Cdl成正比. 按文献[19]的方法,通过循环伏安法测量并计算样品的双电层电容. 其结果是,MoS2/BG-1、MoS2/BG-2、MoS2/BG-3的Cdl分别为17.1、20.2、13.1 mF/cm2,明显高于MoS2的3.4 mF/cm2和MoS2/G的5.3 mF/cm2. 在所有样品中,MoS2/BG-2催化剂表现出最大的Cdl,说明其拥有更高的电催化析氢活性位密度. 为了讨论催化剂对HER固有的催化活性,对典型样品MoS2、MoS2/G、MoS2/BG-2计算其析氢反应的转换频率(turn over frequency, TOF,代表单个活性位点每秒析出氢分子的个数), 具体计算方法见文献[20]。结果表明,MoS2/BG-2对HER的TOF显著大于MoS2的,也略大于MoS2/G的. 当过电位为300 mV时,MoS2、MoS2/G、MoS2/BG-2电极上HER的TOF分别为0.42、0.72、0.78 s−1,说明合理的硼掺杂不仅能提高MoS2基催化剂的活性位,同时也增强MoS2催化活性位的固有催化活性。
如图5(b)所示为HER极化曲线的Tafel斜率分析,进一步讨论不同电催化剂的HER性能. 图中,η为过电位. Tafel公式可以表示为η=a+blg j,b为Tafel斜率. 酸性电解液中HER包括3个基本步骤:Volmer反应(H++e→Hads, Hads为吸附氢原子),Heyrovsky反应(H++e→H2)和Tafel反应(Hads+Hads→H2)[4, 7]. 在室温下,这3个步骤的Tafel斜率分别约为120.0、40.0、30.0 mV/dec[4]. 如图5(b)所示,MoS2显示了较高的Tafel斜率(100.5 mV/dec),表明Volmer反应为其HER的速率决定步骤. 这是由于MoS2的活性位点较有限,导电性也较低,在MoS2电极上进行Volmer反应过程非常困难,导致Tafel斜率较大. MoS2/G的Tafel斜率为75.6 mV/dec,表明其HER受Volmer反应和Heyrovsky反应的混合控制. 这是由于与石墨烯的复合提高复合材料的导电能力,增加MoS2的边缘活性位点,改善HER的Volmer反应过程. MoS2/BG复合材料的Tafel斜率进一步降低到46.0~50.0 mV/dec,其中MoS2/BG-2具有最低的Tafel斜率(46.3 mV/dec),表明其HER是通过Volmer-Heyrovsky步骤进行,Heyrovsky反应为速率决定步骤. 更低的Tafel斜率是由于掺硼石墨烯独特的电子结构和表面特性,以及更多边缘或缺陷的弱堆积MoS2层均匀地负载在B掺杂石墨烯上,使复合材料催化剂具有大量电催化活性中心, 并在HER电极过程中具有更好的电子转移能力[14-15].
为了更好地理解MoS2/BG-2优异的电催化HER性能,对其进行电化学阻抗谱(electrochemical impedance spectrum,EIS)分析. 如图5(c)所示为在不同催化剂电极上HER的电化学阻抗谱图,插图为相应的等效电路. 图中,Rs为电解液电阻,Rct为电子转移阻抗,Z′为阻抗实部,Z′′为阻抗虚部,CPE为催化剂/电解液界面的恒相位元. 如表1所示为EIS数据拟合HER电化学动力学参数的结果. 由于MoS2导电性能较低,MoS2电极显示了最大的Rct(1 131 Ω). MoS2/B电极的Rct降低为339 Ω,是由于石墨烯提高了复合材料的导电性,改善HER电极过程中电子转移. MoS2/BG电极的Rct进一步降低,其中MoS2/BG-2催化剂电极显示了最小的Rct(87 Ω),为MoS2/G电极的25.6%,说明MoS2/BG-2电极上的HER具有更好的电子转移能力.
表 1 电化学阻抗拟合所得HER动力学参数
Tab.1
| 电极 | Rs/Ω | Rct/Ω |
| MoS2 | 3.2 | 1 131 |
| MoS2/G | 4.3 | 339 |
| MoS2/BG-1 | 4.8 | 104 |
| MoS2/BG-2 | 3.6 | 87 |
| MoS2/BG-5 | 4.5 | 152 |
2.3. 电化学储锂性能
如图6所示为不同复合材料电极的恒电流充放电曲线. 图中,C为比容量。如图6(a)所示为MoS2/G电极在第1次放电过程中出现2个电位平台,其中1.50 V左右的平台对应Li+插入MoS2晶格形成LixMoS2[10,21],0.75 V的平台对应于转换反应:LixMoS2+(4−x)Li→Mo+2Li2S[10];0.60 V以下的斜坡区段归属于锂储存在Mo纳米簇与Li2S的界面相或缺陷位处[5]. 在充电过程中,MoS2/G电极在1.85、2.25 V出现2个电位平台,分别归属于锂离子从Mo与Li2S界面相或缺陷位处的移除,以及Li2S的脱锂(Li2S−2e=S+2Li+)[10,21]. 在第1次充放电循环后,复合材料中MoS2已经主要转化成Mo纳米簇和S[9]. 在第2、3次放电过程中,1.50 V左右的平台对应于S的锂化生成Li2S,0.70 V以下的斜线区段归属于锂储存在Mo/Li2S的界面相或材料的缺陷位处[5]. 如图6(b)所示为MoS2/BG-2复合材料电极的前3圈充放电曲线,其充放电电位平台的特征与MoS2/G电极充放电曲线类似. MoS2/G和MoS2/BG-2电极的前3圈充放电曲线电位平台也与文献报道的MoS2基复合材料电化学储锂的循环伏安曲线特征相符合[5,21]. 如图6所示,MoS2/G电极的首次电化学储锂比容量和可逆比容量分别为1 395、1 023 mA·h/g,库仑效率为73.2%;MoS2/BG-2电极首次储锂比容量和可逆比容量分别为1 593、1 205 mA·h/g,库仑效率为75.6%. 首次充放电容量的损失主要是由于固体电解质界面膜(solid electrolyte interphase,SEI)膜的形成,以及部分不可逆锂的损失和其他不可逆电极反应[5,21]. 在第2、3次充放电循环时,MoS2/G电极的库仑效率分别为95.6%、96.3%;MoS2/BG-2电极的库仑效率分别为95.5%、96.5%.
图 6
图 6 不同复合材料电极前3个循环的充放电曲线 (电流密度为100 mA/g)
Fig.6 Charge-discharge curves of different composite electrodes for first three cycles at 100 mA/g
如图7(a)所示为不同复合材料电极的电化学储锂比容量C随循环次数n的变化. 当电流密度为100 mA/g时,MoS2/G的电化学储锂初始可逆比容量为1 023 mA·h/g,100次循环后降低到715 mA·h/g. 与之相比,MoS2/BG显示了更高的电化学储锂可逆比容量和更稳定的循环性能. MoS2/BG-2电极的初始可逆比容量为1 205 mA·h/g,在100次循环后依然保持有1 153 mA·h/g,说明其循环性能稳定. 在第4次充放电循环以后,不同电极的库仑效率都大于97.0%. 如图7(b)所示,与MoS2/G相比,MoS2/BG-2电极表现出明显增强的高倍率充放电特性. 在不同电流密度下充放电循环30次后,MoS2/BG-2电极在1 000 mA/g电流密度的倍率特性为836 mA·h/g,明显大于MoS2/G的581 mA·h/g. 当电流密度重新回到100 mA/g时,MoS2/BG-2电极的储锂比容量基本恢复到初始值. 如图7(b)所示,MoS2/BG-2在不同充放电电流密度下循环100次后,依然保持有1 161 mA·h/g的可逆比容量,明显大于MoS2/G的687 mA·h/g,说明与MoS2/G相比,MoS2/BG-2不仅具有更高倍率充放电特性,并具有更稳定的循环性能.
图 7
图 7 不同复合材料电极的充放电循环性能及其倍率特性
Fig.7 Cycling behavior of different composite electrodes and their rate capability
3. 结 语
在氧化石墨烯和硼酸存在下,通过一步水热反应法制备MoS2/BG复合材料. 在水热条件下氧化石墨烯可以被还原,同时被硼酸释放的B原子掺杂. MoS2层可以在硼掺杂的石墨烯表面选择性地生长和均匀地分散,并显示弱堆积和缺陷较多的微观结构. 与MoS2/G相比,MoS2/BG复合材料显示出更好的电催化HER性能和电化学储锂性能. 尤其是MoS2/BG-2具有较高的电催化HER活性,以及较低的Tafel斜率(46.3 mV/dec). 作为电化学储锂电极材料,MoS2/BG-2不仅具有较高的储锂可逆比容量(1 205 mA·h·g−1),并显示出稳定的循环性能和明显增强的高倍率充放电特性. MoS2/BG-2复合材料优异的电化学性能主要是由于石墨烯的硼掺杂改变了其电子性质和表面特性,以及弱堆积和无序结构较多的MoS2层均匀地分散在硼掺杂石墨烯表面,增加了电催化HER的活性位点和电化学储锂能力,并降低电极反应过程中电子转移阻抗,增强了其电极反应的动力学性能. 这种具有优异电化学性能的MoS2/BG复合材料为低成本的HER电催化剂的研发和高性能电化学储锂电极材料的研发及其在电化学储能和能源转化中的应用提供新的思路.
参考文献
Ultrathin MoS2nanoplates with rich active sites as highly efficient catalyst for hydrogen evolution
[J].DOI:10.1021/am404843b [本文引用: 3]
Superior stability and high capacity of restacked molybdenum disulfide as anode material for lithium ion batteries
[J].DOI:10.1039/B920277C [本文引用: 1]
Exfoliated MoS2 nanocomposite as an anode material forlithium ion batteries
[J].DOI:10.1021/cm101254j [本文引用: 1]
MoS2 nanoparticles grown on graphene: an advanced catalyst for the hydrogen evolution reaction
[J].DOI:10.1021/ja201269b [本文引用: 4]
L-cysteine-assisted synthesis of layered MoS2/graphene composites with excellent electrochemical performances for lithium ion batteries
[J].DOI:10.1021/nn200659w [本文引用: 6]
Facile synthesis of low crystalline MoS2 nanosheet-coated CNTs for enhanced hydrogen evolution reaction
[J].DOI:10.1039/c3nr02994h [本文引用: 2]
Ni 掺杂MoS2/石墨烯催化剂的制备及其电催化析氢活性
[J].
Synthesis of Ni-doped MoS2/graphene hybrids and their electrocatalytic activity for hydrogen evolution reaction
[J].
Heteroatom-doped graphene-based materials for energy-relevant electrocatalytic processes
[J].DOI:10.1021/acscatal.5b00991 [本文引用: 4]
MoS2/sulfur and nitrogen co-doped reduced graphene oxide nanocomposite for enhanced electrocatalytic hydrogen evolution
[J].DOI:10.1016/j.ijhydene.2015.11.114 [本文引用: 4]
Facile synthesis of molybdenum disulfide/nitrogen-doped graphene composites for enhanced electrocatalytic hydrogen evolution and electrochemical lithium storage
[J].DOI:10.1016/j.carbon.2016.06.074 [本文引用: 8]
Generation of b-doped graphene nanoplatelets using a solution process and their supercapacitor applications
[J].
Synthesis of boron doped graphene for oxygen reduction reaction in fuel cells
[J].DOI:10.1039/C1JM14694G [本文引用: 1]
Two-dimensional boron-doped graphyne nanosheet: a new metal-free catalyst for oxygen evolution reaction
[J].DOI:10.1016/j.carbon.2017.08.003 [本文引用: 1]
Green synthesis of boron doped graphene and its application as high performance anode material in Li ion battery
[J].DOI:10.1016/j.materresbull.2014.10.049 [本文引用: 9]
Metal-free B-doped graphene with efficient electrocatalytic activity for hydrogen evolution reaction
[J].DOI:10.1039/C4CY00075G [本文引用: 9]
Ionic-liquid mediated synthesis of molybdenum disulfide/graphene composites: an enhanced electrochemical hydrogen evolution catalyst
[J].DOI:10.1016/j.ijhydene.2016.05.186 [本文引用: 1]
Synthesis, structure, and properties of boron- and nitrogen-doped graphene
[J].
Facile synthesis of boron-doped porous carbon as anode for lithium–ion batteries with excellent electrochemical performance
[J].DOI:10.1007/s11581-018-2647-7 [本文引用: 2]
Ni掺杂MoS2/石墨烯催化剂的制备及其电催化析氢活性
[J].DOI:10.3785/j.issn.1008-973X.2019.08.020 [本文引用: 1]
Synthesis of Ni-doped MoS2/graphene hybrids and their electrocatalytic activity for hydrogen evolution reaction
[J].DOI:10.3785/j.issn.1008-973X.2019.08.020 [本文引用: 1]
Phase engineering of a multiphasic 1T/2H MoS2 catalyst for highly efficient hydrogen evolution
[J].DOI:10.1039/C6TA09409K [本文引用: 1]
Cationic surfactant-assisted hydrothermal synthesis of few-layerMoS2/graphene composites: microstructure and electrochemical lithium storage
[J].