本文链接 :https://www.zjujournals.com/gcsjxb/CN/10.3785/j.issn.1006-754X.2024.03.202
皮肤作为人体最大的器官,具有很多重要功能:1)充当人体与外部环境之间的物理屏障;2)作为温度调节系统;3)排放代谢产物,以调节人体的健康状况[1 ] 。热力、化学物质、电击或机械性外力易造成皮肤大面积损伤,引起皮肤组织破坏与缺失,这类伤口难以愈合。这种长期难以愈合的伤口会给患者带来巨大的身体和心理负担以及经济压力[2 ] 。世界卫生组织2023年的统计报告显示:低收入和中等收入国家每年死于烧伤的人数高达18万。目前,临床上常采用自体皮肤移植术和伤口敷料进行皮肤大面积损伤修复。自体皮肤移植是指从患者未受损伤的部位取皮并覆盖至受损部位。然而,皮肤移植治疗会造成新的皮肤损伤,且当患者皮肤受损面积过大时,其自身未受损皮肤面积有限,无法满足皮肤移植的需求。而伤口敷料必须具备良好的机械强度和透气性、一定的生物活性和吸水性能、适宜的生物相容性以及降解性能。用于制备伤口敷料的材料有很多,最常用的是一些天然聚合物、合成聚合物以及纳米复合材料[3 ] 。天然聚合物中常用于制备伤口敷料的材料为壳聚糖和明胶。其中:壳聚糖具有出色的生物相容性和生物降解性,有助于细胞黏附、增殖和分化,但单一壳聚糖的机械性能较差,拉伸时易断裂,挤压时易变形[4 ] ;明胶可以很好地保持水分,有利于细胞黏附,且其含有丰富的胶原蛋白,可为细胞的生长提供营养物质[5 ] 。在合成聚合物以及纳米复合材料中,常用于制备伤口敷料的材料为纳米黏土,由其生成的水凝胶敷料具有良好的机械性能和耐热性能,但该类伤口敷料含有不可降解的纳米微粒,不利于伤口恢复。此外,合成聚合物以及纳米复合材料的优缺点单一,极大地限制了治疗效果[6 ] 。
生物3D打印作为一种创新性的医疗手段[7 ] ,已成为受损皮肤修复的新途径之一,推动了生物医药行业的发展[8 -9 ] 。生物3D打印技术具有细胞打印定位精确、细胞活性高及制造效率高等特点[10 ] 。按打印方式的不同,生物3D打印可分为激光打印、喷墨打印和挤出式打印三种。其中,喷墨打印技术通过热、压电或声学驱动等方式将细胞悬浮液滴沉积在目标位置处[11 ] ,以在液体基质中打印出高分辨率的图案化细胞结构[12 ] 。基于喷墨打印技术打印的水凝胶3D结构带有大量细胞,可加快受损皮肤愈合[13 ] ,其在组织工程中得到了广泛应用。
原位皮肤打印技术是根据患者皮肤受损处的形态,直接在受损部位进行生物3D打印,以修复受损组织[14 ] 。多伦多大学的Hakimi等[15 ] 研制了一种手持式皮肤打印机,该打印机的多喷头结构可打印出多种不同种类的细胞,从而形成多种皮肤组织形态。杭州捷诺飞生物科技有限公司的赵占盈等[16 ] 自主研发了Regenovo生物3D打印机,该打印机的运动精度为20 μ m [17 ] 所研制的嵌入式3D打印平台的工作空间为230 mm×300 mm,打印精度为100~400 μ m μ m [18 ] 研制了一款工作空间为100 mm×100 mm×50 mm的生物打印平台,并通过打印硅胶材料开展了切片参数优化实验,确定了合适的打印工艺参数。
根据《人体损伤程度鉴定标准》,一级轻伤的判定标准包括头皮创口或瘢痕长度累计超过20 cm。现有的生物打印机无法满足皮肤大面积打印的需求。此外,现有的生物打印机多为三轴打印机,无法满足皮肤曲面随形打印的需求,且运动精度也不符合皮肤原位打印的要求。针对以上问题,笔者团队开发了一款原位皮肤打印系统,并对其工作空间进行分析,旨在为实现皮肤大面积损伤修复提供参考。
1 原位皮肤打印系统结构设计
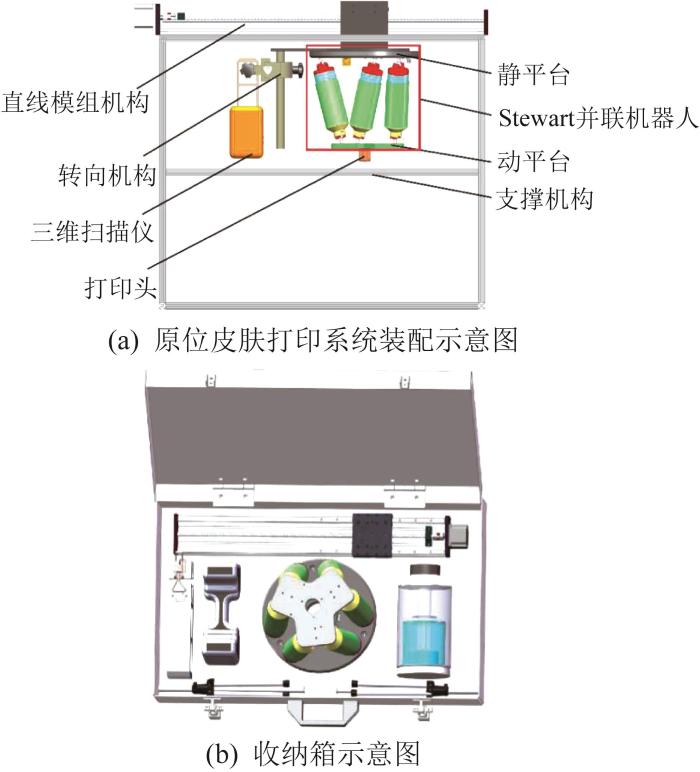
本文所设计的原位皮肤打印系统主要由直线模组机构、转向机构、三维扫描仪、Stewart并联机器人、打印头和支撑机构等组成。其中,Stewart并联机器人的运动姿态灵活,可满足打印系统沿皮肤受损表面随形打印的需求。该打印系统的工作原理如下:首先,利用三维扫描仪对受损皮肤进行扫描,以获取受损部位的高分辨率图像信息;然后,通过图像识别算法来识别所获取图像的轮廓和深度,并利用CAD(computer aided design,计算机辅助设计)技术对轮廓进行实体化与分层处理,以生成打印路径;最后,利用并联机器人驱动打印头在受损部位进行打印,实现对受损部位的修复。利用SolidWorks软件对原位皮肤打印系统进行建模设计,其结构装配如图1 (a)所示。该打印系统利用铝型材框架作为支撑机构,直线模组机构固定在支撑机构上方;Stewart并联机器人安装在直线模组机构下方,并通过连接件与三维扫描仪相连;打印头固定在并联机器人动平台一端,其在动平台驱动下进行随形打印,以实现对受损皮肤的修复。其中,直线模组机构可有效扩大整个打印系统的工作范围;转向机构可使三维扫描仪转换方向,实现对伤口的全方位扫描。所设计的原位皮肤打印系统采用负压打印方式,其储料仓顶部固定在Stewart并联机器人的静平台上,储料仓底部直接与打印头相连,模块化设计缩小了储料仓与打印头之间的距离,节省了打印材料。此外,为满足现场救治的需求,可采用三脚架代替铝型材框架作为打印系统的支撑机构。同时,打印系统的整套设备可放入图1 (b)所示的收纳箱中,方便携带,且收纳箱中配有便携式液氮罐。在皮肤损伤修复前,将液氮罐中的生物墨水取出,并使用由便携式USB(universal serial bus,通用串行总线)电池供电的微型加热垫解冻至37 ℃。
图1
图1
原位皮肤打印系统及其收纳箱示意图
Fig.1
Schematic of in situ skin printing system and its storage box
2 Stewart 并联机器人的结构与运动学分析
2.1 并联机器人结构与自由度分析
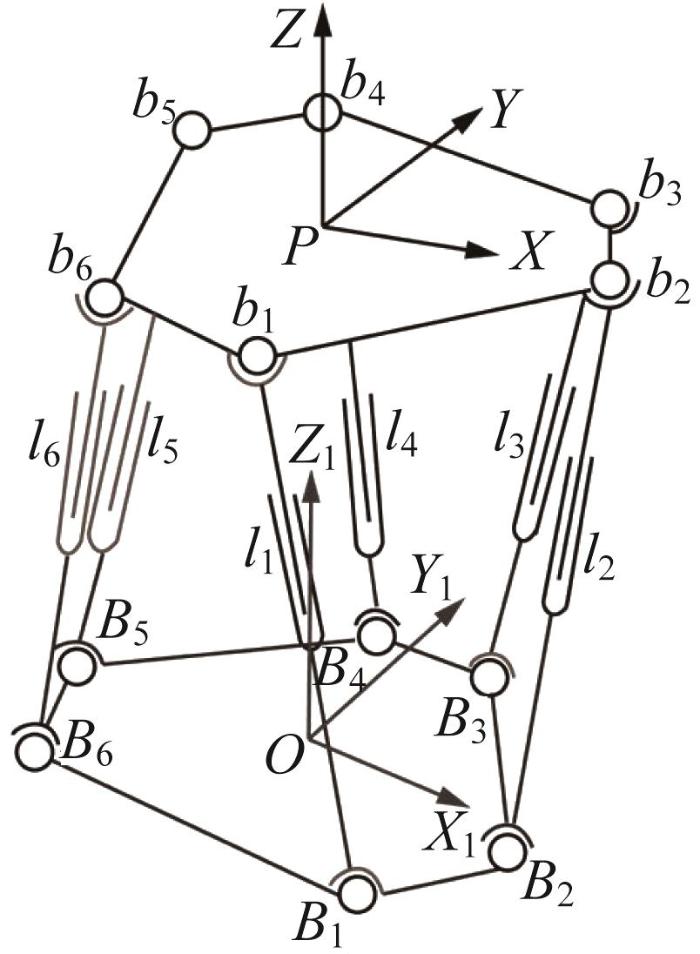
原位皮肤打印系统中Stewart并联机器人的结构简图如图2 所示,其主要由动平台、连杆、球副、滑块、静平台和直线驱动器等零部件组成。
图2
图2
Stewart 并联机器人结构简图
Fig.2
Structure diagram of Stewart parallel robot
Stewart并联机器人共有6条运动支链,每条运动支链的两端通过球副分别与动、静平台相连接。直线驱动器通过驱动运动支链,使并联机器人动平台完成平移和旋转运动。并联机器人自由度W 的计算式如下:
W = 6 n - p 1 + 2 p 2 + 3 p 3 + 4 p 4 + 5 p 5 = 6 n - ∑ i = 1 5 i p i (1)
式中:n 为活动构件数量,p i 为 i
Stewart并联机器人的活动构件数量n =13,其直线驱动器的运动副为圆柱副,圆柱副属于空间IV级副,IV级副的相对自由度p 4 =18。Stewart并联机器人中不存在局部自由度和虚约束构件,根据式(1),计算得到其自由度:
W = 6 × 13 - 4 × 18 = 6 (2)
由此可知,Stewart并联机器人具有6个自由度,其动平台可沿X 、Y 、Z 三个方向进行平移和旋转运动。在并联机器人动平台驱动下,打印头可进行平移与旋转,充分利用角度调整来提高曲面打印精度,从而实现高适配性的随形打印,推进皮肤大面积损伤的个性化修复。
2.2 并联机器人运动学分析
2.2.1 坐标平移变换
在Stewart并联机器人动平台高度不变的条件下,动平台从初始位置沿直线向任意方向平移到某一位置,假设沿X 、Y 、Z 方向分别平移了r 、q 、s ,则动平台上某点沿3个方向的平移齐次变换可表示为:
X C = 1 0 0 r 0 1 0 0 0 0 1 0 0 0 0 1 Y C = 1 0 0 0 0 1 0 q 0 0 1 0 0 0 0 1 Z C = 1 0 0 0 0 1 0 0 0 0 1 s 0 0 0 1
式中: X C Y C Z C X 、Y 、Z 方向的平移矩阵。
C = X C Y C Z C = 1 0 0 r 0 1 0 q 0 0 1 s 0 0 0 1 (3)
利用三维扫描仪对伤口进行扫描,将伤口路径转化为G代码后,Stewart并联机器人的动平台根据G代码分别沿X 、Y 、Z 方向作平移运动,以带动打印头平移,完成皮肤的原位打印。
2.2.2 坐标旋转变换
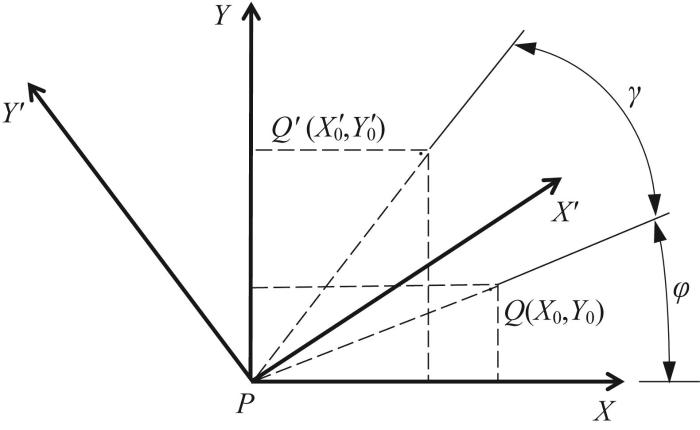
在Stewart并联机器人动平台中心保持位置不变的条件下,动平台朝任意方向旋转某一角度,6条运动支链的长度随动平台转角的变化而变化。图3 所示为动平台上某点坐标的旋转变换示意。图中:P -XY 为动平台旋转前的原始坐标系,P -X ' Y ' Z 轴旋转γ
图3
图3
坐标旋转变换示意
Fig.3
Schematic of coordinate rotation transformation
根据图3 ,动平台旋转后Q ' X 0 ' Y 0 ' Z 0 ' ) 可表示为:
X 0 ' Y 0 ' Z 0 ' = c o s γ - s i n γ 0 s i n γ c o s γ 0 0 0 1 X 0 Y 0 Z 0 (4)
R Z , γ = c o s γ - s i n γ 0 s i n γ c o s γ 0 0 0 1
式中:(X 0 , Y 0 , Z 0 )为旋转前Q 点的坐标, R Z , γ Z 轴旋转γ 时对应的旋转矩阵。
同理,动平台绕X 轴旋转α 和绕Y 轴旋转β 时的旋转矩阵 R X , α R Y , β
R X , α = 1 0 0 0 c o s α - s i n α 0 s i n α c o s α
R Y , β = c o s β 0 s i n β 0 1 0 - s i n β 0 c o s β
由此可得,坐标系P -XY 与P -X ' Y ' R
R = R X , α R Y , β R Z , γ = c o s β c o s γ s i n α s i n β c o s γ - c o s α s i n γ s i n α s i n γ + c o s α c o s γ s i n β c o s β s i n γ c o s α c o s γ + s i n α s i n β s i n γ c o s α s i n β s i n γ - s i n α c o s γ - s i n β s i n α c o s β c o s α c o s β (5)
因皮肤伤口多为不规则形状,Stewart并联机器人动平台需通过旋转来调整角度,以驱动打印头沿伤口法向进行曲面随形打印,使得生物墨水完整地覆盖在皮肤损伤处,以更好地促进伤口恢复。
2.2.3 并联机器人位置正解
通过上文分析可知,确定Stewart并联机器人动平台位姿的独立参数有6个,分别为确定动平台位置的 X C Y C Z C α 、 β 、 γ
b j = B j X C , Y C , Z C , α , β , γ , j = 1 , 2 , ⋯ , 6
式中: b j bj 的位姿向量, B j Bj 的位姿向量。
在给定6个直线驱动器位移l j j = 1 , 2 , ⋯ , 6
l j 2 = b j - B j T b j - B j (6)
式(6)为含有6个未知数、6个非线性方程的方程组,可利用最小二乘法进行求解,建立如下目标函数:
F X C , Y C , Z C , α , β , γ = ∑ j = 1 6 l j - b j - B j T b j - B j 2 (7)
利用式(7)可以求解得到动平台的位姿参数,为后续求解Stewart并联机器人的工作空间提供了理论基础。
3 原位皮肤打印系统工作空间分析
3.1 并联机器人工作空间数值求解
分析原位皮肤打印系统的工作空间时需考虑以下2种情况:1)直线模组机构固定,仅依靠Stewart并联机器人的平移和旋转进行打印;2)直线模组机构工作,通过直线模组机构和Stewart并联机器人的联合运动进行打印。并联机器人动平台的操作范围即为其工作空间,工作空间是评估并联机器人功能的关键指标之一[19 -20 ] 。并联机器人工作空间的主要影响因素包括连杆长度、关节转角及连杆间距等。常用的并联机器人工作空间计算方法包括解析法和数值法。其中:解析法是一种基于数学模型的方法,从并联机器人的几何和运动学关系出发,推导出工作空间边界的函数表达式,但由于所推导的函数表达式过于烦琐,解析法不具有通用性[21 ] ;数值法是指利用计算机算法,先通过迭代计算搜索并联机器人动平台的可达区域,再通过求解运动学方程来计算工作空间的边界[22 -25 ] 。数值法运算简单,适用于多种并联机构。基于此,本文采用数值法来求解直线模组机构固定时Stewart并联机器人的工作空间。先利用Python程序遍历并联机器人运动支链与静平台角度的所有组合,随后通过正运动学运算得到所有组合对应的位置正解,剔除不符合要求的位置后,剩余位置对应点的集群即构成了并联机器人的工作空间。
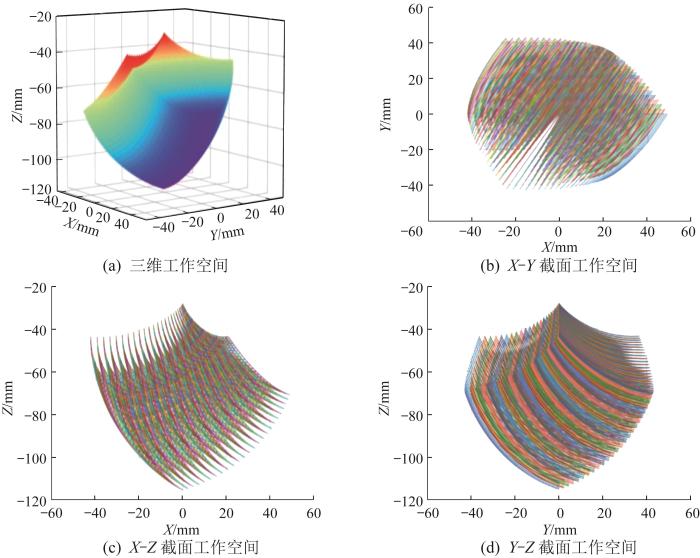
图4 所示为直线模组机构固定时Stewart并联机器人工作空间的数值求解结果。由图4 (a)可以看出,该并联机器人动平台的工作空间在三维空间中呈倒立的非旋转体锥形,具有良好的连续性;由图4 (b)可以看出,在直线模组机构固定的情况下,该并联机器人沿X 方向的移动距离为91 mm,沿Y 方向的移动距离为84 mm。
图4
图4
Stewart 并联机器人工作空间
Fig.4
Workspace of Stewart parallel robot
3.2 原位皮肤打印系统工作空间仿真分析
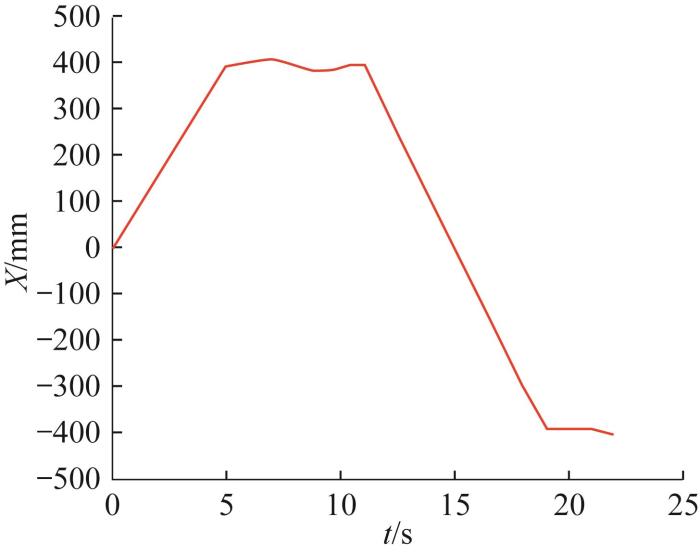
为了得到直线模组机构工作时整个原位皮肤打印系统的工作空间,在ADAMS仿真软件中构建原位皮肤打印系统仿真模型(对结构作一定简化)并开展工作空间分析。如图5 所示,将原位皮肤打印系统各部分赋予材料属性,并设置连接副和驱动副;设仿真时间为23 s。通过仿真分析得到了直线模组机构与Stewart并联机器人联合运动时打印头质心沿X 方向的移动距离,结果如图6 所示。
图5
图5
原位皮肤打印系统仿真模型
Fig.5
Simulation model of in situ skin printing system
图6
图6
打印头质心沿 X
Fig.6
Movement distance of print head centroid along X direction
根据图6 ,打印头质心在第5秒时到达X =400 mm处,在第19秒时到达X =-400 mm处。由此可知,打印头质心沿X 方向的移动距离达到了800 mm。结合图4 和图6 可知,在直线模组机构固定时,原位皮肤打印系统的工作空间可达到80 mm×80 mm×50 mm;在直线模组机构工作时,打印系统的工作空间可达到800 mm×80 mm×50 mm。
4 打印实验
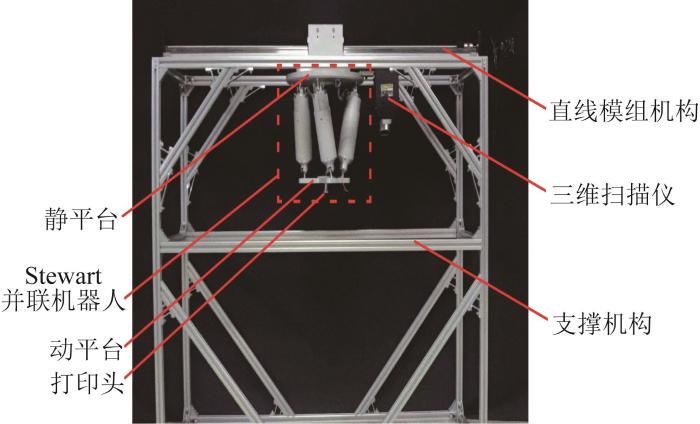
为验证原位皮肤打印系统打印过程的稳定性以及其工作空间仿真结果的准确性,开展打印实验。原位皮肤打印系统样机如图7 所示。在实验过程中,为了保证Stewart并联机器人的工作空间,先使用Inkscape软件将半径为40 mm的圆形图案以及SIA(中国科学院沈阳自动化研究所)和SUT(沈阳工业大学)两组字母图案生成G代码,再将G代码传输至打印系统以驱动并联机器人运动,打印头在并联机器人的驱动下打印圆形图案和字母图案,最后通过对比各组图案来分析并联机器人的工作空间。将图案转化为G代码后,使用MATLAB软件进行可视化处理,如图8 (a)所示。结果表明,转化后的G代码连续性良好,可保证打印路径的准确性。将G代码传输至打印系统后,利用加入红色墨水的3%海藻酸钠溶液(生物相容性良好,且具有高剪切稀化和快速胶凝性能)进行打印,打印效果如图8 (b)所示。结果显示,在打印过程中,Stewart并联机器人运动平稳,无卡顿现象;打印头可平稳打印,且液滴喷射均匀;并联机器人动平台的运动轨迹与G代码对应的期望轨迹相符,打印出的点阵图案与软件生成图案相同,且打印范围与并联机器人工作空间仿真结果相符,进一步验证了原位皮肤打印系统实现大面积皮肤损伤修复的可行性。
图7
图7
原位皮肤打印系统样机
Fig.7
In situ skin printing system prototype
图8
图8
海藻酸钠打印实验结果对比
Fig.8
Comparison of sodium alginate printing experiment results
为了进一步测试原位皮肤打印系统对不同生物墨水的打印性能,配置浓度为5%的明胶溶液并开展打印实验。为了方便观察,加入蓝色墨水,打印图案为螺旋线;为了满足大面积原位覆盖的需求,调整打印参数,以实现连续线条打印。设置打印底板平台的温度为-10 ℃,以保证明胶可在底板平台上更好地固化。明胶打印实验结果如图9 所示。结果显示,螺旋线粗细均匀且打印线条连续,即打印过程未出现中断现象,说明原位皮肤打印系统对不同生物墨水具有较强的适应性。
图9
图9
明胶打印实验结果
Fig.9
Gelatin printing experiment result
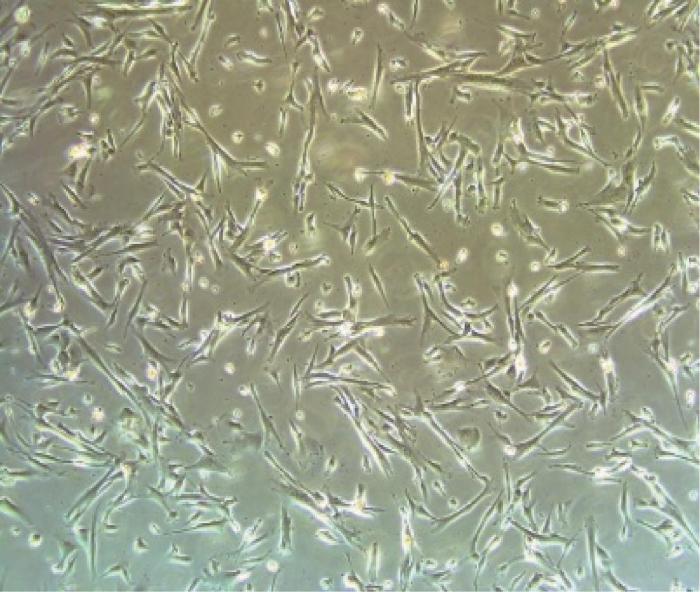
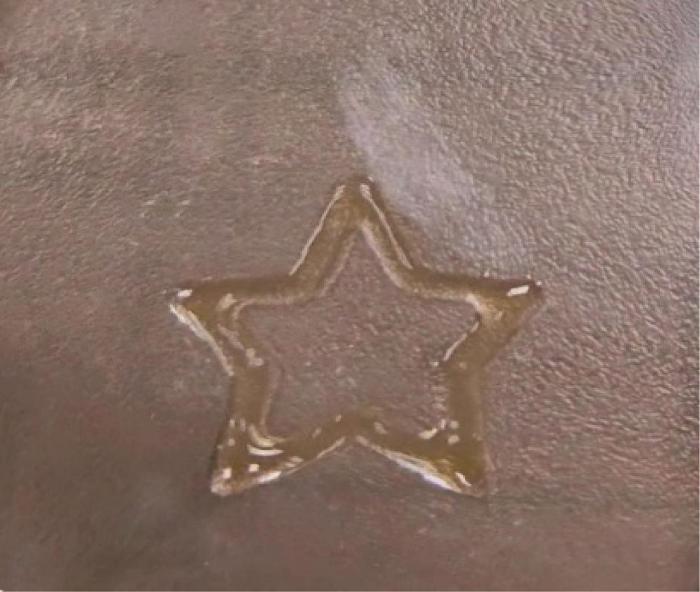
为了验证原位皮肤打印系统进行生物打印的可行性,开展细胞打印实验。首先,培养平滑肌细胞。图10 所示为平滑肌细胞培养2 d后贴壁生长的形态。利用显微镜进行观察发现,平滑肌细胞生长良好,未受到细菌污染。然后,对原位皮肤打印系统进行消毒。其中,储料仓和管路使用酒精浸泡消毒,其余机构利用紫外线照射消毒。待平滑肌细胞达到一定数量后,配置GelMA生物墨水,并将平滑肌细胞混入GelMA溶液以进行打印。在打印前,对混合溶液进行细胞浓度测试,结果显示,细胞浓度为1.28×105 个/mL。利用混合溶液打印五角星图案,打印结果如图11 所示。在打印出五角星图案后,使用紫外线照射图案20 s,以使图案更好地固化在培养皿中。利用扫描电镜观察培养皿中的固化图案,发现平滑肌细胞均匀地分布在五角星内部,如图12 所示。向培养皿中加入培养基,并将其放入培养箱进行培养。经过24 h的培养后,细胞成活率达到92%,由此说明原位皮肤打印系统可用于生物打印。
图10
图10
平滑肌细胞形态
Fig.10
Smooth muscle cell morphology
图11
图11
细胞打印实验结果
Fig.11
Cell printing experiment result
图12
图12
打印后平滑肌细胞分布情况
Fig.12
Distribution of smooth muscle cells after printing
5 结 论
针对皮肤大面积损伤修复问题,本文设计了一款原位皮肤打印系统,有效解决了现有生物打印设备打印范围小及打印精度低的问题。通过数值法对Stewart并联机器人的工作空间进行分析,得到了直线模组机构固定时原位皮肤打印系统的工作空间;通过ADAMS仿真分析得到了直线模组机构和并联机器人联合运动时该打印系统的工作空间。最后,通过打印实验验证了原位皮肤打印系统的可行性以及工作空间仿真分析结果的准确性。仿真结果表明,当直线模组机构固定时,原位皮肤打印系统可实现80 mm×80 mm×50 mm的打印范围;当直线模组机构与并联机器人联合运动时,该打印系统可实现800 mm×80 mm×50 mm的打印范围,可满足皮肤大面积损伤修复的需求。实验结果表明,原位皮肤打印系统中的并联机器人可按指定路径运行,打印头可稳定、均匀地喷射不同的生物墨水,这可为后续皮肤大面积修复动物实验奠定基础。
参考文献
View Option
[1]
STANTON D N GANGULI-INDRA G INDRA A K et al Bioengineered efficacy models of skin disease: advances in the last 10 years
[J]. Pharmaceutics , 2022 , 14 (2 ): 319 .
[本文引用: 1]
[2]
CHOUHAN D DEY N BHARDWAJ N et al Emerging and innovative approaches for wound healing and skin regeneration: current status and advances
[J]. Biomaterials , 2019 , 216 : 119267 .
[本文引用: 1]
[3]
ZENG D SHEN S H FAN D D Molecular design, synthesis strategies and recent advances of hydrogels for wound dressing applications
[J]. Chinese Journal of Chemical Engineering , 2021 , 30 : 308 -320 .
[本文引用: 1]
[4]
PISANI S DORATI R SCOCOZZA F et al Preliminary investigation on a new natural based poly (gamma-glutamic acid)/Chitosan bioink
[J]. Journal of Biomedical Materials Research Part B: Applied Biomaterials , 2020 , 108 (7 ): 2718 -2732 .
[本文引用: 1]
[5]
NOROUZI M BOROUJENI S M OMIDVARKOR DSHOULI N et al Advances in skin regeneration: application of electrospun scaffolds
[J]. Advanced Healthcare Materials , 2015 , 4 (8 ): 1114 -1133 .
[本文引用: 1]
[6]
王瑞 生物3D打印技术构建dECM基人工皮肤的研究
[D].泉州 :华侨大学 ,2021 .
[本文引用: 1]
WANG R Research on 3D bioprinting technology to construct dECM-based artificial skin
[D]. Quanzhou : Huaqiao University , 2021 .
[本文引用: 1]
[7]
MURPHY S V ATALA A 3D bioprinting of tissues and organs
[J]. Nature Biotechnology , 2014 , 32 : 773 -785 .
[本文引用: 1]
[8]
TSENG H GAGE J A HAISLER W L et al A high-throughput in vitro ring assay for vasoactivity using magnetic 3D bioprinting
[J]. Scientific Reports , 2016 , 6 : 30640 .
[本文引用: 1]
[9]
OZBOLAT I T Bioprinting scale-up tissue and organ constructs for transplantation
[J]. Trends in Biotechnology , 2015 , 33 (7 ): 395 -400 .
[本文引用: 1]
[10]
NG W L WANG S YEONG W Y et al Skin bioprinting: impending reality or fantasy?
[J]. Trends in Biotechnology , 2016 , 34 (9 ): 689 -699 .
[本文引用: 1]
[11]
PARK J A LEE H R PARK S Y et al Self-organization of fibroblast-laden 3D collagen microstructures from inkjet-printed cell patterns
[J]. Advanced Biosystems , 2020 , 4 (5 ): 1900280 .
[本文引用: 1]
[12]
PARK J A YOON S KWON J et al Freeform micropatterning of living cells into cell culture medium using direct inkjet printing
[J]. Scientific Reports , 2017 , 7 : 14610 .
[本文引用: 1]
[13]
YOON S PARK J A LEE H R et al Inkjet-spray hybrid printing for 3D freeform fabrication of multilayered hydrogel structures
[J]. Advanced Healthcare Materials , 2018 , 7 (14 ): e1800050 .
[本文引用: 1]
[14]
连伟龙 ,连芩 ,焦天 ,等 皮肤修复生物3D打印的研究进展与挑战
[J].光电工程 ,2021 ,48 (8 ):210105 .
[本文引用: 1]
LIAN W L LIAN Q JIAO T et al The research progress and challenge of 3D bioprinting for skin repairing
[J]. Opto-Electronic Engineering , 2021 , 48 (8 ): 210105 .
[本文引用: 1]
[15]
HAKIMI N CHENG R LENG L et al Handheld skin printer: in situ formation of planar biomaterials and tissues
[J]. Lab on a Chip , 2018 , 18 (10 ): 1440 -1451 .
[本文引用: 1]
[16]
赵占盈 ,徐铭恩 ,石然 ,等 基于细胞3D打印技术的肿瘤药物筛选细胞芯片研究
[J].中国生物医学工程学报 ,2014 ,33 (2 ):161 -169 .
[本文引用: 1]
ZHAO Z Y XU M E SHI R et al Research of anti-tumor drug screening cell chip based on 3D cell printing technique
[J]. Chinese Journal of Biomedical Engineering , 2014 , 33 (2 ): 161 -169 .
[本文引用: 1]
[17]
张伟 面向软体机器人的软材料嵌入式3D打印基础研究
[D].苏州 :苏州大学 ,2021 .
[本文引用: 1]
ZHANG W Experimental research on embedded 3D printing technology with soft materials for soft robotics
[D]. Suzhou : Soochow University , 2021 .
[本文引用: 1]
[18]
王润秋 模拟生物软组织应变硬化特性的超材料结构设计与3D打印方法研究
[D].杭州 :浙江大学 ,2020 .
[本文引用: 1]
WANG R Q Research on metamaterial structure design and 3D printing method for simulating strain-stiffening property of biological soft tissue
[D]. Hangzhou : Zhejiang University , 2020 .
[本文引用: 1]
[19]
蔡自兴 机器人学 [M].2版 .北京 :清华大学出版社 ,2009 :1 -30 .
[本文引用: 1]
CAI Z X Robotics [M]. 2nd ed . Beijing : Tsinghua University Press , 2009 : 1 -30 .
[本文引用: 1]
[20]
黄真 ,赵永生 ,赵铁石 高等空间机构学 [M].2版 .北京 :高等教育出版社 ,2014 :159 -184 .
[本文引用: 1]
HUANG Z ZHAO Y S ZHAO T S Advanced spatial mechanism [M]. 2nd ed . Beijing : Higher Education Press , 2014 : 159 -184 .
[本文引用: 1]
[21]
WANG Y J FANG C JIANG Q M Singularity-free workspace of parallel robots
[J]. Advances in Robotics & Automation , 2015 , 4 (2 ): 1000122 .
[本文引用: 1]
[22]
吴生富 ,王洪波 ,黄真 并联机器人工作空间的研究
[J].机器人 ,1991 ,13 (3 ):33 -39 .
[本文引用: 1]
WU S F WANG H B HUANG Z Study of workspace in parallel robot manipulator
[J]. Robot , 1991 , 13 (3 ): 33 -39 .
[本文引用: 1]
[23]
KUMAR V Characterization of workspaces of parallel manipulators
[J]. Journal of Mechanical Design , 1992 , 114 (3 ): 368 -375 .
[24]
魏修亭 ,李刚 ,杜强 ,等 6-PTRT型齿顶倒角机器人运动学及工作空间分析
[J].中国机械工程 ,2013 ,24 (6 ):750 -754 .
WEI X T LI G DU Q et al Kinematic analysis and workspace calculation of a 6-PTRT manipulator for chamfering gear addendum
[J]. China Mechanical Engineering , 2013 , 24 (6 ): 750 -754
[25]
于晖 ,孙立宁 ,刘品宽 ,等 新型 6-HTRT 并联机器人工作空间和参数研究
[J].机器人 ,2002 ,24 (4 ):293 -298 ,313 .
[本文引用: 1]
YU H SUN L N LIU P K et al Study on the workspace and parameter of novel 6-HTRT parallel robot
[J]. Robot , 2002 , 24 (4 ): 293 -298 , 313 .
[本文引用: 1]
Bioengineered efficacy models of skin disease: advances in the last 10 years
1
2022
... 皮肤作为人体最大的器官,具有很多重要功能:1)充当人体与外部环境之间的物理屏障;2)作为温度调节系统;3)排放代谢产物,以调节人体的健康状况[1 ] .热力、化学物质、电击或机械性外力易造成皮肤大面积损伤,引起皮肤组织破坏与缺失,这类伤口难以愈合.这种长期难以愈合的伤口会给患者带来巨大的身体和心理负担以及经济压力[2 ] .世界卫生组织2023年的统计报告显示:低收入和中等收入国家每年死于烧伤的人数高达18万.目前,临床上常采用自体皮肤移植术和伤口敷料进行皮肤大面积损伤修复.自体皮肤移植是指从患者未受损伤的部位取皮并覆盖至受损部位.然而,皮肤移植治疗会造成新的皮肤损伤,且当患者皮肤受损面积过大时,其自身未受损皮肤面积有限,无法满足皮肤移植的需求.而伤口敷料必须具备良好的机械强度和透气性、一定的生物活性和吸水性能、适宜的生物相容性以及降解性能.用于制备伤口敷料的材料有很多,最常用的是一些天然聚合物、合成聚合物以及纳米复合材料[3 ] .天然聚合物中常用于制备伤口敷料的材料为壳聚糖和明胶.其中:壳聚糖具有出色的生物相容性和生物降解性,有助于细胞黏附、增殖和分化,但单一壳聚糖的机械性能较差,拉伸时易断裂,挤压时易变形[4 ] ;明胶可以很好地保持水分,有利于细胞黏附,且其含有丰富的胶原蛋白,可为细胞的生长提供营养物质[5 ] .在合成聚合物以及纳米复合材料中,常用于制备伤口敷料的材料为纳米黏土,由其生成的水凝胶敷料具有良好的机械性能和耐热性能,但该类伤口敷料含有不可降解的纳米微粒,不利于伤口恢复.此外,合成聚合物以及纳米复合材料的优缺点单一,极大地限制了治疗效果[6 ] . ...
Emerging and innovative approaches for wound healing and skin regeneration: current status and advances
1
2019
... 皮肤作为人体最大的器官,具有很多重要功能:1)充当人体与外部环境之间的物理屏障;2)作为温度调节系统;3)排放代谢产物,以调节人体的健康状况[1 ] .热力、化学物质、电击或机械性外力易造成皮肤大面积损伤,引起皮肤组织破坏与缺失,这类伤口难以愈合.这种长期难以愈合的伤口会给患者带来巨大的身体和心理负担以及经济压力[2 ] .世界卫生组织2023年的统计报告显示:低收入和中等收入国家每年死于烧伤的人数高达18万.目前,临床上常采用自体皮肤移植术和伤口敷料进行皮肤大面积损伤修复.自体皮肤移植是指从患者未受损伤的部位取皮并覆盖至受损部位.然而,皮肤移植治疗会造成新的皮肤损伤,且当患者皮肤受损面积过大时,其自身未受损皮肤面积有限,无法满足皮肤移植的需求.而伤口敷料必须具备良好的机械强度和透气性、一定的生物活性和吸水性能、适宜的生物相容性以及降解性能.用于制备伤口敷料的材料有很多,最常用的是一些天然聚合物、合成聚合物以及纳米复合材料[3 ] .天然聚合物中常用于制备伤口敷料的材料为壳聚糖和明胶.其中:壳聚糖具有出色的生物相容性和生物降解性,有助于细胞黏附、增殖和分化,但单一壳聚糖的机械性能较差,拉伸时易断裂,挤压时易变形[4 ] ;明胶可以很好地保持水分,有利于细胞黏附,且其含有丰富的胶原蛋白,可为细胞的生长提供营养物质[5 ] .在合成聚合物以及纳米复合材料中,常用于制备伤口敷料的材料为纳米黏土,由其生成的水凝胶敷料具有良好的机械性能和耐热性能,但该类伤口敷料含有不可降解的纳米微粒,不利于伤口恢复.此外,合成聚合物以及纳米复合材料的优缺点单一,极大地限制了治疗效果[6 ] . ...
Molecular design, synthesis strategies and recent advances of hydrogels for wound dressing applications
1
2021
... 皮肤作为人体最大的器官,具有很多重要功能:1)充当人体与外部环境之间的物理屏障;2)作为温度调节系统;3)排放代谢产物,以调节人体的健康状况[1 ] .热力、化学物质、电击或机械性外力易造成皮肤大面积损伤,引起皮肤组织破坏与缺失,这类伤口难以愈合.这种长期难以愈合的伤口会给患者带来巨大的身体和心理负担以及经济压力[2 ] .世界卫生组织2023年的统计报告显示:低收入和中等收入国家每年死于烧伤的人数高达18万.目前,临床上常采用自体皮肤移植术和伤口敷料进行皮肤大面积损伤修复.自体皮肤移植是指从患者未受损伤的部位取皮并覆盖至受损部位.然而,皮肤移植治疗会造成新的皮肤损伤,且当患者皮肤受损面积过大时,其自身未受损皮肤面积有限,无法满足皮肤移植的需求.而伤口敷料必须具备良好的机械强度和透气性、一定的生物活性和吸水性能、适宜的生物相容性以及降解性能.用于制备伤口敷料的材料有很多,最常用的是一些天然聚合物、合成聚合物以及纳米复合材料[3 ] .天然聚合物中常用于制备伤口敷料的材料为壳聚糖和明胶.其中:壳聚糖具有出色的生物相容性和生物降解性,有助于细胞黏附、增殖和分化,但单一壳聚糖的机械性能较差,拉伸时易断裂,挤压时易变形[4 ] ;明胶可以很好地保持水分,有利于细胞黏附,且其含有丰富的胶原蛋白,可为细胞的生长提供营养物质[5 ] .在合成聚合物以及纳米复合材料中,常用于制备伤口敷料的材料为纳米黏土,由其生成的水凝胶敷料具有良好的机械性能和耐热性能,但该类伤口敷料含有不可降解的纳米微粒,不利于伤口恢复.此外,合成聚合物以及纳米复合材料的优缺点单一,极大地限制了治疗效果[6 ] . ...
Preliminary investigation on a new natural based poly (gamma-glutamic acid)/Chitosan bioink
1
2020
... 皮肤作为人体最大的器官,具有很多重要功能:1)充当人体与外部环境之间的物理屏障;2)作为温度调节系统;3)排放代谢产物,以调节人体的健康状况[1 ] .热力、化学物质、电击或机械性外力易造成皮肤大面积损伤,引起皮肤组织破坏与缺失,这类伤口难以愈合.这种长期难以愈合的伤口会给患者带来巨大的身体和心理负担以及经济压力[2 ] .世界卫生组织2023年的统计报告显示:低收入和中等收入国家每年死于烧伤的人数高达18万.目前,临床上常采用自体皮肤移植术和伤口敷料进行皮肤大面积损伤修复.自体皮肤移植是指从患者未受损伤的部位取皮并覆盖至受损部位.然而,皮肤移植治疗会造成新的皮肤损伤,且当患者皮肤受损面积过大时,其自身未受损皮肤面积有限,无法满足皮肤移植的需求.而伤口敷料必须具备良好的机械强度和透气性、一定的生物活性和吸水性能、适宜的生物相容性以及降解性能.用于制备伤口敷料的材料有很多,最常用的是一些天然聚合物、合成聚合物以及纳米复合材料[3 ] .天然聚合物中常用于制备伤口敷料的材料为壳聚糖和明胶.其中:壳聚糖具有出色的生物相容性和生物降解性,有助于细胞黏附、增殖和分化,但单一壳聚糖的机械性能较差,拉伸时易断裂,挤压时易变形[4 ] ;明胶可以很好地保持水分,有利于细胞黏附,且其含有丰富的胶原蛋白,可为细胞的生长提供营养物质[5 ] .在合成聚合物以及纳米复合材料中,常用于制备伤口敷料的材料为纳米黏土,由其生成的水凝胶敷料具有良好的机械性能和耐热性能,但该类伤口敷料含有不可降解的纳米微粒,不利于伤口恢复.此外,合成聚合物以及纳米复合材料的优缺点单一,极大地限制了治疗效果[6 ] . ...
Advances in skin regeneration: application of electrospun scaffolds
1
2015
... 皮肤作为人体最大的器官,具有很多重要功能:1)充当人体与外部环境之间的物理屏障;2)作为温度调节系统;3)排放代谢产物,以调节人体的健康状况[1 ] .热力、化学物质、电击或机械性外力易造成皮肤大面积损伤,引起皮肤组织破坏与缺失,这类伤口难以愈合.这种长期难以愈合的伤口会给患者带来巨大的身体和心理负担以及经济压力[2 ] .世界卫生组织2023年的统计报告显示:低收入和中等收入国家每年死于烧伤的人数高达18万.目前,临床上常采用自体皮肤移植术和伤口敷料进行皮肤大面积损伤修复.自体皮肤移植是指从患者未受损伤的部位取皮并覆盖至受损部位.然而,皮肤移植治疗会造成新的皮肤损伤,且当患者皮肤受损面积过大时,其自身未受损皮肤面积有限,无法满足皮肤移植的需求.而伤口敷料必须具备良好的机械强度和透气性、一定的生物活性和吸水性能、适宜的生物相容性以及降解性能.用于制备伤口敷料的材料有很多,最常用的是一些天然聚合物、合成聚合物以及纳米复合材料[3 ] .天然聚合物中常用于制备伤口敷料的材料为壳聚糖和明胶.其中:壳聚糖具有出色的生物相容性和生物降解性,有助于细胞黏附、增殖和分化,但单一壳聚糖的机械性能较差,拉伸时易断裂,挤压时易变形[4 ] ;明胶可以很好地保持水分,有利于细胞黏附,且其含有丰富的胶原蛋白,可为细胞的生长提供营养物质[5 ] .在合成聚合物以及纳米复合材料中,常用于制备伤口敷料的材料为纳米黏土,由其生成的水凝胶敷料具有良好的机械性能和耐热性能,但该类伤口敷料含有不可降解的纳米微粒,不利于伤口恢复.此外,合成聚合物以及纳米复合材料的优缺点单一,极大地限制了治疗效果[6 ] . ...
生物3D打印技术构建dECM基人工皮肤的研究
1
2021
... 皮肤作为人体最大的器官,具有很多重要功能:1)充当人体与外部环境之间的物理屏障;2)作为温度调节系统;3)排放代谢产物,以调节人体的健康状况[1 ] .热力、化学物质、电击或机械性外力易造成皮肤大面积损伤,引起皮肤组织破坏与缺失,这类伤口难以愈合.这种长期难以愈合的伤口会给患者带来巨大的身体和心理负担以及经济压力[2 ] .世界卫生组织2023年的统计报告显示:低收入和中等收入国家每年死于烧伤的人数高达18万.目前,临床上常采用自体皮肤移植术和伤口敷料进行皮肤大面积损伤修复.自体皮肤移植是指从患者未受损伤的部位取皮并覆盖至受损部位.然而,皮肤移植治疗会造成新的皮肤损伤,且当患者皮肤受损面积过大时,其自身未受损皮肤面积有限,无法满足皮肤移植的需求.而伤口敷料必须具备良好的机械强度和透气性、一定的生物活性和吸水性能、适宜的生物相容性以及降解性能.用于制备伤口敷料的材料有很多,最常用的是一些天然聚合物、合成聚合物以及纳米复合材料[3 ] .天然聚合物中常用于制备伤口敷料的材料为壳聚糖和明胶.其中:壳聚糖具有出色的生物相容性和生物降解性,有助于细胞黏附、增殖和分化,但单一壳聚糖的机械性能较差,拉伸时易断裂,挤压时易变形[4 ] ;明胶可以很好地保持水分,有利于细胞黏附,且其含有丰富的胶原蛋白,可为细胞的生长提供营养物质[5 ] .在合成聚合物以及纳米复合材料中,常用于制备伤口敷料的材料为纳米黏土,由其生成的水凝胶敷料具有良好的机械性能和耐热性能,但该类伤口敷料含有不可降解的纳米微粒,不利于伤口恢复.此外,合成聚合物以及纳米复合材料的优缺点单一,极大地限制了治疗效果[6 ] . ...
生物3D打印技术构建dECM基人工皮肤的研究
1
2021
... 皮肤作为人体最大的器官,具有很多重要功能:1)充当人体与外部环境之间的物理屏障;2)作为温度调节系统;3)排放代谢产物,以调节人体的健康状况[1 ] .热力、化学物质、电击或机械性外力易造成皮肤大面积损伤,引起皮肤组织破坏与缺失,这类伤口难以愈合.这种长期难以愈合的伤口会给患者带来巨大的身体和心理负担以及经济压力[2 ] .世界卫生组织2023年的统计报告显示:低收入和中等收入国家每年死于烧伤的人数高达18万.目前,临床上常采用自体皮肤移植术和伤口敷料进行皮肤大面积损伤修复.自体皮肤移植是指从患者未受损伤的部位取皮并覆盖至受损部位.然而,皮肤移植治疗会造成新的皮肤损伤,且当患者皮肤受损面积过大时,其自身未受损皮肤面积有限,无法满足皮肤移植的需求.而伤口敷料必须具备良好的机械强度和透气性、一定的生物活性和吸水性能、适宜的生物相容性以及降解性能.用于制备伤口敷料的材料有很多,最常用的是一些天然聚合物、合成聚合物以及纳米复合材料[3 ] .天然聚合物中常用于制备伤口敷料的材料为壳聚糖和明胶.其中:壳聚糖具有出色的生物相容性和生物降解性,有助于细胞黏附、增殖和分化,但单一壳聚糖的机械性能较差,拉伸时易断裂,挤压时易变形[4 ] ;明胶可以很好地保持水分,有利于细胞黏附,且其含有丰富的胶原蛋白,可为细胞的生长提供营养物质[5 ] .在合成聚合物以及纳米复合材料中,常用于制备伤口敷料的材料为纳米黏土,由其生成的水凝胶敷料具有良好的机械性能和耐热性能,但该类伤口敷料含有不可降解的纳米微粒,不利于伤口恢复.此外,合成聚合物以及纳米复合材料的优缺点单一,极大地限制了治疗效果[6 ] . ...
3D bioprinting of tissues and organs
1
2014
... 生物3D打印作为一种创新性的医疗手段[7 ] ,已成为受损皮肤修复的新途径之一,推动了生物医药行业的发展[8 -9 ] .生物3D打印技术具有细胞打印定位精确、细胞活性高及制造效率高等特点[10 ] .按打印方式的不同,生物3D打印可分为激光打印、喷墨打印和挤出式打印三种.其中,喷墨打印技术通过热、压电或声学驱动等方式将细胞悬浮液滴沉积在目标位置处[11 ] ,以在液体基质中打印出高分辨率的图案化细胞结构[12 ] .基于喷墨打印技术打印的水凝胶3D结构带有大量细胞,可加快受损皮肤愈合[13 ] ,其在组织工程中得到了广泛应用. ...
A high-throughput in vitro ring assay for vasoactivity using magnetic 3D bioprinting
1
2016
... 生物3D打印作为一种创新性的医疗手段[7 ] ,已成为受损皮肤修复的新途径之一,推动了生物医药行业的发展[8 -9 ] .生物3D打印技术具有细胞打印定位精确、细胞活性高及制造效率高等特点[10 ] .按打印方式的不同,生物3D打印可分为激光打印、喷墨打印和挤出式打印三种.其中,喷墨打印技术通过热、压电或声学驱动等方式将细胞悬浮液滴沉积在目标位置处[11 ] ,以在液体基质中打印出高分辨率的图案化细胞结构[12 ] .基于喷墨打印技术打印的水凝胶3D结构带有大量细胞,可加快受损皮肤愈合[13 ] ,其在组织工程中得到了广泛应用. ...
Bioprinting scale-up tissue and organ constructs for transplantation
1
2015
... 生物3D打印作为一种创新性的医疗手段[7 ] ,已成为受损皮肤修复的新途径之一,推动了生物医药行业的发展[8 -9 ] .生物3D打印技术具有细胞打印定位精确、细胞活性高及制造效率高等特点[10 ] .按打印方式的不同,生物3D打印可分为激光打印、喷墨打印和挤出式打印三种.其中,喷墨打印技术通过热、压电或声学驱动等方式将细胞悬浮液滴沉积在目标位置处[11 ] ,以在液体基质中打印出高分辨率的图案化细胞结构[12 ] .基于喷墨打印技术打印的水凝胶3D结构带有大量细胞,可加快受损皮肤愈合[13 ] ,其在组织工程中得到了广泛应用. ...
Skin bioprinting: impending reality or fantasy?
1
2016
... 生物3D打印作为一种创新性的医疗手段[7 ] ,已成为受损皮肤修复的新途径之一,推动了生物医药行业的发展[8 -9 ] .生物3D打印技术具有细胞打印定位精确、细胞活性高及制造效率高等特点[10 ] .按打印方式的不同,生物3D打印可分为激光打印、喷墨打印和挤出式打印三种.其中,喷墨打印技术通过热、压电或声学驱动等方式将细胞悬浮液滴沉积在目标位置处[11 ] ,以在液体基质中打印出高分辨率的图案化细胞结构[12 ] .基于喷墨打印技术打印的水凝胶3D结构带有大量细胞,可加快受损皮肤愈合[13 ] ,其在组织工程中得到了广泛应用. ...
Self-organization of fibroblast-laden 3D collagen microstructures from inkjet-printed cell patterns
1
2020
... 生物3D打印作为一种创新性的医疗手段[7 ] ,已成为受损皮肤修复的新途径之一,推动了生物医药行业的发展[8 -9 ] .生物3D打印技术具有细胞打印定位精确、细胞活性高及制造效率高等特点[10 ] .按打印方式的不同,生物3D打印可分为激光打印、喷墨打印和挤出式打印三种.其中,喷墨打印技术通过热、压电或声学驱动等方式将细胞悬浮液滴沉积在目标位置处[11 ] ,以在液体基质中打印出高分辨率的图案化细胞结构[12 ] .基于喷墨打印技术打印的水凝胶3D结构带有大量细胞,可加快受损皮肤愈合[13 ] ,其在组织工程中得到了广泛应用. ...
Freeform micropatterning of living cells into cell culture medium using direct inkjet printing
1
2017
... 生物3D打印作为一种创新性的医疗手段[7 ] ,已成为受损皮肤修复的新途径之一,推动了生物医药行业的发展[8 -9 ] .生物3D打印技术具有细胞打印定位精确、细胞活性高及制造效率高等特点[10 ] .按打印方式的不同,生物3D打印可分为激光打印、喷墨打印和挤出式打印三种.其中,喷墨打印技术通过热、压电或声学驱动等方式将细胞悬浮液滴沉积在目标位置处[11 ] ,以在液体基质中打印出高分辨率的图案化细胞结构[12 ] .基于喷墨打印技术打印的水凝胶3D结构带有大量细胞,可加快受损皮肤愈合[13 ] ,其在组织工程中得到了广泛应用. ...
Inkjet-spray hybrid printing for 3D freeform fabrication of multilayered hydrogel structures
1
2018
... 生物3D打印作为一种创新性的医疗手段[7 ] ,已成为受损皮肤修复的新途径之一,推动了生物医药行业的发展[8 -9 ] .生物3D打印技术具有细胞打印定位精确、细胞活性高及制造效率高等特点[10 ] .按打印方式的不同,生物3D打印可分为激光打印、喷墨打印和挤出式打印三种.其中,喷墨打印技术通过热、压电或声学驱动等方式将细胞悬浮液滴沉积在目标位置处[11 ] ,以在液体基质中打印出高分辨率的图案化细胞结构[12 ] .基于喷墨打印技术打印的水凝胶3D结构带有大量细胞,可加快受损皮肤愈合[13 ] ,其在组织工程中得到了广泛应用. ...
皮肤修复生物3D打印的研究进展与挑战
1
2021
... 原位皮肤打印技术是根据患者皮肤受损处的形态,直接在受损部位进行生物3D打印,以修复受损组织[14 ] .多伦多大学的Hakimi等[15 ] 研制了一种手持式皮肤打印机,该打印机的多喷头结构可打印出多种不同种类的细胞,从而形成多种皮肤组织形态.杭州捷诺飞生物科技有限公司的赵占盈等[16 ] 自主研发了Regenovo生物3D打印机,该打印机的运动精度为20 μ m [17 ] 所研制的嵌入式3D打印平台的工作空间为230 mm×300 mm,打印精度为100~400 μ m μ m . 浙江大学的王润秋[18 ] 研制了一款工作空间为100 mm×100 mm×50 mm的生物打印平台,并通过打印硅胶材料开展了切片参数优化实验,确定了合适的打印工艺参数. ...
皮肤修复生物3D打印的研究进展与挑战
1
2021
... 原位皮肤打印技术是根据患者皮肤受损处的形态,直接在受损部位进行生物3D打印,以修复受损组织[14 ] .多伦多大学的Hakimi等[15 ] 研制了一种手持式皮肤打印机,该打印机的多喷头结构可打印出多种不同种类的细胞,从而形成多种皮肤组织形态.杭州捷诺飞生物科技有限公司的赵占盈等[16 ] 自主研发了Regenovo生物3D打印机,该打印机的运动精度为20 μ m [17 ] 所研制的嵌入式3D打印平台的工作空间为230 mm×300 mm,打印精度为100~400 μ m μ m . 浙江大学的王润秋[18 ] 研制了一款工作空间为100 mm×100 mm×50 mm的生物打印平台,并通过打印硅胶材料开展了切片参数优化实验,确定了合适的打印工艺参数. ...
Handheld skin printer: in situ formation of planar biomaterials and tissues
1
2018
... 原位皮肤打印技术是根据患者皮肤受损处的形态,直接在受损部位进行生物3D打印,以修复受损组织[14 ] .多伦多大学的Hakimi等[15 ] 研制了一种手持式皮肤打印机,该打印机的多喷头结构可打印出多种不同种类的细胞,从而形成多种皮肤组织形态.杭州捷诺飞生物科技有限公司的赵占盈等[16 ] 自主研发了Regenovo生物3D打印机,该打印机的运动精度为20 μ m [17 ] 所研制的嵌入式3D打印平台的工作空间为230 mm×300 mm,打印精度为100~400 μ m μ m . 浙江大学的王润秋[18 ] 研制了一款工作空间为100 mm×100 mm×50 mm的生物打印平台,并通过打印硅胶材料开展了切片参数优化实验,确定了合适的打印工艺参数. ...
基于细胞3D打印技术的肿瘤药物筛选细胞芯片研究
1
2014
... 原位皮肤打印技术是根据患者皮肤受损处的形态,直接在受损部位进行生物3D打印,以修复受损组织[14 ] .多伦多大学的Hakimi等[15 ] 研制了一种手持式皮肤打印机,该打印机的多喷头结构可打印出多种不同种类的细胞,从而形成多种皮肤组织形态.杭州捷诺飞生物科技有限公司的赵占盈等[16 ] 自主研发了Regenovo生物3D打印机,该打印机的运动精度为20 μ m [17 ] 所研制的嵌入式3D打印平台的工作空间为230 mm×300 mm,打印精度为100~400 μ m μ m . 浙江大学的王润秋[18 ] 研制了一款工作空间为100 mm×100 mm×50 mm的生物打印平台,并通过打印硅胶材料开展了切片参数优化实验,确定了合适的打印工艺参数. ...
基于细胞3D打印技术的肿瘤药物筛选细胞芯片研究
1
2014
... 原位皮肤打印技术是根据患者皮肤受损处的形态,直接在受损部位进行生物3D打印,以修复受损组织[14 ] .多伦多大学的Hakimi等[15 ] 研制了一种手持式皮肤打印机,该打印机的多喷头结构可打印出多种不同种类的细胞,从而形成多种皮肤组织形态.杭州捷诺飞生物科技有限公司的赵占盈等[16 ] 自主研发了Regenovo生物3D打印机,该打印机的运动精度为20 μ m [17 ] 所研制的嵌入式3D打印平台的工作空间为230 mm×300 mm,打印精度为100~400 μ m μ m . 浙江大学的王润秋[18 ] 研制了一款工作空间为100 mm×100 mm×50 mm的生物打印平台,并通过打印硅胶材料开展了切片参数优化实验,确定了合适的打印工艺参数. ...
面向软体机器人的软材料嵌入式3D打印基础研究
1
2021
... 原位皮肤打印技术是根据患者皮肤受损处的形态,直接在受损部位进行生物3D打印,以修复受损组织[14 ] .多伦多大学的Hakimi等[15 ] 研制了一种手持式皮肤打印机,该打印机的多喷头结构可打印出多种不同种类的细胞,从而形成多种皮肤组织形态.杭州捷诺飞生物科技有限公司的赵占盈等[16 ] 自主研发了Regenovo生物3D打印机,该打印机的运动精度为20 μ m [17 ] 所研制的嵌入式3D打印平台的工作空间为230 mm×300 mm,打印精度为100~400 μ m μ m . 浙江大学的王润秋[18 ] 研制了一款工作空间为100 mm×100 mm×50 mm的生物打印平台,并通过打印硅胶材料开展了切片参数优化实验,确定了合适的打印工艺参数. ...
面向软体机器人的软材料嵌入式3D打印基础研究
1
2021
... 原位皮肤打印技术是根据患者皮肤受损处的形态,直接在受损部位进行生物3D打印,以修复受损组织[14 ] .多伦多大学的Hakimi等[15 ] 研制了一种手持式皮肤打印机,该打印机的多喷头结构可打印出多种不同种类的细胞,从而形成多种皮肤组织形态.杭州捷诺飞生物科技有限公司的赵占盈等[16 ] 自主研发了Regenovo生物3D打印机,该打印机的运动精度为20 μ m [17 ] 所研制的嵌入式3D打印平台的工作空间为230 mm×300 mm,打印精度为100~400 μ m μ m . 浙江大学的王润秋[18 ] 研制了一款工作空间为100 mm×100 mm×50 mm的生物打印平台,并通过打印硅胶材料开展了切片参数优化实验,确定了合适的打印工艺参数. ...
模拟生物软组织应变硬化特性的超材料结构设计与3D打印方法研究
1
2020
... 原位皮肤打印技术是根据患者皮肤受损处的形态,直接在受损部位进行生物3D打印,以修复受损组织[14 ] .多伦多大学的Hakimi等[15 ] 研制了一种手持式皮肤打印机,该打印机的多喷头结构可打印出多种不同种类的细胞,从而形成多种皮肤组织形态.杭州捷诺飞生物科技有限公司的赵占盈等[16 ] 自主研发了Regenovo生物3D打印机,该打印机的运动精度为20 μ m [17 ] 所研制的嵌入式3D打印平台的工作空间为230 mm×300 mm,打印精度为100~400 μ m μ m . 浙江大学的王润秋[18 ] 研制了一款工作空间为100 mm×100 mm×50 mm的生物打印平台,并通过打印硅胶材料开展了切片参数优化实验,确定了合适的打印工艺参数. ...
模拟生物软组织应变硬化特性的超材料结构设计与3D打印方法研究
1
2020
... 原位皮肤打印技术是根据患者皮肤受损处的形态,直接在受损部位进行生物3D打印,以修复受损组织[14 ] .多伦多大学的Hakimi等[15 ] 研制了一种手持式皮肤打印机,该打印机的多喷头结构可打印出多种不同种类的细胞,从而形成多种皮肤组织形态.杭州捷诺飞生物科技有限公司的赵占盈等[16 ] 自主研发了Regenovo生物3D打印机,该打印机的运动精度为20 μ m [17 ] 所研制的嵌入式3D打印平台的工作空间为230 mm×300 mm,打印精度为100~400 μ m μ m . 浙江大学的王润秋[18 ] 研制了一款工作空间为100 mm×100 mm×50 mm的生物打印平台,并通过打印硅胶材料开展了切片参数优化实验,确定了合适的打印工艺参数. ...
1
2009
... 分析原位皮肤打印系统的工作空间时需考虑以下2种情况:1)直线模组机构固定,仅依靠Stewart并联机器人的平移和旋转进行打印;2)直线模组机构工作,通过直线模组机构和Stewart并联机器人的联合运动进行打印.并联机器人动平台的操作范围即为其工作空间,工作空间是评估并联机器人功能的关键指标之一[19 -20 ] .并联机器人工作空间的主要影响因素包括连杆长度、关节转角及连杆间距等.常用的并联机器人工作空间计算方法包括解析法和数值法.其中:解析法是一种基于数学模型的方法,从并联机器人的几何和运动学关系出发,推导出工作空间边界的函数表达式,但由于所推导的函数表达式过于烦琐,解析法不具有通用性[21 ] ;数值法是指利用计算机算法,先通过迭代计算搜索并联机器人动平台的可达区域,再通过求解运动学方程来计算工作空间的边界[22 -25 ] .数值法运算简单,适用于多种并联机构.基于此,本文采用数值法来求解直线模组机构固定时Stewart并联机器人的工作空间.先利用Python程序遍历并联机器人运动支链与静平台角度的所有组合,随后通过正运动学运算得到所有组合对应的位置正解,剔除不符合要求的位置后,剩余位置对应点的集群即构成了并联机器人的工作空间. ...
1
2009
... 分析原位皮肤打印系统的工作空间时需考虑以下2种情况:1)直线模组机构固定,仅依靠Stewart并联机器人的平移和旋转进行打印;2)直线模组机构工作,通过直线模组机构和Stewart并联机器人的联合运动进行打印.并联机器人动平台的操作范围即为其工作空间,工作空间是评估并联机器人功能的关键指标之一[19 -20 ] .并联机器人工作空间的主要影响因素包括连杆长度、关节转角及连杆间距等.常用的并联机器人工作空间计算方法包括解析法和数值法.其中:解析法是一种基于数学模型的方法,从并联机器人的几何和运动学关系出发,推导出工作空间边界的函数表达式,但由于所推导的函数表达式过于烦琐,解析法不具有通用性[21 ] ;数值法是指利用计算机算法,先通过迭代计算搜索并联机器人动平台的可达区域,再通过求解运动学方程来计算工作空间的边界[22 -25 ] .数值法运算简单,适用于多种并联机构.基于此,本文采用数值法来求解直线模组机构固定时Stewart并联机器人的工作空间.先利用Python程序遍历并联机器人运动支链与静平台角度的所有组合,随后通过正运动学运算得到所有组合对应的位置正解,剔除不符合要求的位置后,剩余位置对应点的集群即构成了并联机器人的工作空间. ...
1
2014
... 分析原位皮肤打印系统的工作空间时需考虑以下2种情况:1)直线模组机构固定,仅依靠Stewart并联机器人的平移和旋转进行打印;2)直线模组机构工作,通过直线模组机构和Stewart并联机器人的联合运动进行打印.并联机器人动平台的操作范围即为其工作空间,工作空间是评估并联机器人功能的关键指标之一[19 -20 ] .并联机器人工作空间的主要影响因素包括连杆长度、关节转角及连杆间距等.常用的并联机器人工作空间计算方法包括解析法和数值法.其中:解析法是一种基于数学模型的方法,从并联机器人的几何和运动学关系出发,推导出工作空间边界的函数表达式,但由于所推导的函数表达式过于烦琐,解析法不具有通用性[21 ] ;数值法是指利用计算机算法,先通过迭代计算搜索并联机器人动平台的可达区域,再通过求解运动学方程来计算工作空间的边界[22 -25 ] .数值法运算简单,适用于多种并联机构.基于此,本文采用数值法来求解直线模组机构固定时Stewart并联机器人的工作空间.先利用Python程序遍历并联机器人运动支链与静平台角度的所有组合,随后通过正运动学运算得到所有组合对应的位置正解,剔除不符合要求的位置后,剩余位置对应点的集群即构成了并联机器人的工作空间. ...
1
2014
... 分析原位皮肤打印系统的工作空间时需考虑以下2种情况:1)直线模组机构固定,仅依靠Stewart并联机器人的平移和旋转进行打印;2)直线模组机构工作,通过直线模组机构和Stewart并联机器人的联合运动进行打印.并联机器人动平台的操作范围即为其工作空间,工作空间是评估并联机器人功能的关键指标之一[19 -20 ] .并联机器人工作空间的主要影响因素包括连杆长度、关节转角及连杆间距等.常用的并联机器人工作空间计算方法包括解析法和数值法.其中:解析法是一种基于数学模型的方法,从并联机器人的几何和运动学关系出发,推导出工作空间边界的函数表达式,但由于所推导的函数表达式过于烦琐,解析法不具有通用性[21 ] ;数值法是指利用计算机算法,先通过迭代计算搜索并联机器人动平台的可达区域,再通过求解运动学方程来计算工作空间的边界[22 -25 ] .数值法运算简单,适用于多种并联机构.基于此,本文采用数值法来求解直线模组机构固定时Stewart并联机器人的工作空间.先利用Python程序遍历并联机器人运动支链与静平台角度的所有组合,随后通过正运动学运算得到所有组合对应的位置正解,剔除不符合要求的位置后,剩余位置对应点的集群即构成了并联机器人的工作空间. ...
Singularity-free workspace of parallel robots
1
2015
... 分析原位皮肤打印系统的工作空间时需考虑以下2种情况:1)直线模组机构固定,仅依靠Stewart并联机器人的平移和旋转进行打印;2)直线模组机构工作,通过直线模组机构和Stewart并联机器人的联合运动进行打印.并联机器人动平台的操作范围即为其工作空间,工作空间是评估并联机器人功能的关键指标之一[19 -20 ] .并联机器人工作空间的主要影响因素包括连杆长度、关节转角及连杆间距等.常用的并联机器人工作空间计算方法包括解析法和数值法.其中:解析法是一种基于数学模型的方法,从并联机器人的几何和运动学关系出发,推导出工作空间边界的函数表达式,但由于所推导的函数表达式过于烦琐,解析法不具有通用性[21 ] ;数值法是指利用计算机算法,先通过迭代计算搜索并联机器人动平台的可达区域,再通过求解运动学方程来计算工作空间的边界[22 -25 ] .数值法运算简单,适用于多种并联机构.基于此,本文采用数值法来求解直线模组机构固定时Stewart并联机器人的工作空间.先利用Python程序遍历并联机器人运动支链与静平台角度的所有组合,随后通过正运动学运算得到所有组合对应的位置正解,剔除不符合要求的位置后,剩余位置对应点的集群即构成了并联机器人的工作空间. ...
并联机器人工作空间的研究
1
1991
... 分析原位皮肤打印系统的工作空间时需考虑以下2种情况:1)直线模组机构固定,仅依靠Stewart并联机器人的平移和旋转进行打印;2)直线模组机构工作,通过直线模组机构和Stewart并联机器人的联合运动进行打印.并联机器人动平台的操作范围即为其工作空间,工作空间是评估并联机器人功能的关键指标之一[19 -20 ] .并联机器人工作空间的主要影响因素包括连杆长度、关节转角及连杆间距等.常用的并联机器人工作空间计算方法包括解析法和数值法.其中:解析法是一种基于数学模型的方法,从并联机器人的几何和运动学关系出发,推导出工作空间边界的函数表达式,但由于所推导的函数表达式过于烦琐,解析法不具有通用性[21 ] ;数值法是指利用计算机算法,先通过迭代计算搜索并联机器人动平台的可达区域,再通过求解运动学方程来计算工作空间的边界[22 -25 ] .数值法运算简单,适用于多种并联机构.基于此,本文采用数值法来求解直线模组机构固定时Stewart并联机器人的工作空间.先利用Python程序遍历并联机器人运动支链与静平台角度的所有组合,随后通过正运动学运算得到所有组合对应的位置正解,剔除不符合要求的位置后,剩余位置对应点的集群即构成了并联机器人的工作空间. ...
并联机器人工作空间的研究
1
1991
... 分析原位皮肤打印系统的工作空间时需考虑以下2种情况:1)直线模组机构固定,仅依靠Stewart并联机器人的平移和旋转进行打印;2)直线模组机构工作,通过直线模组机构和Stewart并联机器人的联合运动进行打印.并联机器人动平台的操作范围即为其工作空间,工作空间是评估并联机器人功能的关键指标之一[19 -20 ] .并联机器人工作空间的主要影响因素包括连杆长度、关节转角及连杆间距等.常用的并联机器人工作空间计算方法包括解析法和数值法.其中:解析法是一种基于数学模型的方法,从并联机器人的几何和运动学关系出发,推导出工作空间边界的函数表达式,但由于所推导的函数表达式过于烦琐,解析法不具有通用性[21 ] ;数值法是指利用计算机算法,先通过迭代计算搜索并联机器人动平台的可达区域,再通过求解运动学方程来计算工作空间的边界[22 -25 ] .数值法运算简单,适用于多种并联机构.基于此,本文采用数值法来求解直线模组机构固定时Stewart并联机器人的工作空间.先利用Python程序遍历并联机器人运动支链与静平台角度的所有组合,随后通过正运动学运算得到所有组合对应的位置正解,剔除不符合要求的位置后,剩余位置对应点的集群即构成了并联机器人的工作空间. ...
Characterization of workspaces of parallel manipulators
0
1992
6-PTRT型齿顶倒角机器人运动学及工作空间分析
0
2013
6-PTRT型齿顶倒角机器人运动学及工作空间分析
0
2013
新型 6-HTRT 并联机器人工作空间和参数研究
1
2002
... 分析原位皮肤打印系统的工作空间时需考虑以下2种情况:1)直线模组机构固定,仅依靠Stewart并联机器人的平移和旋转进行打印;2)直线模组机构工作,通过直线模组机构和Stewart并联机器人的联合运动进行打印.并联机器人动平台的操作范围即为其工作空间,工作空间是评估并联机器人功能的关键指标之一[19 -20 ] .并联机器人工作空间的主要影响因素包括连杆长度、关节转角及连杆间距等.常用的并联机器人工作空间计算方法包括解析法和数值法.其中:解析法是一种基于数学模型的方法,从并联机器人的几何和运动学关系出发,推导出工作空间边界的函数表达式,但由于所推导的函数表达式过于烦琐,解析法不具有通用性[21 ] ;数值法是指利用计算机算法,先通过迭代计算搜索并联机器人动平台的可达区域,再通过求解运动学方程来计算工作空间的边界[22 -25 ] .数值法运算简单,适用于多种并联机构.基于此,本文采用数值法来求解直线模组机构固定时Stewart并联机器人的工作空间.先利用Python程序遍历并联机器人运动支链与静平台角度的所有组合,随后通过正运动学运算得到所有组合对应的位置正解,剔除不符合要求的位置后,剩余位置对应点的集群即构成了并联机器人的工作空间. ...
新型 6-HTRT 并联机器人工作空间和参数研究
1
2002
... 分析原位皮肤打印系统的工作空间时需考虑以下2种情况:1)直线模组机构固定,仅依靠Stewart并联机器人的平移和旋转进行打印;2)直线模组机构工作,通过直线模组机构和Stewart并联机器人的联合运动进行打印.并联机器人动平台的操作范围即为其工作空间,工作空间是评估并联机器人功能的关键指标之一[19 -20 ] .并联机器人工作空间的主要影响因素包括连杆长度、关节转角及连杆间距等.常用的并联机器人工作空间计算方法包括解析法和数值法.其中:解析法是一种基于数学模型的方法,从并联机器人的几何和运动学关系出发,推导出工作空间边界的函数表达式,但由于所推导的函数表达式过于烦琐,解析法不具有通用性[21 ] ;数值法是指利用计算机算法,先通过迭代计算搜索并联机器人动平台的可达区域,再通过求解运动学方程来计算工作空间的边界[22 -25 ] .数值法运算简单,适用于多种并联机构.基于此,本文采用数值法来求解直线模组机构固定时Stewart并联机器人的工作空间.先利用Python程序遍历并联机器人运动支链与静平台角度的所有组合,随后通过正运动学运算得到所有组合对应的位置正解,剔除不符合要求的位置后,剩余位置对应点的集群即构成了并联机器人的工作空间. ...