2. 浙江省海洋渔业资源可持续利用技术研究重点实验室, 浙江 舟山 316021;
3. 中国水产科学研究院, 北京 100141
2. Key Lab of Sustainable Utilization of Technology Research for Fishery Resource of Zhejiang, Zhoushan 316021, Zhejiang Province, China;
3. Chinese Academy of Fishery Sciences, Beijing 100141, China
红霉素(Erythromycin)是由红霉素链霉菌产生的一种广谱大环内酯类抗生素,对革兰阳性杆菌、葡萄球菌和链球菌属都具有良好的抑制作用,广泛应用于临床和养殖领域[1].红霉素能与敏感细菌的50S核蛋白体亚基可逆性结合,通过抑制新合成的肽基tRNA分子从核蛋白体受体部位移至肽酰基结合部位,从而抑制细菌蛋白质的合成[2].然而,红霉素在生物体内代谢时间长,且过量使用会引起人体过敏,造成胃肠道、肝脏损伤等危害.鉴于红霉素的严重危害性,为更好地保障食品安全,欧美EC 1181/2002[3]和我国农业部235号公告规定,动物源性组织中红霉素的最大残留量为200 μg·kg-1.
目前测定动物源性组织中红霉素残留的方法主要有薄层色谱法(TLC)[4]、液相色谱-二极管阵列检测法(LC-DAD)[5]、液相色谱-电喷雾法(LC-CAD)[6]和液相色谱-质谱法(LC-MS/MS)[7].液相色谱-串联质谱法灵敏度高、精确度好,是目前检测红霉素残留的主要方法.由于水产品的成分和基质较复杂,目标分析物易被基质干扰遮蔽,故开发一种能有效提取净化的前处理方法是水产品药物残留分析测定的关键.目前,红霉素残留检测的前处理方法主要有传统液液萃取、在线固相萃取和分子印迹固相萃取等,但这些方法存在试剂量消耗大、操作步骤烦琐、需使用特殊设备或需要特定的实验环境等问题.QuEChERS(Quick、Easy、Cheap、Effective、Rugged、Safe)是一种快速、简单、便宜、高效、耐用和安全的新兴提取净化技术,所需实验设备简单、试剂消耗量少、操作步骤简单、处理时间短、提取净化效率高、可控性强,为解决上述问题提供了新途径[8-10].本研究改进了QuEChERS提取净化方法,并结合超高效液相色谱串联质谱定量分析高灵敏度的优势,建立QuEChERS-超高效液相色谱串联质谱法以测定水产品中的红霉素残留.
1 实验部分 1.1 仪器和试剂ACQUITYTM UPLC-Quattro Premier XE质谱仪(美国Waters公司);Centrifuge5810高速离心机(德国Eppendorf公司);N-EVAP-112氮吹仪(美国Organomation公司);MS2漩涡混合器(德国IKA公司).甲醇、乙腈(均为色谱纯,德国Merck公司);氯化钠、甲酸、无水硫酸镁均来自美国Sigma公司;石墨化炭黑(GCB,37~125 μm)、N-丙基乙二胺(PSA,40~63 μm)、十八烷基硅烷键合硅胶(C18,40~63 μm);实验用水为Millipore-Q系统制备的超纯水.
红霉素标准品(纯度≥97.0%,德国Dr. Ehrenstorfer公司);红霉素同位素标记物标准品(纯度≥99.0%,美国Sigma公司).准确称取5 mg红霉素和红霉素同位素标记物,用甲醇溶解并分别定容至50 mL,-20 ℃保存,保存期3个月;使用时分别用甲醇逐级稀释成100 ng·mL-1的红霉素标准工作液和红霉素内标工作液.
1.2 前处理方法称取已均质样品(5.00±0.02) g于50 mL离心管中,添加100 μL浓度为100 ng·mL-1的红霉素内标工作液和10 mL乙腈,涡旋提取2 min,加入4.00 g无水硫酸镁和1.00 g氯化钠,涡旋振荡2 min,6 000 r·min-1离心5 min;取5 mL上清液至15 mL离心管,50 ℃氮吹至干,用1 mL 30%甲醇水溶液溶解残留物,称取100 mg PSA添加到离心管,振荡涡旋1 min,8 000 r·min-1离心5 min,再用0.22 μm滤膜过滤,供仪器测定分析.
1.3 仪器条件液相色谱柱:ACQUITYTM UPLC BEH C18柱(50 mm×2.1 mm,1.7 μm);样品室温度10 ℃;柱温40 ℃;流速0.3 mL·min-1;进样量10 μL;流动相A为甲醇,B为0.1%甲酸溶液,梯度洗脱:0~1.0 min,70% B;1.0~1.2 min,70%~10% B;1.2~3.0 min,10% B;3.0~3.5 min,10%~70% B;3.5~5.0 min,70% B.
质谱条件:电喷雾正离子源(ESI+);检测模式:多反应监测模式(MRM);毛细管电压:3.5 kV;离子源温度:110 ℃;脱溶剂温度:360 ℃;脱溶剂气流量:800 L·h-1;锥孔气流量:50 L·h -1.红霉素及红霉素内标物的质谱多反应监测采集参数如表 1所示.
| 表 1 红霉素和红霉素内标物的质谱采集参数 Table 1 Mass parameters for erythromycin and its internal standard |
实验以0.1%甲酸-甲醇为红霉素和红霉素内标物的色谱分离流动相,一方面分析物在甲醇中的离子化效率和分析灵敏度较乙腈高;另一方面0.1%体积分数的甲酸溶液能改善分析物的色谱峰形,提高分析物的响应值.在保证高灵敏度的同时,实验开发的洗脱条件能在2 min内完全洗脱分析物,大大缩短了分析时间,提高了色谱分离的效率,且峰形尖锐对称,无出现拖尾和双头峰等现象.
为获得分析物的质谱采集参数和质谱的仪器分析条件,比较了ESI+和ESI-扫描模式下红霉素及其内标物的响应,并对锥孔电压、碰撞能量等参数进行优化.结果表明,ESI+扫描模式下分析物的响应值较ESI-扫描模式高.在正离子一级全扫描下,发现特征离子峰[C37H67NO13+H]+(m/z=734.5) 丰度最高,将其选择为红霉素的母离子,并进行二级质谱裂解分析.从裂解得到的离子碎片信息中发现,红霉素特征离子峰m/z=734.5在二级碰撞能量不断增大时,离子碎片逐渐增多,其中离子碎片峰m/z为158.1和576.4时,丰度较高,依次将其选为定量离子和定性离子.红霉素的离子碎片信息及二级裂解质谱图如图 1所示.
|
图 1 红霉素质谱图 Fig. 1 Mass spectra of erythromycin |
液相色谱串联质谱法通常依据色谱峰面积进行定量,为确保仪器的稳定性和重现性,根据单个离子色谱峰需有12~20个扫描点数的原则,采用质谱多反应监测模式(MRM),并将单个通道内的3种监测离子对滞留时间(Dwell time)都设为0.18 s.在有效保证色谱峰宽为0.15 min的同时,使每个离子色谱峰扫描点数达到15个,提高了液相色谱串联质谱分析的重现性.
2.2 前处理方法改进QuEChERS技术分为提取、盐析和净化3个步骤,通常将纯乙腈或酸化乙腈作为萃取剂.由于红霉素对酸较敏感,在酸性条件下不稳定,故选择10 mL纯乙腈作为萃取剂,既能有效提取样品中残留的红霉素,也能保持目标物的稳定性;而氮吹后的残留物不采用初始流动相溶解,因此,便于样品液保存.水产品本身含有大量水分,需在萃取过程中加入无水MgSO4、NaCl以去除水分.NaCl的饱和水溶液对混合液起分层作用;无水MgSO4能吸水发热,且能促使分析物从水相转移至有机相,提高萃取效率.为缩短前处理时间,减少吸附剂的消耗量,同时保证有足够的样品提取液,本实验将样品提取液稀释1倍,并氮吹浓缩至干,用30%体积分数甲醇水溶液复溶残留物.结果表明,改进后方法的检出限、回收率和重复性并无显著变化,但缩短了前处理时间,符合实际检测需求.
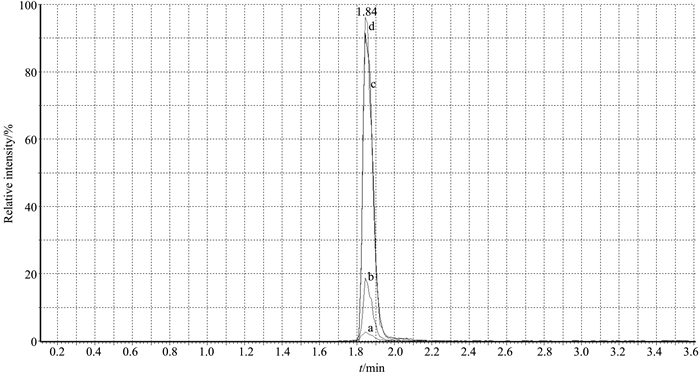
2.3 吸附剂的选择QuEChERS方法是利用萃取液中的吸附剂与样品基质中的杂质相互作用,实现分析物的提取和净化.选择适合的吸附剂是开发QuEChERS方法的核心,只有适合的吸附剂才能在高效吸附杂质的同时,不干扰分析物的测定.吸附剂的选择主要依据样品基质中蛋白、脂肪酸及色素等杂质的分布,其中C18能通过非极性相互作用去除样品中的脂肪和糖类物质;GCB是具有阴离子交换作用的吸附剂,能有效吸附平面分子结构的杂质;PSA带有2个氨基,通过氢键相互作用吸附极性色素、极性有机酸等杂质.为考察3种吸附剂对分析物的影响,分别将100 mg的3种吸附剂加入到1 mL浓度为20 μg·L-1的红霉素标准溶液中,比较相对应的红霉素色谱峰面积,结果如图 2所示.GCB和C18对红霉素具有很强的吸附能力,而PSA对红霉素无明显吸附作用,因此选择PSA作为净化吸附剂.

|
图 2 不同吸附剂对红霉素面积的影响 Fig. 2 Effect of different sorbents on erythromycin a—GCB; b—C18; c—PSA; d—空白标准溶液(Standard). |
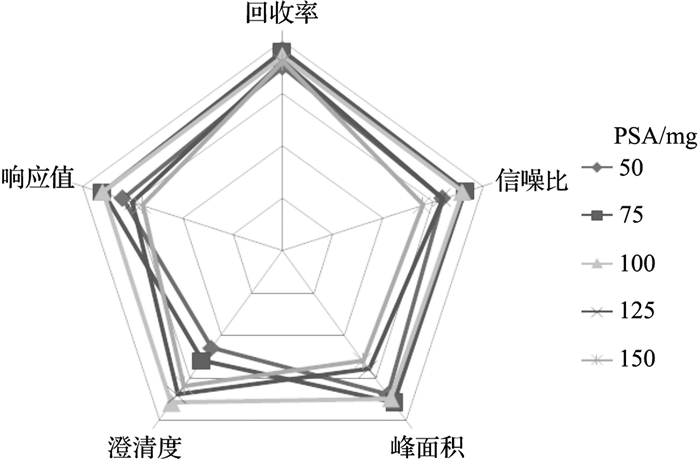
为确定吸附剂PSA的合适用量,实验分别称取50,75,100,125,150 mg PSA净化添加浓度为10 μg·kg-1的草鱼样品.通过比较分析物的响应值、峰面积,计算分析物的信噪比,从样品回收率、样品净化液的实际澄清度及吸附剂消耗量等角度评价PSA的合适用量.综合评价结果如图 3所示,75,100 mg PSA都有较高的响应值和回收率,但75 mg PSA在实际使用过程中复溶液透明度不高,仍有部分杂质存在,影响过膜及仪器分析.因此,最终选定100 mg PSA为本实验的合适用量,其对应白虾样品的MRM图如图 4所示.
|
图 3 不同用量PSA对实验结果的影响 Fig. 3 Effects of different amounts of PSAon the experimental results |
|
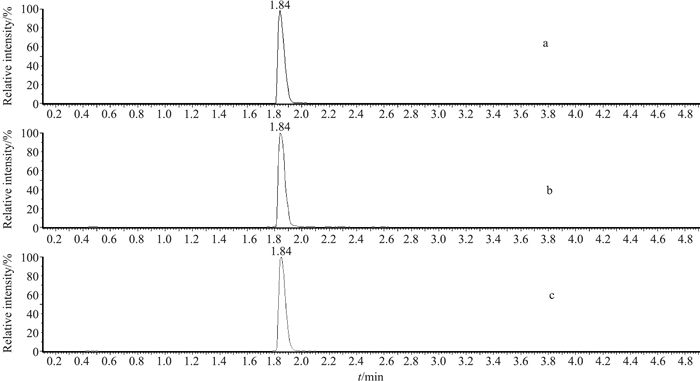
图 4 100 mg PSA净化后的白虾样品(红霉素加标浓度为2 μg·kg-1)MRM图 Fig. 4 MRM ion chromatograms of white prawn containing 2 μg·kg-1 erythromycin purified with 100 mg PSA a—定量离子对(quantitative ion pair); b—定性离子对(qualitative ion pair); c—内标离子对(internal standard ion pair). |
内标的使用能部分抵消基质效应及前处理过程中产生的实验误差.为进一步检测基质效应,将提取液作为基质溶液,分别用基质溶液与30%甲醇水溶液各配制2和5 μg·L-1红霉素溶液,比较对应的平均峰面积.计算可得基质效应(ME)为3.6%,表明基质效应对定量分析影响较小.
在优化的实验条件下,用30%甲醇水溶液配制0.5~50 μg·L-1系列标准工作液,内标浓度均为10 μg·L-1,以峰面积对应的浓度绘制标准曲线.结果表明,红霉素浓度在0.5~50 μg·L-1时具有良好的线性关系(R2=0.997 6), 能够满足定量分析的需求;分别以3倍信噪比计算红霉素的检出限(LOD)、10倍信噪比计算定量限(LOQ),得到检出限和定量限分别为0.1和0.3 μg·kg-1.
2.5 方法的精密度与准确度称取5.00 g阴性白虾和草鱼样品,添加0.50,2.00和10.0 μg·kg-1 3种红霉素加标浓度,每个加标浓度重复测定6次,计算对应的精密度和准确率, 结果如表 2所示.红霉素的平均回收率为87.6%~96.1%;相对标准偏差为2.2%~5.3%;符合红霉素残留检测的要求.
| 表 2 红霉素在阴性样品中的加标回收率和相对标准偏差(n=6) Table 2 Recoveries and RSD of samples for erythromycin(n=6) |
为了验证方法的实用性和适用性,对市售20份水产品进行检测分析,被测样品中红霉素的浓度均低于0.1 μg·kg-1.表明此批次抽检样品均未有红霉素检出,红霉素滥用、乱用的情况在水产品行业中得到了有效的控制.
3 结论实验建立了QuEChERS净化-超高效液相色谱串联质谱测定水产品中红霉素残留的分析方法.以乙腈为提取剂,QuEChERS法净化,结合超高效液相色谱串联质谱定量分析水产品中的红霉素残留,重复性好,回收率高,简便高效,能够满足红霉素检测分析的要求,具有实际应用价值,为保障水产品的质量安全提供了技术支撑.
| [1] |
于慧娟, 蔡友琼, 惠芸华, 等. 高效液相色谱-电喷雾串联质谱法测定水产品中红霉素的残留[J].
分析化学, 2009, 37(1): 91–94.
YU H J, CAI Y Q, HUI Y H, et al. Determination of erythromycin residue in fishery products by high performance liquid chromatography-electrospray ionization tandem mass spectrometry[J]. Chinese Journal of Analytical Chemistry, 2009, 37(1): 91–94. |
| [2] |
周玲, 吴黎明, 周金慧. 高效液相色谱-串联质谱检测巢脾中红霉素残留[J].
中国食品学报, 2013, 13(6): 198–202.
ZHOU L, WU L M, ZHOU J H. Determination of erythromycin residue in honeycomb by high performance liquid chromatography-tandem mass spectrometry[J]. Journal of Chinese Institute of Food Science and Technology, 2013, 13(6): 198–202. |
| [3] | Official Journal of the European Communities Commission Regulation(EC) NO.1181/2002[EB/OL][2002-06-01].http://ec.europa.eu/health/sites/health/files/files/mrl/regpdf/2002_07_01_1181_en.pdf. |
| [4] |
韩南银, 周婷. 蜂蜜中红霉素残留量的检测[J].
食品科学, 2003, 24(2): 118–119.
HAN N Y, ZHOU T. Determination of erythromycin residue in honey[J]. Food Science, 2003, 24(2): 118–119. |
| [5] | KAMAREI F, ATTAR H, NIKJAH S, et al. Determination of erythromycins in fermentation broth using liquid phase extraction with back extraction combined with high performance liquid chromatography[J]. Arabian Journal of Chemistry, 2014, 7(3): 292–296. DOI:10.1016/j.arabjc.2010.10.033 |
| [6] |
周茜, 陈满堂, 朱丽华, 等. 在线固相萃取结合高效液相色谱-电喷雾式检测器测定鸡粪中红霉素残留[J].
分析化学, 2014, 42(12): 1838–1841.
ZHOU Q, CHEN M T, ZHU L H, et al. Determination of erythromycin in chicken manure by high performance liquid chromatography-corona-charged aerosol detection coupled with on-line solid phase extraction[J]. Chinese Journal of Analytical Chemistry, 2014, 42(12): 1838–1841. |
| [7] | PENDELA M, VAN DEN BOSSCHE L, HOOGMARTENS J, et al. Combination of a liquid chromatography-ultraviolet method with a non-volatile eluent, peak trapping and a liquid chromatography-mass spectrometry method with a volatile eluent to characterise erythromycin related substances[J]. Journal of Chromatography A, 2008, 1180(1/2): 108–121. |
| [8] | FERNANDES P J, BARROS N, CAMARA J S. A survey of the occurrence of ochratoxin A in Madeira wines based on a modified QuEChERS extraction procedure combined with liquid chromatography-triple quadrupole tandem mass spectrometry[J]. Food Research International, 2013, 54(1): 293–301. DOI:10.1016/j.foodres.2013.07.020 |
| [9] | FASANO E, CIRILLO T, ESPOSITO F, et al. Migration of monomers and plasticizers from packed foods and heated microwave foods using QuEChERS sample preparation and gas chromatography/mass spectrometry[J]. LWT-Food Science and Technology, 2015, 64(2): 1015–1021. DOI:10.1016/j.lwt.2015.06.066 |
| [10] |
刘玉, 张同来, 杨利, 等. QuEChERS-超高效液相色谱串联质谱法测定土壤中三硝基酚类物质[J].
分析化学, 2014, 42(8): 1183–1188.
LIU Y, ZHANG T L, YANG L, et al. QuEChERS-ultra performance liquid chromatography-tandem mass spectrometry for determination of 2, 4, 6-trinitrophenol, 2, 4, 6-trinitroresorcinate and 2, 4, 6-trinitrophloroglucinol in soil[J]. Chinese Journal of Analytical Chemistry, 2014, 42(8): 1183–1188. DOI:10.11895/j.issn.0253-3820.131174 |



