生物质作为自然界来源极为广泛的一种可再生能源,具有燃烧清洁、低污染和价格低廉的特点,是一种可替代化石等不可再生能源的理想能源.生物质主要分为纤维素、半纤维素和木质素,其中木质素中存在芳香结构和大量的醚结构,可通过催化加氢脱氧(hydrodeoxygenation,HDO)方法转化为烃类作为燃料或燃料助剂[1-3].香兰素是木质素热解产物中最具代表性的典型含氧化合物, 研究香兰素的催化转化对于生物质资源的转化和高效利用具有重要意义.香兰素分子结构中含有酚羟基,且其对位上由芳醛基取代,令其具有还原性,易氧化,热稳定性较差.通过高压及中等温度下的催化加氢反应,可将反应物中的氧以H2O的形式脱除,以消除或部分消除不稳定的活性功能团.但是,由于反应产物中有水生成,要求加氢脱氧催化剂具有较高的水热稳定性.目前,研究较多的用于加氢脱氧的催化剂主要是负载型的硫化催化剂[4-6]和贵金属催化剂[7-10]等.贵金属催化剂具有比硫化Co-Mo、Ni-Mo基催化剂更好的催化加氢性能,可在较温和的条件下实现底物的加氢脱氧,其中Pt/Al2O3虽表现出较好的脱氧活性,但其载体的耐水性较差.
加氢脱氧反应通常在较高的氢压下完成,不仅氢气的消耗量大,而且氢气易燃、易泄露,对反应设备的安全性要求非常严格[11].相较于氢气,采用低碳脂肪醇作为氢供体的设备更安全、反应条件更温和、操作更方便、成本更低廉.本文基于前期研究工作[12],在不外加氢气的条件下,直接利用含氢的有机小分子氢供体作为氢源,分别考察甲醇、乙醇、正丙醇、异丙醇和正丁醇等短链脂肪醇作为氢供体在生物质模化物香兰素加氢脱氧催化反应中的作用,探讨其催化反应的路径及催化剂的加氢脱氧活性.
1 实验 1.1 催化剂的制备采用共沉淀法制备Ce0.5Zr0.5O2载体[13].根据摩尔比Ce:Zr=1:1,准确称取适量Zr(NO3)4·5H2O和Ce(NO3)3·6H2O于烧杯中,加入蒸馏水,充分搅拌使其溶解,再滴加过量的氨水使其充分沉淀,经过滤、洗涤、干燥、研磨、煅烧得到粉末状的Ce0.5Zr0.5O2复合氧化物.
采用溶胶凝胶法制备Ce0.5Ti0.5O2载体[14].准确称取一定量的Ti(OC4H9)4置于烧杯中,加入一定比例的乙酸和乙醇溶液,再用浓硝酸调整pH值.然后准确称取等摩尔量的Ce(NO3)3·6H2O于另一烧杯中,加入一定量的水和乙醇,充分搅拌至溶解.将Ce(NO3)3混合溶液缓慢滴加到Ti(OC4H9)4混合溶液中,稳定后得到溶胶,经老化、干燥得到凝胶,最后经研磨和煅烧后得到Ce0.5Ti0.5O2载体.
采用等体积浸渍法制备Ce0.5Zr0.5O2和Ce0.5Ti0.5O2复合氧化物负载2%Pt的催化剂.持续搅拌,将1 g载体缓慢加入0.2 mL的0.1 g·mL-1氯铂酸溶液中,继续搅拌4 h,水浴超声1 h,室温静置5 h后快速炒干,在110 ℃下烘干12 h后500 ℃煅烧3 h得到新鲜催化剂.将其转移到石英加热管中,在550 ℃下用高纯氢气还原3 h,在氢气气氛下冷却至室温,备用.
1.2 催化剂的表征载体以及催化剂的物相结构用X射线衍射法测定,所用仪器为D8 ADVANCE型X射线衍射仪(Bruker公司,德国).测试条件:辐射源为Cu Kα(λ=0.154 2 nm),管电压40 kV,管电流40 mA,衍射扫描范围2θ=10°~80°,扫描步长0.02°,采样时间0.2 s.
用电镜表征催化剂表面金属的粒径大小和形貌.透射电镜(TEM)与能谱分析(energy dispersive spectrometer,EDX),所用仪器为FEIN Tecnai F30透射电子显微镜(Philips公司,荷兰),加速电压为300 kV.制样过程:将少量粉末样品经充分研磨后超声分散于无水乙醇中,静置后用毛细点样管吸取适量分散液,滴在微栅上,最后在红外灯下烘干.
利用氮气吸脱附测定样品的比表面积和孔结构,所用仪器为Tristar Ⅱ 3020型吸附仪(Micromeritics Instrument Corporation,美国),首先在150 ℃高真空条件下预处理样品12 h,然后在液氮温度(-196 ℃)下测定.比表面积按照Brunauer-Emmett-Teller(BET)公式计算得到,按照Barrett-Joyner-Halenda(BJH)方法以脱附曲线为依据计算样品的孔体积和孔径分布.
利用氨气程序升温脱附法在TPD装置上分析样品的酸性强弱与酸性位点.采用热导池TCD对脱附的NH3进行定量与定性分析.取一定量的样品,在氮气气氛中以10 ℃·min-1的速率升温至500 ℃并保持0.5 h,然后降温至100 ℃,吸附氨气30 min.用氮气吹扫样品30 min,以除去样品表面物理吸附的NH3, 至基线平稳.最后以10 ℃·min-1的速率升温至800 ℃.
1.3 香兰素催化加氢脱氧反应本实验在100 mL的机械搅拌不锈钢高压釜中进行,原料香兰素0.5 g,催化剂0.2 g,低碳脂肪醇50 mL为溶剂和氢供体.向反应釜中充入0.5 MPa的高纯氮气5次以排出釜中空气,然后充入1.0 MPa的氮气.在快速搅拌下,将反应釜加热至220 ℃,然后恒温3 h.反应结束后,将反应釜自然冷却至室温.液相产物经离心过滤后转移至100 mL容量瓶中定容.用气相色谱质谱联用仪(GCMS-QP 2010 SE)检测并确定液相产物的分子结构.同时,以苯甲醚作为内标,利用气相色谱仪(Agilent 6820)进行定量分析.气相色谱分析条件:Agilent HP-5色谱柱(30 m×0.32 mm×0.5 μm), 柱温120 ℃,进样口温度250 ℃,FID检测器温度220 ℃.
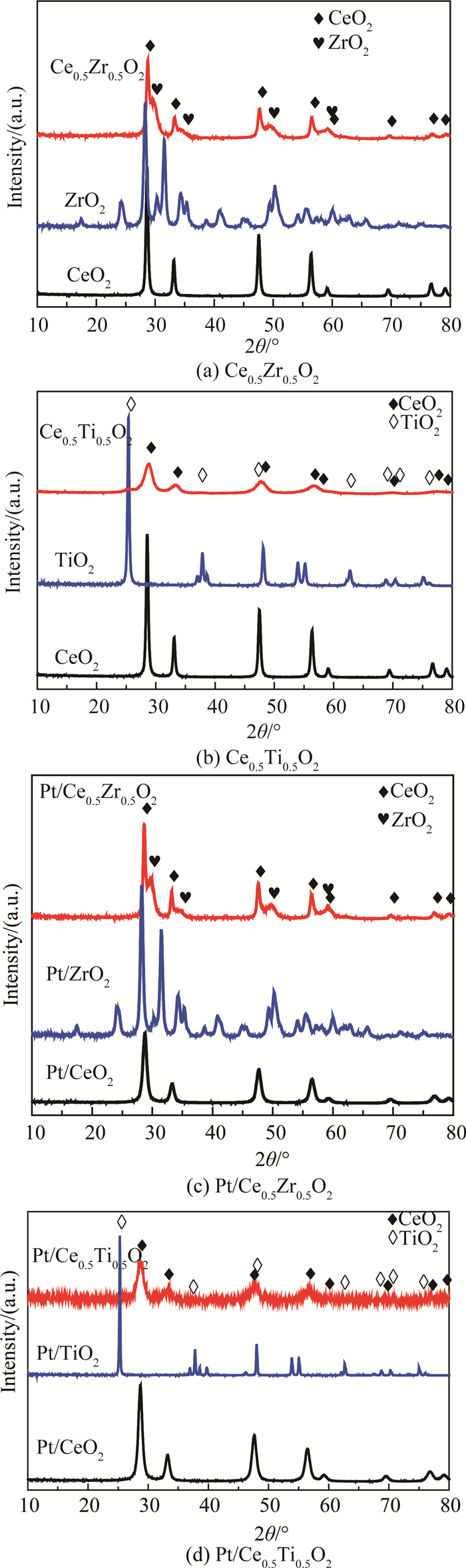
2 结果与讨论 2.1 载体及催化剂的表征X射线衍射表征的结果如图 1所示.由图 1(a)可知,Ce0.5Zr0.5O2样品中28.55°, 33.08°, 47.48°, 56.33°, 59.09°和69.40°位置出现的明显的衍射峰归属于CeO2立方晶相的(111),(200),(220),(311),(222),(400)晶面[15],在30.2°, 44.7°和50.4°处出现的较弱的衍射峰归属于ZrO2四方晶相. Ce0.5Zr0.5O2样品中CeO2(111)面的衍射峰向右偏移,峰形变宽,表明部分Zr4+离子已经进入CeO2晶胞,由于Zr4+的离子半径(0.084 nm)小于Ce4+(0.097 nm),当Zr4+取代部分Ce4+晶格后,造成晶胞的扭曲和收缩,形成了铈锆固溶体.
|
图 1 载体及催化剂的XRD谱图 Fig. 1 XRD patterns of supports and catalysts |
由图 1(b)可知,Ce0.5Ti0.5O2样品中出现了CeO2的立方晶相的特征峰. Ti4+取代Ce4+进入立方晶相的结构后,峰强度变小、峰形变宽,表明其晶粒度减小.这令25.6°处归属于TiO2锐钛矿晶型的强度最大的(101)面的特征峰[16]变得很弱,表明Ti4+几乎完全进入CeO2晶格中形成了铈钛固溶体,部分未能进入晶格的Ti以无定形状态存在[17].
由图 1(c)和(d)中可知,负载Pt后的催化剂与载体相比,其特征峰的峰形并未发生变化,也没有出现归属于贵金属Pt的特征衍射峰.说明贵金属Pt粒子高度分散于载体表面,对载体的物相结构基本无影响.
负载金属铂后催化剂的透射电镜(TEM)和能谱图如图 2所示.除了在电镜图(a)中有极少量纳米尺寸铂颗粒外,图(b)中几乎无铂相关的颗粒,但能谱图表明有铂存在,说明催化剂中铂金属颗粒太小,呈高度分散状态.

|
图 2 催化剂的透射电镜图及能谱图 Fig. 2 TEM images and EDAX patterns for the corresponding catalysts |
BET计算得到的载体和相应催化剂的物理结构数据如表 1所示,Ce0.5Zr0.5O2和Ce0.5Ti0.5O2样品的比表面积均较组分单一的氧化物CeO2、ZrO2、TiO2大.结合XRD的分析结果,Ce0.5Zr0.5O2和Ce0.5Ti0.5O2样品中氧化物的特征峰较单独组分中同一特征峰强度弱且峰形宽,表明其晶粒尺寸减小了,继而比表面积增大.催化剂的比表面积相较于载体发生了改变,可能是在制备负载2%Pt催化剂时,浸渍和煅烧过程对催化剂比表面积有一定的影响[18].
| 表 1 载体及催化剂的物理结构参数 Table 1 Specific surface areas, pore diameter and pore volume for supports and corresponding catalysts |
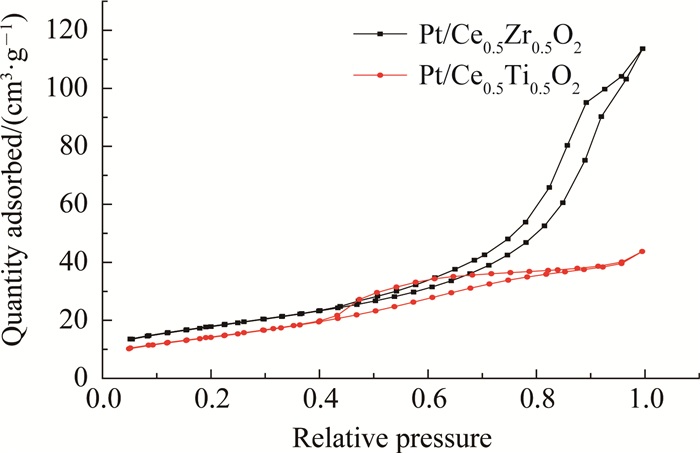
催化剂的氮气吸脱附结果如图 3所示,吸附-脱附曲线均为Ⅰ型和Ⅳ型的结合,存在H2型的滞留回环[19]. 表 1中样品的孔径大小表明,催化剂主要是介孔材料,催化剂中介孔的存在可减小加氢脱氧催化反应中底物分子的扩散阻力,有利于改善催化剂的催化活性.
|
图 3 催化剂的低温氮气吸附-脱附曲线 Fig. 3 N2 adsorbtion-desorption isotherms of catalysts |
加氢脱氧催化剂对载体的水热稳定性要求比较高,实验采取较为苛刻的水热条件考察载体Ce0.5Zr0.5O2和Ce0.5Ti0.5O2的水热稳定性,即在反应釜中充入1.0 MPa氮气,加入32 mL蒸馏水及8 mL的冰醋酸,温度为260 ℃,处理时间为4~8 h.
表 2和图 4分别为水热处理前后载体比表面积和物相随水热时间的变化情况,可以看出,载体Ce0.5M0.5O2(M=Zr, Ti)的比表面积无明显变化,其晶相结构在水热处理过程中均未发生显著变化,表明复合氧化物载体Ce0.5M0.5O2(M=Zr, Ti)具有较高的水热稳定性.
| 表 2 水热处理前后载体的比表面积 Table 2 BET specific surface area for supports before and after hydrothermal treatment |

|
图 4 水热处理前后载体的XRD谱图 Fig. 4 XRD patterns for supports before and after hydrothermal treatment |
在所有实验条件相同的情况下,以乙醇为氢供体时,2种不同载体的复合氧化物催化剂Pt/Ce0.5M0.5O2(M=Zr, Ti)的香兰素加氢脱氧反应数据如表 3中所示,反应产物主要有香兰醇(vanillyl alcohol)、4-甲基愈创木酚(p-cresol)、愈创木酚(guaiacol)等加氢产物,还有少量香兰醇乙醚(vanillyl ethyl ether)副产物.复合氧化物催化剂Pt/Ce0.5M0.5O2(M=Zr, Ti)均具有优良的加氢脱氧活性,催化性能与载体表面上高度分散的贵金属Pt粒子密切相关.其中,催化剂Pt/Ce0.5Zr0.5O2的活性较Pt/Ce0.5Ti0.5O2更胜一筹,香兰素的转化率可达89.8%,主要转化为脱羰反应产物愈创木酚,部分转化为加氢脱氧产物4-甲基愈创木酚.从图 5的NH3-TPD脱附温度和脱附峰面积可知,酸强度和酸量较高的催化剂会发生缩醛醚化副反应.在相同的反应条件下,酸量较低的Pt/Ce0.5Zr0.5O2更利于香兰素的转化和加氢脱氧反应,说明催化剂的加氢脱氧性能还与其表面的酸性质以及贵金属与载体之间的相互作用有关.
| 表 3 催化剂载体对香兰素加氢脱氧反应的影响 Table 3 The influence of different catalysts for HDO of vanillin |

|
图 5 催化剂的NH3-TPD表征图 Fig. 5 NH3-TPD profiles for catalysts |
从催化反应路径的角度分析,4-甲基愈创木酚由香兰素加氢后的产物香兰醇经氢解断裂C—O键得到,如图 6(a)所示.愈创木酚由香兰素分子对位上的芳醛基直接发生脱羰反应得到,见图 6(b).此外,香兰素加氢生成香兰醇的同时,还可与作为氢供体的低碳脂肪醇直接醚化生成少量的香兰醇单乙醚半缩醛副产物(见图 6(c)).因此,结合图 5和表 3,在香兰素加氢脱氧催化反应中,催化剂载体的酸性强度和酸量对催化剂的活性和产物分布有重要影响.

|
图 6 香兰素催化反应路径图 Fig. 6 Reaction pathways of the vanillin |
以Pt/Ce0.5Zr0.5O2为催化剂,分别以甲醇、乙醇、正丙醇、异丙醇、正丁醇为氢供体,香兰素加氢脱氧反应的结果见表 4.催化反应以Pt/Ce0.5Zr0.5O2为催化剂,甲醇为氢供体时,以加氢脱氧反应路径为主(见图 6(a)),香兰素加氢脱氧催化反应的转化率高达99.3%,产物4-甲基愈创木酚的选择性达80.2%.乙醇、丙醇和正丁醇作为氢供体时,反应路径以脱羰反应为主(见图 6(b)),其中异丙醇作为氢供体时,香兰素的转化率高达97.6%,脱羰反应的产物愈创木酚的选择性达80.9%.实验结果表明,催化剂的催化活性不仅与催化剂中贵金属Pt纳米粒子的高分散性有关,而且跟Pt与Ce0.5Zr0.5O2、Ce0.5Ti0.5O2固溶体载体的相互作用以及载体表面的酸性有关.
| 表 4 低碳脂肪醇氢供体对香兰素加氢脱氧反应的影响 Table 4 The effect of different hydrogen donors on HDO of vanillin |
从表 3和表 4的催化活性评价结果可知,低碳脂肪醇作为氢源并兼作溶剂,是香兰素加氢脱氧催化反应较理想的氢供体,与采用氢气的加氢脱氧过程相比,低碳脂肪醇作为有机小分子氢供体溶剂,其溶剂的极性[20-21]和酸性[21]对加氢脱氧反应存在对应关系.从表 4可以看出,溶剂极性对不饱和醛加氢有着重要影响,因为催化剂能吸附溶剂改变其表面性质.溶剂的极性越大,越有利于C=O的加氢.甲醇较其他低碳脂肪醇的极性均高,有利于生成加氢脱氧反应产物4-甲基愈创木酚.正丙醇、异丙醇及正丁醇作为氢供体时,4-甲基愈创木酚的选择性大小为:正丙醇>正丁醇>异丙醇,与其极性规律相符.低碳脂肪醇同时也是质子化溶剂,酸性越强,给出[H]的能力越强,活泼氢越多对加氢反应越有利.甲醇的酸性在上述5种低碳脂肪醇中最高,给出质子的能力最强,更有利于香兰素的加氢脱氧反应.
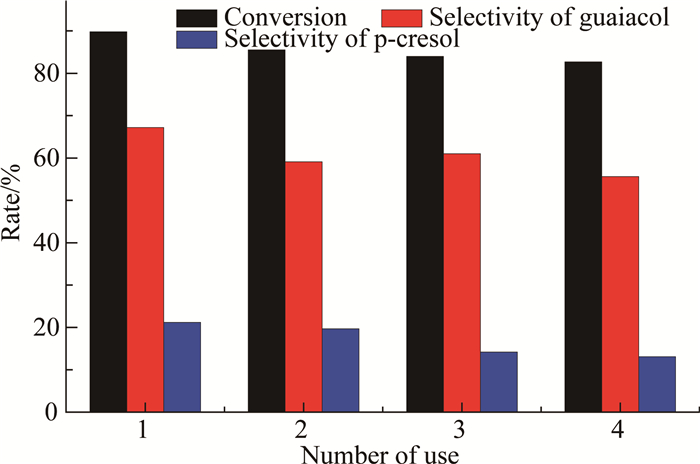
2.4 催化剂的重复使用情况在反应温度为220 ℃,反应时间为3 h的条件下,以50 mL乙醇为氢供体, 考察催化剂Pt/Ce0.5Zr0.5O2在香兰素加氢脱氧反应中的重复使用性能.将反应后的催化剂经过滤、干燥、煅烧后继续使用,重复4次后的实验结果如图 7所示,香兰素的转化率基本不变,4-甲基愈创木酚和愈创木酚的选择性也无太大变化,说明Pt/Ce0.5Zr0.5O2催化剂重复使用后活性仍然良好,表明其具有较高的水热稳定性,适用于香兰素加氢脱氧反应.
|
图 7 催化剂重复使用对香兰素加氢脱氧反应的影响 Fig. 7 The effect of recycling use of catalyst on the HDO of vanillin |
复合氧化物Ce0.5M0.5O2(M=Zr, Ti)可作为高水热稳定性的载体,故催化剂Pt/Ce0.5M0.5O2(M=Zr, Ti)具有优良的加氢脱氧性能. Pt/Ce0.5Zr0.5O2较于Pt/Ce0.5Ti0.5O2,催化性能更胜一筹,催化剂的加氢脱氧活性与其表面酸性以及贵金属Pt在载体上的高度分散有关.以含氢的有机小分子——低碳脂肪醇氢供体替代氢气作为氢源,应用于加氢脱氧催化反应.与采用氢气的加氢脱氧过程相比,低碳脂肪醇氢供体作为氢源兼溶剂,不仅能有效节能,大大减少氢气的消耗,而且来源广泛,易于储存和运输、安全性高、反应条件温和、设备要求低,有利于解决目前木质素乃至生物基化学品催化加氢脱氧过程中氢耗量大、设备要求高的问题,为生物质的催化转化提供了一种新的途径,是一种理想的氢供体.
| [1] | SAVALIYA M L, DHORAJIYA B D, DHOLAKIYA B Z. Recent advancement in production of liquid biofuels from renewable resources:A review[J]. Research on Chemical Intermediates, 2015, 41(2): 475–509. DOI:10.1007/s11164-013-1231-z |
| [2] | MÄKI-ARVELA P, MURZIN D. Hydrodeoxygenation of lignin-derived phenols:From fundamental studies towards industrial applications[J]. Catalysts, 2017, 7(9): 265–305. DOI:10.3390/catal7090265 |
| [3] |
张兴华, 陈伦刚, 张琦, 等. 木质素基酚类化合物加氢脱氧制取碳氢燃料[J].
化学进展, 2014, 26(12): 1997–2006.
ZHANG X H, CHEN L G, ZHANG Q, et al. Production of hydrocarbons via hydrodeoxygenation of lignin-derived phenolic compounds[J]. Progress in Chemistry, 2014, 26(12): 1997–2006. |
| [4] | SENOL O, RYYMIN E M, VILJAVA T R, et al. Reactions of methyl heptanoate hydrodeoxygenation on sulphided catalysts[J]. Journal of Molecular Catalysis A:Chemical, 2007, 268(1/2): 1–8. |
| [5] | FERRARI M, BOSMANS S, MAGGI R, et al. CoMo/carbon hydrodeoxygenation catalysts:Influence of the hydrogen sulfide partial pressure and of the sulfidation temperature[J]. Catalysis Today, 2001, 65(2/3/4): 257–264. |
| [6] | NIAZ S, MANZOOR T, PANDITH A H. Production of renewable diesel through the hydroprocessing of lignocellulosic biomass-derived bio-oil:A review[J]. Renewable and Sustainable Energy Reviews, 2016, 58: 1293–1307. DOI:10.1016/j.rser.2015.12.146 |
| [7] | FISK C A, MORGAN T, JI Y, et al. Bio-oil upgrading over platinum catalysts using in situ generated hydrogen[J]. Applied Catalysis A:General, 2009, 358(2): 150–156. DOI:10.1016/j.apcata.2009.02.006 |
| [8] | PANAGIOTOPOULOU P, MARTIN N, VLACHOS D G. Effect of hydrogen donor on liquid phase catalytic transfer hydrogenation of furfural over a Ru/RuO2/C catalyst[J]. Journal of Molecular Catalysis A:Chemical, 2014, 392: 223–228. DOI:10.1016/j.molcata.2014.05.016 |
| [9] | HUANG Y B, YANG Z, CHEN M Y, et al. Heterogeneous palladium catalysts for decarbonylation of biomass-derived molecules under mild conditions[J]. Chem Sus Chem, 2013, 6(8): 1348–1351. DOI:10.1002/cssc.201300190 |
| [10] | SUN Q, CHEN M, AGUILA B, et al. Enhancing the biofuel upgrade performance for Pd nanoparticles via increasing the support hydrophilicity of metal-organic frameworks[J]. Faraday Discuss, 2017, 201: 317–326. DOI:10.1039/C7FD00015D |
| [11] | LASKAR D D, TUCKER M P, CHEN X W, et al. Noble-metal catalyzed hydrodeoxygenation of biomass-derived lignin to aromatic hydrocarbons[J]. Green Chemistry, 2014, 16(2): 897–910. DOI:10.1039/c3gc42041h |
| [12] |
王枫濂, 楼辉, 陈平. 低碳醇用于香兰素加氢脱氧反应的研究[J].
浙江大学学报(理学版), 2016, 43(1): 28–34.
WANG F L, LOU H, CHEN P. The short-chain alcohol hydrogen donor for the hydrodeoxygenation of vanillin[J]. Journal of Zhejiang University (Science Edition), 2016, 43(1): 28–34. |
| [13] | HORI C E, PERMANA H, NG K Y S, et al. Thermal stability of oxygen storage properties in a mixed CeO2-ZrO2 system[J]. Applied Catalysis B Environmental, 1998, 16(2): 105–117. DOI:10.1016/S0926-3373(97)00060-X |
| [14] | ZHANG X H, LUO L T, DUANA Z H. Preparation and application of Ce-doped mesoporous TiO2 oxide[J]. Reaction Kinetics and Catalysis Letters, 2005, 87(1): 43–50. DOI:10.1007/s11144-006-0007-5 |
| [15] | DAMYANOVA S, PEREZ C A, SCHMAL M, et al. Characterization of ceria-coated alumina carrier[J]. Applied Catalysis A:General, 2002, 234(1/2): 271–282. |
| [16] | FANG J, BI X, SI D, et al. Spectroscopic studies of interfacial structures of CeO2-TiO2 mixed oxides[J]. Applied Surface Science, 2007, 253(22): 8952–8961. DOI:10.1016/j.apsusc.2007.05.013 |
| [17] | YANG S, ZHU W, JIANG Z, et al. The surface properties and the activities in catalytic wet air oxidation over CeO2-TiO2 catalysts[J]. Applied Surface Science, 2006, 252(24): 8499–8505. DOI:10.1016/j.apsusc.2005.11.067 |
| [18] | ARSLAN A, DOĞU T. Effect of calcination/reduction temperature of Ni impregnated CeO2-ZrO2 catalysts on hydrogen yield and coke minimization in low temperature reforming of ethanol[J]. International Journal of Hydrogen Energy, 2016, 41(38): 16752–16761. DOI:10.1016/j.ijhydene.2016.07.082 |
| [19] | SING K S W, EVERETT D H, HAUL R A W. Reporting physisorption data for gas/solid systems with special reference to the determination of surface area and porosity[J]. Pure Applied Chemistry, 2009, 54(11): 2201–2218. |
| [20] | FENG G, LIU Z, CHEN P, et al. Influence of solvent on upgrading of phenolic compounds in pyrolysis bio-oil[J]. Rsc Advances, 2014, 4(91): 49924–49929. DOI:10.1039/C4RA10891D |
| [21] | MARCUS Y. The properties of organic liquids that are relevant to their use as solvating solvents[J]. Chemical Society Reviews, 1993, 22: 409–416. DOI:10.1039/cs9932200409 |



