2. 浙江大学 化学系, 浙江 杭州 310027
2. Department of Chemistry, Zhejiang University, Hangzhou 310027, China
聚酯材料被视作最有可能替代传统塑料, 解决“白色污染”的新型生物可降解材料之一.与传统塑料相比,连接聚酯材料单体的酯键更易降解,从而被生物体或自然界代谢所吸收[1-7].近年来,学术界对生物可降解聚酯材料的研究一直抱有极大的兴趣.聚羟基丁酸酯(poly hydroxybutyrate, PHB)是1925年由法国微生物学家Maurice Lemoigne首次分离得到的一种天然聚酯材料. 20世纪70年代研究发现该类聚合物具有天然塑性,此后该化合物就被认为是最具开发价值的聚酯材料之一.
近年来,人们在对PHB合成和应用的研究过程中发现,与普通PHB相比,光学纯PHB结构更加明晰、应用范围更加广泛.研究表明,聚R-3-羟基丁酸酯可以稳定人体内的蛋白质以及多磷酸钙盐并能形成DNA通道[8].同时发现聚R-3-羟基丁酸乙酯广泛存在于细菌、真菌以及动植物的组织结构中[9-11].各项研究表明,聚R-3-羟基丁酸乙酯是“第5类在生理上具有重要作用的有机生物聚合物”[12].
PHB的合成方法包括生物合成法和化学合成法.研究表明,木醋杆菌、醋杆菌、农杆菌、氢细胞等在合适的条件下都能产生PHB[13].但是生物合成很难得到构型单一的聚3-羟基丁酸酯.单一构型的聚3-羟基丁酸酯多由化学合成法得到. JEDLINSKI等[14-16]发展了一种超分子催化β-丁内酯的立体选择性开环聚合合成聚R-3-羟基丁酸的方法. SEEBACH等[17-19]则采用R-3-羟基丁酸乙酯的四聚体合成聚合度为8,16,32,64,96和128的聚R-3-羟基丁酸酯.这些方法虽然为聚R-3-羟基丁酸酯的合成提供了多种途径,但是仍然存在催化剂昂贵、光学纯度不高等不足.因此,开发光学纯度高的聚R-PHB合成方法具有重要的理论和现实意义.
酶促聚合是近些年发展起来的一种新型聚合方法.该方法具有环境友好度高、立体选择性专一等优点,在手性聚酯合成中具有广泛的应用前景.以MEJER和HEISE为代表的课题组开发了一系列酶促开环聚合和酶促缩聚合成手性聚酯的方法,所得手性聚酯具有分子量高、分布窄以及光学纯度高等优点[20-22].因此,在充分借鉴酶促聚合反应优点的基础上发展了一种合成聚R-3-羟基丁酸乙酯的立体选择性缩合聚合方法.
本文建立的脂肪酶催化立体选择性动态动力学拆分/聚合合成聚R-3-羟基丁酸乙酯的方法如图 1所示.首先,考察了底物构型、溶剂等对聚合反应的影响,实现了酶促动力学拆分和聚合一锅合成聚R-3-羟基丁酸酯的目的.在此基础上结合过渡金属配合物对醇的原位外消旋化作用与酶促聚合反应,提出了更加绿色、高效的酶促动态动力学拆分/聚合一锅合成聚R-3-羟基丁酸酯的方法.通过该方法制备所得聚合物的分子量可以达到2.0×103 Da,同时聚合物降解所得单体ee值高达93%.此外,还通过改变聚合单体的光学纯度实现对聚合物分子量的调控,在不同光学纯度聚合单体的聚合反应中,聚合物的分子量可以较为均匀地分布在0.3×103~1.3×103 Da内.该方法具有高效、无毒等优点,对进一步研究手性聚酯的应用具有重要的理论和现实意义.

|
图 1 酶促立体选择性缩聚合成聚R-3-羟基丁酸酯 Fig. 1 Lipase-catalyzed stereo-selective condensation of rac-ethyl-3-hydroxybutyrate |
乙醇,乙醇钠,rac-3-羟基丁酸乙酯(分析纯,阿拉丁),R-3-羟基丁酸乙酯(分析纯,韶远试剂),S-3-羟基丁酸乙酯(分析纯,韶远试剂),Shov's试剂(分析纯,百灵威).
化合物的核磁共振氢谱(1H-NMR)采用Bruker Advance DMX 400MHz型核磁共振仪测定,其中四甲基硅烷(TMS)作为内标.
R/S-3-羟基丁酸乙酯的对映体过量值(ee %)采用手性气相色谱仪测定,型号为岛津2014C.检测条件为:手性色谱柱CP-chirasil-DEX CB 25×0.25 (Agilent),升温速度为1.0 ℃·min-1, 从70 ℃升至100℃,保持10 min.
1.2 实验过程 1.2.1 酶促动力学拆分/聚合合成聚R-3-羟基丁酸酯200 mg CAL-B(lipase B from Candida antarctica,南极假丝酵母脂肪酶,10 000 U·g-1,immobilized on)加入装有1.0 g rac-3-羟基丁酸乙酯的单口烧瓶中,并在氮气保护下加热至70 ℃反应24 h,然后拆去氮气保护抽真空.反应体系继续在0.01 MPa条件下反应48 h (70 ℃反应24 h,拆去氮气保护,将反应体系抽真空,反应压强维持在0.01 MPa,反应24 h).反应结束后,将反应体系冷却到室温,加入正己烷洗涤(5.0 mL×6),回收上清液并浓缩得到未反应的3-羟基丁酸乙酯,用手性气相检测其ee值.通过NMR和GPC分别表征所得聚合物的结构及分子量.
1.2.2 酶促动态动力学拆分/聚合合成聚R-3-羟基丁酸酯将200 mg CAL-B酶、10 mg Shov's试剂加入含有2.0 mL rac-3-羟基丁酸乙酯(1.0 g)苯甲醚溶液的单口烧瓶中,然后将烧瓶内的空气置换为氮气,并在氮气保护下加热到70 ℃预聚合24 h.待预聚合结束后,拆去氮气保护,将反应体系抽真空,反应压强维持在0.01 MPa,反应48 h.反应结束后,将反应体系冷却至室温,加入正己烷洗涤(5.0 mL×6),回收上清液并浓缩得到未反应的3-羟基丁酸乙酯,用手性气相检测其ee值.通过NMR和GPC分别表征所得聚合物的结构及分子量.
1.2.3 聚合物纯化动力学拆分/聚合所得聚合物由于分子量较低,形态为黏稠液体,纯化较为困难,因此通过正己烷不断洗涤就可以除去未反应的单体.动态动力学拆分/聚合所得聚合物的分子量较高,因此在反应结束分离所得粗产物后需要进一步纯化聚合物.具体操作过程为:将黏稠的产物溶于0.2 mL氯仿,并逐渐加入3.0 mL甲醇,然后将所得悬浊液放入4 ℃冰箱静置过夜.待聚合物完全析出后将上层清液移除,并用甲醇(1.0 mL)洗涤聚合物3次,然后真空干燥.
2 结果与讨论 2.1 聚R-3-羟基丁酸酯酶促动力学拆分/聚合一锅合成研究为实现酶促动态动力拆分/聚合一锅合成聚R-3-羟基丁酸乙酯,首先优化了酶促动力学拆分/聚合合成该手性聚合物的反应条件.在动力学拆分/聚合反应中,考察了酶的立体选择以及溶剂对反应结果的影响. CAL-B是立体选择性聚合反应以及动力学拆分反应中应用最广泛的脂肪酶之一,因此也被选择作为制备聚R-3-羟基丁酸酯的催化剂.分别考察了R-、S-、rac-3-羟基丁酸乙酯的酶促动力学拆分/聚合反应,结果如表 1所示.
| 表 1 酶促动力学拆分/聚合合成聚R-3羟基丁酸酯 Table 1 Lipase-catalyzed synthesis of Poly (R-HB) via kinetic resolution/polymerization a |
实验结果表明,CAL-B不能催化S-3-羟基丁酸乙酯的聚合反应,与CAL-B催化仲醇与仲胺的动力学拆分的立体选择性一致.当聚合单体为R-3-羟基丁酸乙酯时,聚合反应可以顺利进行,所得R-构型聚合物为白色固体,分子量能够达到1.3×103Da (见表 1, entry 4).当聚合单体为3-羟基丁酸乙酯外消旋体时,结果较差,所得聚合物为黏稠状液体,分子量仅为0.4 ×103 Da.通过计算可知,这些聚合物为三聚体或四聚体(见表 1, entry 1).尽管CAL-B催化rac-3-羟基丁酸乙酯的缩聚反应效率不高,其立体选择性仍然十分优异.反应结束后剩余单体的ee值高达90% (见表 1,entry 1~3).由此可知,该反应的立体构型选择性为R-构型.得到上述结果后,继续优化了rac-3-羟基丁酸乙酯的聚合反应条件,包括延长预聚合时间以及采用不同的反应溶剂等.结果显示,延长预反应时间对反应结果影响不大,而采用不同的溶剂(例如:DMF和苯甲醚)时,聚合度有一定程度的提高.聚合物的分子量从0.4 ×103 Da上升到0.6×103 Da,因此在后续反应中将采用溶剂聚合.
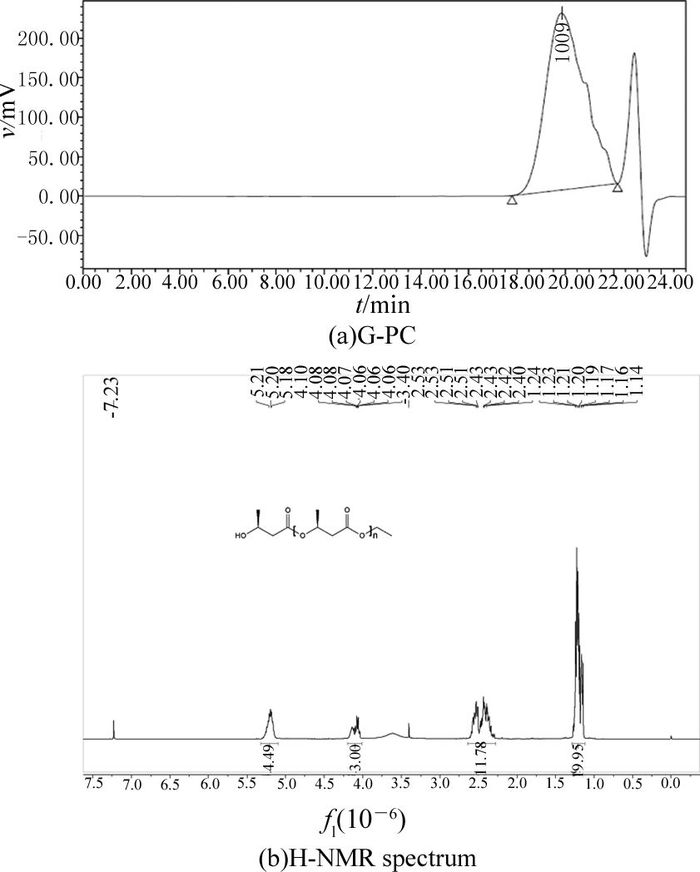
表 1中所有聚合物的分子量由GPC测定.以rac-3-羟基丁酸乙酯的聚合为例,GPC所测得的分子量为数均分子量,Mn=0.6×103 Da,重均分子量Mw为0.9×103 Da,多分散性DPI为1.45,如图 2(a)所示.还采用1H-NMR对聚合物的结构进行表征(见图 2(b)).同时,根据1H-NMR提供的信息计算聚合物的分子量.
|
图 2 聚R-3-羟基丁酸酯GPC与核磁氢谱 Fig. 2 GPC and 1H-NMR spectrum of Poly (R-HB) |
聚R-3-羟基丁酸酯的1H-NMR谱图中共有4组峰,分别为:δ=5.24×10-6~5.17 ×10-6 (主链次甲基氢)、δ=4.15×10-6~4.06 ×10-6(末端次甲基与亚甲基氢)、δ=2.57×10-6~2.34 ×10-6(主链亚甲基上氢)和δ=1.27×10-6~1.14×10-6(末端与主链甲基氢).由聚合物的1H-NMR谱图(δ=4.15×10-6~4.06×10-6,δ=1.27×10-6~1.14 ×10-6)2组峰的比例可知,聚合物末端为酯基. 图 1(b)中聚合物末端次甲基、亚甲基的吸收峰(δ=4.14×10-6~4.06 ×10-6)与聚R-3-羟基丁酸乙酯重复结构单元中次甲基的吸收峰(δ=5.24×10-6~5.17×10-6)之比可以计算末端与重复单元的比例,从而计算其分子量.具体计算公式如下:
| $n=\left( \frac{{{a}^{\prime }}}{{{b}^{\prime }}} \right):\left( \frac{a}{b} \right),$ |
其中,n为聚合物的聚合度, a′为聚合物主链次甲基吸收峰的面积积分, b′为聚合物末端次甲基、亚甲基吸收峰的面积积分, a为聚合单体次甲基吸收峰的面积积分, b为聚合单体末端次甲基、亚甲基吸收峰的面积,根据单体结构可知(a/b)=1/3.
由上述公式计算得图 1(b)聚合物的聚合度为4.5,分子量为0.5×103Da.该分子量与GPC测定的一致,因此在后续实验中将直接采用1H-NMR计算所得的聚合物的分子量.
2.2 聚R-3-羟基丁酸酯酶促动态动力学拆分/聚合一锅合成研究通过优化溶剂、底物构型等反应条件后获得分子量为1.3×103Da的聚R-3-羟基丁酸酯.但是动态动力学拆分/聚合的底物利用效率仍然较低.反应中只用S-构型聚合单体参加反应,反应的最大理论产率为50%.除此之外,S-构型聚合单体的存在会阻碍聚合反应的顺利进行.聚合过程S-构型单体的羰基可以参与反应,与R-构型单体的羟基反应生成大量含S-构型的寡聚物.这些寡聚物的存在会产生一种封端效应,从而降低寡聚物的反应活性,最终导致聚合物分子量过低(见图 3).为了克服动力学拆分/聚合的上述缺点,结合过渡金属配合物进行醇的原位消旋化以及酶的立体选择性拆分,实现了酶促动态动力学拆分/聚合制备聚R-3-羟基丁酸酯的目的.

|
图 3 S-构型单体阻碍聚合机理示意图 Fig. 3 Inhibition mechanism of S-substrate in the polymerization |
近年来,过渡金属催化醇或胺的酶促动态动力学研究发展迅速,各种消旋化试剂层出不穷,其中使用最广泛的是金属钌(Ru)的配合物.本文采用shov's试剂来实现rac-3-羟基丁酸乙酯的消旋.实验结果表明, 将shov's试剂引入反应体系后,聚合物分子量可以得到较大提高.最优条件下得到的聚R-3-羟基丁酸乙酯分子量可达到2.0×103 Da,同时反应的转化率维持在89%.所得聚合物的结构和分子量通过1H-NMR表征,如图 4所示.

|
图 4 聚R-3-羟基丁酸酯的核磁氢谱 Fig. 4 1H-NMR spectrum of Poly (R-HB) |
在利用核磁成功对聚合物分子量进行表征的基础上,还对聚合物的光学纯度进行了测试.聚合物与小分子化合物不同,其光学纯度很难利用色谱进行表征.因此,采用检测其降解后单体的ee值来间接表征聚合物的ee值.最初通过气相色谱分别检测了聚R-3-羟基丁酸乙酯的水解产物和醇解产物.由于聚R-3-羟基丁酸乙酯的水解产物3-羟基丁酸的标样很难在气相色谱检测中实现基线分离,若要准确测得3-羟基丁酸的ee值, 则需要对3-羟基丁酸进一步衍生化.因此采用聚R-3-羟基丁酸乙酯的醇解产物来间接表征聚合物的ee值,具体结果如图 5所示. 图 5中保留时间为13.48 min的色谱峰为R-3-羟基丁酸乙酯,保留时间为13.7 min的色谱峰为S-3-羟基丁酸乙酯.测试结果显示,通过该方法制备的聚R-3-羟基丁酸乙酯的ee值高达93%.

|
图 5 聚R-3-羟基丁酸乙酯醇解产物的气相色谱图 Fig. 5 Monomer GC spectrum of poly (R-PHB) |
控制聚合反应的进度一直是高分子合成中的难点之一.在研究过程中发现,S-构型单体在聚合过程中会产生封端效应, 因此尝试了R-/S-比例不同的聚合单体的酶促聚合反应,以期达到控制反应进度的目的,从而实现对聚合物分子量的调控.
研究过程中一共考察了7组不同R-、S-比例聚合单体的聚合反应,结果如图 6所示.从图 6中可以看出,当反应底物全部由S-构型的底物组成时,不能得到聚3-羟基丁酸乙酯.随着R-构型单体比例的不断增加,可以得到不同分子量的聚合物,其分子量与R-构型单体的含量成正比.当聚合单体R-/S-达到5:1时,聚合物分子量基本达到稳定(1.3×103 Da),继续增加R-构型的含量对聚合物分子量的影响不大.产生这一现象的原因可能是当聚合单体R-/S-达到5:1后继续增加R-构型单体,使得聚合过程中形成含S-单体寡聚物的几率大大降低,因此所得聚合物分子量也与纯R-构型单体的聚合反应所得聚合物的分子量接近.

|
图 6 R-与S-构型比例对聚合物分子量的影响 Fig. 6 Effect of different substrates ratio (R:S) on the molecular weights of poly (R-PHB) |
报道了一种高效的酶促动态动力学拆分/聚合合成聚R-3-羟基丁酸酯的方法.研究过程中充分考虑了底物构型、溶剂等因素对酶促聚合反应的影响.通过该方法制备所得聚合物的分子量可以达到2.0×103Da,同时聚合物降解所得单体ee值高达93%;此外,还考察了聚合单体R-和S-比例对聚合物分子量的影响.研究结果表明:不同比例的R-、S-单体制备的聚合物分子量可以比较均匀地分布在0.2×103~1.3×103Da.该方法具有高效、无毒等优点,对进一步研究手性聚酯的应用具有重要的理论和现实意义.
| [1] | POULHES F, MOUYSSET D, GIL G, et al. Novozym 435-catalyzed synthesis of polyetherimides from amino-esters, or diesters and diamines built on ethylene-and diethylene-glycol moieties[J]. Polymer, 2012, 53: 1172–1179. DOI:10.1016/j.polymer.2012.01.054 |
| [2] | XU F L, ZHONG J R, QIAN X Q, et al. Multifunctional poly(amine-ester)-type hyperbranched polymers:Lipase-catalyzed green synthesis, characterization, biocompatibility, drug loading and anticancer activity[J]. Polym Chem, 2013(4): 3480–3490. |
| [3] | YAMAGUCHI S, TANHA M, HULT A, et al. Green polymer chemistry:lipase-catalyzed synthesis of bio-based reactive polyesters employing itaconic anhydride as a renewable monomer[J]. Polymer Journal, 2014, 46: 2–13. DOI:10.1038/pj.2013.62 |
| [4] | INPRAKHON P, PANLAWAN P, PONGTHARANKUL T, et al. Toward one-pot lipase-catalyzed synthesis of poly (ε-caprolactone) particles in aqueous dispersion[J]. Colloids and Surfaces B:Biointerfaces, 2014, 113: 254–260. DOI:10.1016/j.colsurfb.2013.09.011 |
| [5] | JIANG Z Z, ZHANG J W. Lipase-catalyzed synthesis of aliphatic polyesters via copolymerization of lactide with diesters and diols[J]. Polymer, 2013, 54: 6105. DOI:10.1016/j.polymer.2013.09.005 |
| [6] | ZHAO X Y, SUN L, WANG M Z, et al. Review of crosslinked and non-crosslinked copolyesters for tissue engineering and drug delivery[J]. Polym Int, 2014, 63: 393–401. DOI:10.1002/pi.2014.63.issue-3 |
| [7] | MA J P, PANG Y, WANG M, et al. The copolymerization reactivity of diols with 2, 5-furandicarboxylic acid for furan-based copolyester materials[J]. J Mater Chem, 2012, 22: 3457–3461. DOI:10.1039/c2jm15457a |
| [8] | REUSCH R N. Biological complexes of poly-β-hydroxybutyrate[J]. FEMS Microhiol Rev, 1992, 103: 119–130. |
| [9] | NAVES A F, FERNANDES H T C, IMMICH A P S, et al. Enzymatic syntheses of unsaturated polyesters based on isosorbide and isomannide[J]. Journal of Polymer Science, Part A:Polymer Chemistry, 2013, 51: 3881–3891. DOI:10.1002/pola.v51.18 |
| [10] | KELLER A. CORRIGENDUM:Polymer crystals[J]. Reports on Progress in Physics, 1969, 32(2): 769. DOI:10.1088/0034-4885/32/2/508 |
| [11] | WELLAND E J, STEJNY J, HALTER A, et al. Selective degradation of chain folded single crystals of poly (β-hydroxybutyrate)[J]. Polym Commun, 1989, 30: 302–304. |
| [12] | SEEBACH D, BRUNNER A, BURGER H M, et al. Isolation and 1H-NMR spectroscopic identification of poly (3-Hydroxybutanoate) from Prokaryotic and Eukaryotic organisms[J]. Eur J Biochem, 1994, 224: 317–328. DOI:10.1111/ejb.1994.224.issue-2 |
| [13] | POOL R. The periaqueductal gray matter mediates opiate-induced immunosuppression[J]. Science, 1989, 245: 188–190. DOI:10.1126/science.2749256 |
| [14] | JEDLIN'SKI Z, KURCOK P, LENZ R W. First facile synthesis of biomimetic poly-(R)-3-hydroxybutyrate via regioselective anionic polymerization of (S)-β-butyrolactone[J]. Macromolecules, 1998, 31: 6718–6720. DOI:10.1021/ma980663p |
| [15] | JEDLIN'SKI Z, KURCOK P, ADAMUS G, et al. Biomimetic polyesters and their role in ion transport across cell membranes[J]. Acta Biochim Pol, 2000, 47: 79–85. |
| [16] | JEDLIN'SKI Z, ADAMUS G, KOWALCZUK SCHUBERT M R, et al. Electrospray tandem mass spectrometry of poly (3-hydroxybutanoic acid) end groups analysis and fragmentation mechanism[J]. Rapid Commun Mass Spectrom, 1998, 12: 357–360. DOI:10.1002/(ISSN)1097-0231 |
| [17] | SEEBACH D, BVRGER H M, MVLLER H M, et al. Synthesis of linear oligomers of (R)-3-hydroxybutyrate and solid-state structural investigations by electron microscopy and X-ray scattering[J]. Helv Chim Acta, 1994, 77: 1099–1123. DOI:10.1002/hlca.v77:4 |
| [18] | LENGWEILER U D, FRITZ M G, SEEBACH D. Synthase monodisperser linearer und cyclischer oligomere der (R)-3-hydroxybuttersäure mit bis zu 128 Einheiten[J]. Helv Chim Acta, 1996, 79: 670–701. DOI:10.1002/hlca.v79:3 |
| [19] | BACHMANN B M, SEEBACH D. Synthesis and structure of linear and cyclic oligomers of 3-hydroxybutanoic acid with specific sequences of (R)-and (S)-configurations[J]. Helv Chim Acta, 1998, 81: 2430–2461. DOI:10.1002/(ISSN)1522-2675 |
| [20] | BUIJTENEN J V, MEULDIJK J, PALMANS A R A, et al. Chiral polymers by iterative tandem catalysis[J]. Chem Commun, 2006, 30: 3169–3171. |
| [21] | BUIJTENEN J, VERBRUGGEN M, ROUMEN L, et al. Switching from S-to R-selectivity in the Candida antarctica Lipase B-catalyzed ring-opening of ω-methylated lactones:Tuning polymerizations by ring size[J]. J Am Chem Soc, 2007, 129: 7393–7398. DOI:10.1021/ja071241a |
| [22] | HILKER I, RABANI G, VERZIJL G K M, et al. Chiral polyesters by dynamic kinetic resolution polymerization[J]. Angew Chem Int Ed, 2006, 45: 2130–2132. DOI:10.1002/(ISSN)1521-3773 |



