矿物燃料在燃烧过程中所产生的氮氧化物会造成光化学烟雾、酸雨和臭氧层破坏等一系列严重的大气污染问题.针对此问题,世界各国制定了相应的排放法规,如美国环境保护署制定了Tier 2法规,严格控制轻型和重型柴油车尾气污染物的排放[1].至今,NH3-SCR是脱除NOx最有效的技术,广泛应用的催化剂多为V基的V-W-Ti复合氧化物[2-5].然而,该类催化剂存在诸多缺点,如:(1) V物种具有生物毒性;(2) 催化剂的低温活性较差,且活性温度窗口窄;(3) V物种的强氧化能力能将SO2氧化成SO3[6-8].为了改善催化剂的NH3-SCR性能,近年来,人们对非V基催化剂进行了广泛研究.金属改性分子筛催化剂由于其高活性、高N2选择性以及良好的水热稳定性而成为新一代NH3-SCR催化材料,如Fe-zeolite和Cu-zeolite已成为研究的热点[9-15],这些催化剂具有很好的N2选择性,几乎不产生N2O等副产物.与Cu-zeolite相比,Fe-zeolite的低温催化活性稍差,但其具有更好的水热稳定性和耐SO2中毒性能.然而,柴油车在平稳的道路上行驶时,排放的尾气平均温度要低于150 ℃[16],这就要求催化剂在低温条件下(200 ℃以下)也要具有很好的SCR活性.提高NOx低温转化率的常用方法是在SCR催化剂上游使用柴油氧化催化剂(DOC)[17],DOC可以提高尾气中NO2的浓度,从而提高NOx低温转化率,但DOCs价格昂贵且易失活.为了进一步提高铁基催化剂的低温活性,同时拓宽其活性温度窗口,仅仅依靠Fe来改性分子筛是较难达到的,需要同时添加其他改性金属元素.考虑到铜改性分子筛催化剂优良的低温活性,在铁基分子筛催化剂中掺入铜,或许可以通过Fe、Cu的协同作用而进一步改善铁基催化剂的低温SCR活性[18-20],这对于开发可实际应用的高效SCR催化剂具有重要意义.
本文以Fe/β(40) 催化剂为基础,研究了Cu添加量对Cu-Fe/β(40) 催化剂NH3-SCR性能的影响.通过离子体发射光谱(ICP-AES)、X射线衍射(XRD)、H2程序升温还原(H2-TPR)、紫外可见光谱(UV-vis)和X射线电子能谱(XPS)等表征手段,系统分析铜掺杂对铁活性物种及催化剂物化性质的影响,同时还考察了Cu-Fe/β(40) 催化剂的水热稳定性和抗SO2性能.
1 实验部分 1.1 催化剂的制备以H-β(SiO2/Al2O3=40) 为载体,采用溶液离子交换法(IE)制备Cu/β(40) 催化剂.首先,用NH4NO3溶液与β(40) 粉末进行离子交换,将混合后形成的浆体在80 ℃水浴条件下搅拌2 h;用布什漏斗过滤,并用大量去离子水洗涤,直至滤液呈中性,之后100 ℃干燥2 h.将所得NH4-β(40) 粉末与不同浓度的(CH3COO)2Cu溶液混合,于80 ℃水浴条件下搅拌3 h,经过滤,用去离子水充分洗涤至中性,所得滤饼100 ℃干燥2 h.最后在空气气氛下500 ℃焙烧5 h,压片,过筛(40~60目),通过等离子体发射光谱(ICP-AES)测定铜交换量,催化剂分别标记为0.23Cu/β(40)、0.54Cu/β(40)、1.27Cu/β(40) 和4.11Cu/β(40).
采用等体积浸渍法制备Cu-Fe/β(40) 催化剂.以上述制得的一系列Cu/β(40) 分子筛为载体,将一定量的Cu/β(40) 分子筛粉末浸渍在一定浓度的Fe(NO3)3溶液中,室温下搅拌过夜,然后经80 ℃水浴烘干,110 ℃下干燥2 h、空气气氛下500 ℃焙烧5 h,压片过筛(40~60目),Fe的质量分数固定为2%.各催化剂分别标记为0.23Cu-2Fe/β (40)、0.54Cu-2Fe/β (40)、1.27Cu-2Fe/β (40) 和4.11Cu-2Fe/β (40).
为了考察催化剂的水热稳定性,将新鲜的2Fe/β(40)、1.27Cu/β(40) 和1.27Cu-2Fe/β(40) 催化剂放在自制的水热老化设备上进行水热老化,老化时间为24 h,气氛中水蒸气体积分数为10%,老化温度为700 ℃.
1.2 催化剂活性测试催化剂性能评价在自制的催化剂评价微反应装置上进行.反应气氛组成(体积分数)为:0.05% NOx、0.05% NH3、5% O2,Ar为平衡气,气体总流量为160 mL·min-1, 空速48 000 h-1.使用Bruker EQUINOX 55型红外仪(气体池体积1.33 L,光路长10 m,分辨率2 cm-1)记录反应前后NO、NO2、N2O和NH3气体的浓度变化.SCR评价测试温度为100~550 ℃.反应中NOx转化率、NH3转化率计算公式如下:
| $\begin{array}{l} {\rm{N}}{{\rm{O}}_{x{\rm{conversion}}}} = \frac{{{\rm{N}}{{\rm{O}}_{x{\rm{inlet}}}} - {\rm{N}}{{\rm{O}}_{x{\rm{outlet}}}}}}{{{\rm{N}}{{\rm{O}}_{x{\rm{inlet}}}}}} \times 100\% ,\\ {\rm{N}}{{\rm{H}}_{3{\rm{conversion}}}} = \frac{{{\rm{N}}{{\rm{H}}_{3{\rm{inlte}}}} - {\rm{N}}{{\rm{H}}_{3{\rm{outlet}}}}}}{{{\rm{N}}{{\rm{H}}_{3{\rm{inlte}}}}}} \times 100\% . \end{array}$ |
为了考察催化剂的抗SO2性能,1.27Cu-2Fe/β(40) 催化剂分别在含有0, 50×10-6和100×10-6 SO2的反应气氛中连续反应10 h,反应温度为170 ℃.
1.3 催化剂的表征XRD测定:采用Shimazu XRD 7000型X射线衍射仪测定,测试使用CuKα靶,管电压为40 kV,管电流为30 mA,扫描范围为5°<2θ<70°,扫描速率为5°·min-1,步长为0.02°.
离子体发射光谱(ICP-AES)测定:催化剂中活性组分的实际含量在IRIS IntrepidⅡXSP型全谱等离子体发射光谱仪(美国热电公司)上测定.样品用浓盐酸预处理.
H2-TPR测定:将100 mg样品置于U型石英反应管中,在高纯氮(纯度99.999%)气氛中400 ℃预处理0.5 h,再冷却至50 ℃,然后将气氛切换为体积分数为5%H2/Ar,流速控制为40 mL·min-1,待基线走稳后程序升温,升温速率为10 ℃·min-1,热导检测器(TCD)检测.还原过程中产生的水用5A分子筛吸收.
紫外可见光谱(UV-vis DRS)测定:催化剂表面物种类型在UV-2401 PC (Shimadzu)仪器上测定,采用统一标准制样,波长测量范围为200~800 nm.测量所得谱图通过origin软件进行分峰处理.
X-射线光电子能谱(XPS)测定:催化剂的表面元素含量及结合能在Thermo ESCALAB 250系统上测定,Al-Kα射线,20 eV/150 W,电子能量1 486.6 eV.所有谱图用C1s的结合能(284.8 eV)作为基准进行校正.
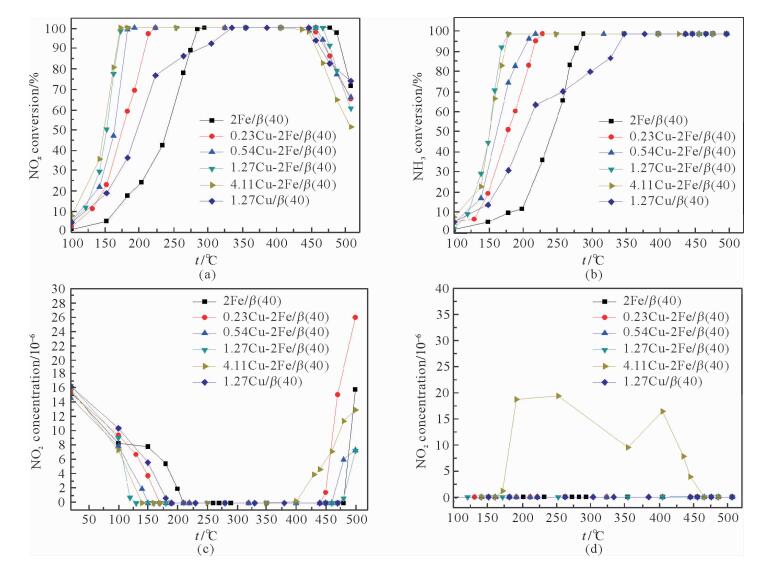
2 结果与讨论 2.1 NH3-SCR催化性能研究 2.1.1 新鲜Cu-Fe/β(40) 催化剂的活性评价图 1(a)给出了不同铜添加量的Cu-Fe/β(40) 催化剂上的NOx转化率曲线.从图(a)中可知,随着Cu添加量的增加,Cu-Fe/β(40) 催化剂的低温活性明显改善,高温活性略有降低,活性温度窗口明显拓宽.当Cu添加质量比达到1.27%时,低温活性达到最佳,活性温度窗口最宽,即165 ℃时NOx转化率就可达到90%,且温度在170~460 ℃时都可实现对NOx的完全转化.在此基础上,进一步添加Cu,当Cu添加质量比达到4.11%时,低温活性几乎不再提高,高温活性反而有所下降.图 1(b)是各催化剂上NH3的转化率曲线.随着温度升高,NH3的转化率也逐渐增加,其变化趋势与NOx转化率的变化趋势一致,表明NH3的消耗与NOx的还原反应密切相关.图 1(c)是反应过程中NO2的浓度变化曲线,原始反应气中含有少量NO2(~16×10-6),随着温度的升高,NO2逐渐被还原浓度降低,但NO2完全转化的温度远远低于NO完全转化的温度,这意味着在低温状态下NH3-NO2的SCR反应比NH3-NO更容易进行[21];当反应温度超过400 ℃时,会逐渐生成少量NO2,这与部分NH3被氧化有关;另一方面,NH3被部分氧化而造成还原剂不足,致使高温条件下NOx转化率下降.图 1(d)是副产物N2O的浓度曲线.从图 1(d)中可以看出,只有4.11Cu-2Fe/β(40) 催化剂上生成了N2O,最大量约为20×10-6,并且随着温度的升高,N2O生成量逐渐减少至0,这说明过量的Cu添加会降低催化剂反应过程中的N2选择性.
|
图 1 不同Cu添加量Cu-Fe/β(40) 催化剂的NH3-SCR性能 Fig. 1 NH3-SCR activity test of various Cu-Fe/β(40) catalysts |
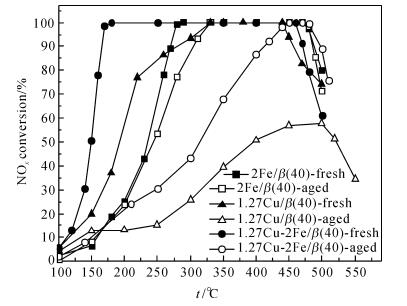
高温水热老化处理后催化剂样品的活性评价结果如图 2所示.对于2Fe/β(40) 催化剂,老化后样品的低温活性有所下降,高温活性几乎不变;对于1.27Cu/β(40) 催化剂,老化后样品的SCR活性大幅降低,NOx转化率最大值仅为58%左右,表明1.27Cu/β(40) 的抗水热老化性能很差;对于1.27Cu-2Fe/β(40) 催化剂,老化后样品的SCR活性也大幅降低,老化前后90% NOx转化率温度窗口分别为165 ~ 470 ℃和410 ~ 500 ℃,表明水热老化处理对于1.27Cu-2Fe/β(40) 催化剂的SCR活性影响很大,同时也表明Cu的添加大大降低了Fe/β(40) 催化剂的水热稳定性.
|
图 2 水热老化对2Fe/β(40)、1.27Cu/β(40) 和1.27Cu-2Fe/β(40) 催化剂上NOx转化率的影响 Fig. 2 Effect of hydrothermal aging on NOx conversion of 2Fe/β(40), 1.27Cu/β(40) and 1.27Cu-2Fe/β(40) catalysts |
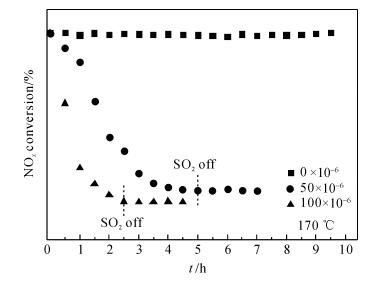
在NOx初始转化率约为95%时的反应温度(170 ℃)下,含不同浓度SO2的反应气持续通过1.27Cu-2Fe/β(40) 催化剂,催化剂活性的变化情况如图 3所示.SO2浓度为0时,1.27Cu-2Fe/β(40) 催化剂上NOx转化率在10 h内保持在95%几乎不变;当反应气中加入SO2后,催化剂的活性随着时间的变化而明显降低,在50×10-6和100×10-6 SO22种情况下,1.27Cu-2Fe/β(40) 的NOx转化率在2.5 h内就从95%分别降至41.2%和17.2%.表明1.27Cu-2Fe/β(40) 催化剂对SO2非常敏感.另外,从图 3中可以看出,反应气中停止通SO2后,催化剂的活性几乎维持不变,不会恢复为初始活性,这可能与催化剂表面生成的硫酸盐物种覆盖了活性位有关,因为在170 ℃的低温反应条件下这些硫酸盐物种是难以分解去除的.
|
图 3 SO2对1.27Cu-2Fe/β(40) 催化剂活性的影响 Fig. 3 Effect of SO2 on NOx conversion of 1.27Cu-2Fe/β(40) catalyst |
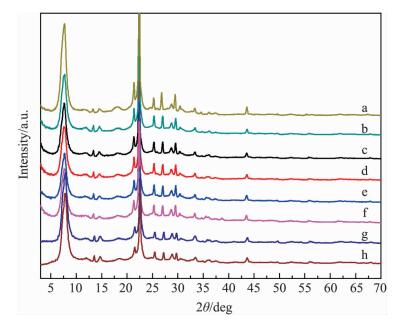
图 4为Cu交换量不同的Cu-Fe/β(40) 系列催化剂及老化后样品的XRD图谱.从图 4可以看出,在2Fe/β(40) 的基础上,添加第2种金属Cu后,新鲜催化剂的XRD谱图(a~f)没有发生明显改变,表明Cu的交换和Fe的负载并没有破坏原来β(40) 分子筛的晶相结构,金属氧化物负载后的Cu-Fe/β(40) 催化剂依然具有规则多孔以及较高结晶度的微观结构特征.此外,在所有新鲜催化剂样品的XRD谱图上均没有发现明显的FeOx或者CuOx物种的晶相衍射峰,表明FeOx或者CuOx物种在β(40) 分子筛表面有很好的分散性,或者所形成的团聚物种的表观粒径不超过3 nm,未达到XRD的检测限.另外,对于2个老化后样品,XRD图谱中仍存在β(40) 分子筛的特征衍射峰,强度也没有明显变化,说明高温水热老化并未导致分子筛的骨架坍塌;同时,两谱图(g~h)中也没有出现与FeOx或者CuOx物种有关的明显特征衍射峰.
|
图 4 各Cu-Fe/β(40) 催化剂的XRD图谱 Fig. 4 XRD patterns of different Cu-Fe/β(40) catalysts (a)H-β(40), (b)2Fe/β(40), (c)0.23Cu-2Fe/β(40), (d)0.54Cu-2 Fe/β(40), (e)1.27Cu-2Fe/β(40), (f)4.11Cu-2Fe/β(40), (g)2Fe/β(40)-aged and (h)1.27Cu-2Fe/β(40)-aged catalysts. |
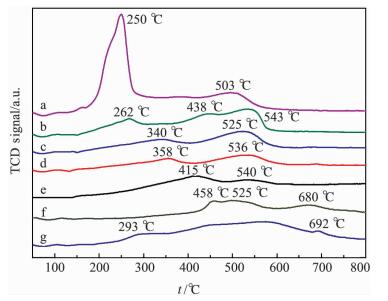
为了研究催化剂的氧化还原性,对新鲜和水热老化样品进行H2-TPR表征.由图 5结果可知,2Fe/β(40) 在415 ℃和540 ℃附近出现了2个还原峰[22],分别归属于孤立Fe3+的还原和低聚FeOx的还原.但在添加Cu后各还原峰温度明显下降,并随着Cu添加量的增加而下降,说明Fe、Cu物种间可能存在较强的相互作用,使得催化剂的还原能力提高.各催化剂的起始还原温度无明显的差别,但其峰温从高到低为4.11Cu-2Fe/β(40)<1.27Cu-2Fe/β(40)<0.54Cu-2Fe/β(40)<0.23Cu-2Fe/β(40)<2Fe/β(40).与2Fe/β(40) 类似,各Cu-Fe/β(40) 催化剂上的低温还原峰可能分别归属于纳米尺度上CuOx物种、Fe3+物种的还原,而高温还原峰可能与分散较好的FeOx物种的还原有关[18, 21].1.27Cu-2Fe/β(40) 在438 ℃附近出现了一个新的还原峰,可能与Cu2+物种的还原有关[23-25].结合活性评价结果,认为较高的低温还原能力可能与1.27Cu-2Fe/β(40) 和4.11Cu-2Fe/β(40) 在140~180 ℃低温段就具有高催化活性有关,因为还原温度越低,低温下越容易将NO氧化为NO2, 而NH3-NO2反应(快速SCR反应)相比于NH3-NO反应(标准SCR反应)更易快速发生[21],进而能够提高催化剂的低温活性.另外,4.11Cu-2Fe/β(40) 催化剂上形成了较多的CuO物种,这可能是N2选择性下降的主要原因.对于老化后的样品,680 ℃左右出现了一个还原峰,归属于铁氧化合物FeO的还原[26-28],表明水热老化过程中铁物种发生了团聚,但其XRD结果中没有观察到该物相的存在,这可能与Fe负载量较低有关.以上H2-TPR结果说明,Fe与Cu物种间的相互作用会影响Cu-Fe/β(40) 催化剂的氧化还原性能,进而影响其催化性能.
|
图 5 各Cu-Fe/β(40) 催化剂的H2-TPR图谱 Fig. 5 H2-TPR profiles of different Cu-Fe/β(40) catalysts (a)4.11Cu-2Fe/β(40), (b)1.27Cu-2Fe/β(40), (c)0.54Cu-2 Fe/β (40), (d)0.23Cu-2Fe/β(40), (e)2Fe/β(40), (f) 2Fe/β(40)-aged and (g) 1.27Cu-2Fe/β(40)-aged catalysts. |
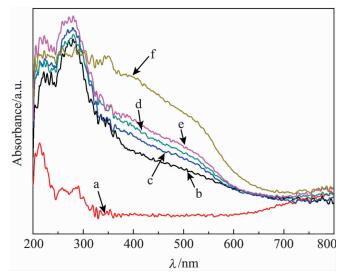
图 6给出了各催化剂的UV-vis DRS图谱.可以看出,对于2Fe/β(40),紫外区间的吸收光谱归属于O→Fe3+电荷转移跃迁(LMCT),可见光区间的吸收谱归属于α-Fe2O3中Fe的d-d跃迁[29-30];对于1.27Cu/β(40),215和280 nm左右的谱峰分别归属于Ozeolite → Cu2+和O2- → Cu2+的电荷转移[31-32].同时,根据文献[33-35],Cu/zeolites中300~500 nm间出现的谱峰为O-Cu-O和Cu-O-Cu的电荷转移,500~800 nm间的谱峰归属于CuO中Cu2+的d-d跃迁;由此,对于Cu-Fe/β(40) 催化剂,300 nm以下的谱峰共同归属于离子交换位的单核Fe3+和游离的Cu2+物种,300~800 nm的谱峰共同归属于FexOy、CuOx、Fe2O3和CuO物种.从图 6中还可以看出,随着Cu交换量的增加,低波段(<300 nm)谱图强度先变大后变小,1.27Cu-2Fe/β(40) 催化剂的谱图强度最强,表明催化剂中存在较多离子交换位的Fe3+和Cu2+物种;高波段(>300 nm)谱图逐渐变宽和变强,表明过量的Cu会形成CuOx和CuO物种.结合活性评价结果可知,Cu-Fe/β(40) 催化剂的低温活性提高与存在较多的Cu2+物种有关,而催化剂的N2选择性降低可能与存在较多的CuO物种有关.图 6的UV-vis DRS结果亦说明,Cu-Fe/β(40) 催化剂中含有多个活性物种,各种Fe、Cu物种的共同作用决定了催化剂的SCR活性,1.27Cu-2Fe/β(40) 催化剂的低温SCR活性较高可能与其存在较多离子交换位的Fe3+和Cu2+物种有关.
|
图 6 各Cu-Fe/β(40) 催化剂的UV-vis DRS图谱 Fig. 6 UV-vis DRS profiles of different Cu-Fe/β(40) catalysts (a)1.27Cu/β(40), (b)2Fe/β(40), (c)0.23Cu-2Fe/β(40), (d)0.54Cu-2Fe/β (40), (e)1.27Cu-2Fe/β(40) and (f)4.11Cu-2Fe/β(40) catalysts. |
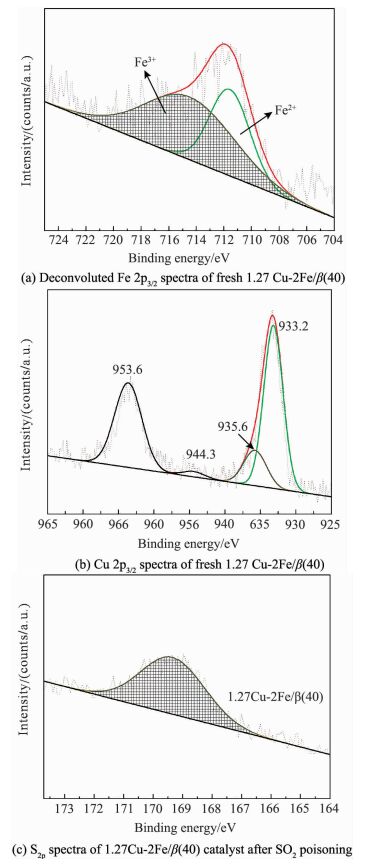
用XPS进一步研究了2Fe/β(40) 和1.27Cu-2Fe/β(40) 催化剂中表面Fe和Cu的原子百分数和化学状态.图 7给出了催化剂的XPS谱图及分峰结果,表 1给出了由XPS分析得到的催化剂表面Fe、Cu原子百分数及化学状态.从图 7(a) Fe 2p3/2的XPS图谱可以看出,Cu-2Fe/β(40) 催化剂中同时存在2种价态的铁物种.从图 7(b) Cu 2p3/2的XPS谱图可以看出,935.6和933.2 eV处出现2个谱峰,对于结合能为935.6 eV的Cu 2p3/2谱峰,由于其在更高结合能944.3 eV处有一个伴随卫星峰,并且还存在结合能为953.6 eV的Cu 2p1/2谱峰,因此可将该峰归属为CuO物种中Cu2+的XPS谱峰,而结合能为933.2 eV的Cu 2p3/2峰归属于Cu+的XPS谱峰[33, 36].
| 表 1 由XPS分析所得的表面Fe、Cu原子百分数及化学状态 Table 1 Surface contents of Fe and Cu and surface atom ratios in the catalysts measured by XPS analysis |
|
图 7 各Cu-Fe/β(40) 催化剂的XPS谱图 Fig. 7 XPS results of 2Fe/β(40) and 1.27Cu-2Fe/β(40) catalysts |
表 1给出了分峰结果,可知添加Cu之后1.27Cu-2Fe/β(40) 催化剂表面的Fe原子百分数高于2Fe/β(40) 催化剂,表明Cu占据了部分离子交换位而形成了Cu2+物种,使得Cu-Fe/β(40) 催化剂的低温活性提高;对于老化后的样品,其表面的Cu原子百分数减少,且Cu2+比例大幅增加,表明水热过程中表面部分Cu物种在热动力驱动下迁移至分子筛孔道内,以CuOx或CuO物种形式存在,这可能是样品老化后其低温活性降低的主要原因.另外,为了得到表面硫物种的价态,用XPS表征1.27Cu-2Fe/β(40) 催化剂的硫物种.从图 7(c)中可以看出,S2p的结合能位于169.3 eV[37],属于硫酸盐物种.表明硫中毒过程中1.27Cu-2Fe/β(40) 催化剂表面会形成硫酸盐物种,从而使Cu-Fe/β(40) 催化剂的抗SO2性能降低.同时,硫中毒的1.27Cu-2Fe/β(40) 催化剂表面的Fe、Cu原子百分数减少,且Cu2+和Fe3+比例增加,表明在含SO2的反应气氛条件下,Cu+和Fe2+分别变为Cu2+和Fe3+,而且,生成的硫酸盐物种可能会进入分子筛孔道并覆盖活性位[38-39],再加上Cu活性位上SO2与NOx的竞争吸附[40],导致1.27Cu-2Fe/β(40) 催化剂的抗SO2性能大大降低.
3 结论 3.1适量Cu添加能够明显提高Fe/β(40) 催化剂的低温活性,拓宽其活性温度窗口,但过量Cu会降低催化剂的N2选择性.Cu存在量为1.27%的1.27Cu-2Fe/β(40) 催化剂表现出最佳SCR性能,温度在165 ℃~470 ℃时NOx转化率均在90%以上,且N2选择性为100%.
3.2Cu、Fe物种间的相互作用会影响催化剂的氧化还原性和活性物种的分布,Cu-Fe/β(40) 催化剂良好的低温SCR活性与其表面存在较多离子交换位的Fe3+和Cu2+物种有关.而当CuO物种较多时会促进氨高温氧化,使催化剂的N2选择性降低、高温窗口变窄.
3.3高温水热条件下Cu的存在可能使Cu、Fe物种更容易发生迁移和团聚,导致Cu-Fe/β(40) 催化剂的水热稳定性变差.
| [1] | BAIKER A, DOLLENMEIER P, GLINSKI M, et al. Selective catalytic reduction of nitric oxide with ammonia:I. monolayer and multilayers of vanadia supported on titania[J]. Applied Catalysis, 1987, 35(2): 351–364. DOI:10.1016/S0166-9834(00)82872-9 |
| [2] | BOSCH H, JANSSEN F. Formation and control of nitrogen oxides[J]. Catalysis Today, 1988(2): 369–379. |
| [3] | BUSCA G, LIETTI L, RAMIS G, et al. Chemical and mechanistic aspects of the selective catalytic reduction of NOx by ammonia over oxide catalysts:A review[J]. Applied Catalysis B:Environmental, 1998, 18: 1–36. DOI:10.1016/S0926-3373(98)00040-X |
| [4] | MUTIN P H, POPA A F, VIOUX A, et al. Nonhydrolyticvanadia-titaniaxerogels:Synthesis, cha-racterization, and behavior in the selective catalytic reduction of NO by NH3[J]. Applied Catalysis B:Environmental, 2006, 69: 49–57. DOI:10.1016/j.apcatb.2006.05.021 |
| [5] | KANG M, YEON T H, PARK E D, et al. Novel MnOx catalysts for NO reduction at low temperature with ammonia[J]. Catalysis Letters, 2006, 106: 77–80. DOI:10.1007/s10562-005-9194-3 |
| [6] | BALLE P, GEIGER B, KURETI S. Selective catalytic reduction of NOx by NH3 on Fe/HBEA zeolite catalysts in oxygen-rich exhaust[J]. Applied Catalysis B:Environmental, 2009, 85: 109–119. DOI:10.1016/j.apcatb.2008.07.001 |
| [7] | DJERAD S, CROCOLL M, KURETI S, et al. Effect of oxygen concentration on the NOx reduction with ammonia over V2 O5-WO3/TiO2 catalyst[J]. Catalysis Today, 2006, 113: 208–214. DOI:10.1016/j.cattod.2005.11.067 |
| [8] | DUNN J P, KOPPULA P R, STENGER H G, et al. Oxidation of sulfur dioxide to sulfur trioxide over supported vanadia catalysts[J]. Applied Catalysis B:Environmental, 1998, 19: 103–117. DOI:10.1016/S0926-3373(98)00060-5 |
| [9] | FENG X, HALL W K. FeZSM-5:A durable SCR catalyst for NOx removal from combustion streams[J]. Journal of Catalysis, 1997, 166: 368–376. DOI:10.1006/jcat.1997.1530 |
| [10] | LONG R Q, YANG R T. Superior Fe-ZSM-5 catalyst for selective catalytic reduction of nitric oxide by ammonia[J]. Journal of the American Chemical Society, 1999, 121: 5595–5596. DOI:10.1021/ja9842262 |
| [11] | LONG R Q, YANG R T. Catalytic Performance of Fe-ZSM-5 catalysts for selective catalytic reduction of nitric oxide by ammonia[J]. Journal of Catalysis, 1999, 188: 332–339. DOI:10.1006/jcat.1999.2674 |
| [12] | SUBBIAH A, CHO B K, BLINT R J, et al. NOx reduction over metal-ion exchanged novel zeolite under lean conditions:Activity and hydrothermal stability[J]. Applied Catalysis B:Environmental, 2003, 42: 155–178. DOI:10.1016/S0926-3373(02)00230-8 |
| [13] | SJÖVALL H, OLSSON L, FRIDELLE, et al. Selective catalytic reduction of NOx with NH3 over Cu-ZSM-5-The effect of changing the gas composition[J]. Applied Catalysis B:Environmental, 2006, 64: 180–188. DOI:10.1016/j.apcatb.2005.12.003 |
| [14] | QI G S, YANG R T. Ultra-active Fe/ZSM-5 catalyst for selective catalytic reduction of nitric oxide with ammonia[J]. Applied Catalysis B:Environmental, 2005, 60: 13–22. DOI:10.1016/j.apcatb.2005.01.012 |
| [15] | JIANG S Y, ZHOU R X. Ce doping effect on performance of the Fe/β catalyst for NOx reduction by NH3[J]. Fuel Process Technol, 2015, 133: 220–226. DOI:10.1016/j.fuproc.2015.02.004 |
| [16] | TWIGG M V. Catalytic control of emissions from cars[J]. Catalysis Today, 2011, 163: 33–41. DOI:10.1016/j.cattod.2010.12.044 |
| [17] | PLÁT F, BÁRTOVÁ S, ŠTĚPÁNEK J, et al. Dynamics of a combined DOC-NSRC-SCR exhaust gas after treatment system with periodic regenerations[J]. Industrial & Engineering Chemistry Research, 2010, 49: 10348–10357. |
| [18] | PEREDA-AYO B, DE LA TORRE U, ILLÁN-GÓMEZ M J, et al. Role of the different copper species on the activity of Cu/zeolite catalysts for SCR of NOx with NH3[J]. Applied Catalysis B:Environmental, 2014, 147: 420–428. DOI:10.1016/j.apcatb.2013.09.010 |
| [19] | ZHANG T, LIU J, WANG D, et al. Selective catalytic reduction of NO with NH3 over HZSM-5-supported Fe-Cu nanocomposite catalysts:The Fe-Cu bimetallic effect[J]. Applied Catalysis B:Environmental, 2014, 148/149: 520–531. DOI:10.1016/j.apcatb.2013.11.006 |
| [20] | FRANCO R M, MOLINER M, CONCEPCION P, et al. Selective catalytic reduction of NO with NH3 over HZSM-5-supported Fe-Cu nanocomposite catalysts:The Fe-Cu bimetallic effect[J]. Journal of Catalysis, 2014, 314: 73–82. DOI:10.1016/j.jcat.2014.03.018 |
| [21] | SULTANA A, SASAKI M, SUZUKI K, et al. Tuning the NOx conversion of Cu-Fe/ZSM-5 catalyst in NH3-SCR[J]. Catalysis Communications, 2013, 41: 21–25. DOI:10.1016/j.catcom.2013.06.028 |
| [22] | MAUVEZIN M, DELAHAY G, COQ B, et al. Identification of iron species in Fe-BEA:Influence of the exchange level[J]. The Journal of Physical Chemistry B, 2001, 105(5): 928–935. DOI:10.1021/jp0021906 |
| [23] | XUE J, WANG X, QI G, et al. Characterization of copper species over Cu/SAPO-34 in selective catalytic reduction of NOx with ammonia:Relationships between active Cu sites and de-NOx performance at low temperature[J]. Journal of Catalysis, 2013, 297: 56–64. DOI:10.1016/j.jcat.2012.09.020 |
| [24] | DE LA TORRE U, PERE-AYO B, GONZÁLEZ-VELASCO J R. Cu-zeolite NH3-SCR catalysts for NOx removal in the combined NSR-SCR technology[J]. Chemical Engineering Journal, 2012, 207/208: 10–17. DOI:10.1016/j.cej.2012.06.092 |
| [25] | SHEN K, ZHANG Y, WANG X, et al. Influence of chromium modification on the properties of MnOx-FeOx catalysts for the low-temperature selective catalytic reduction of NO by NH3[J]. Journal of Energy Chemistry, 2013, 22: 617–623. DOI:10.1016/S2095-4956(13)60081-9 |
| [26] | CHEN B, LIU N, LIU X, et al. Study on the direct decomposition of nitrous oxide over Fe-beta zeolites:From experiment to theory[J]. Catalysis Today, 2011, 175: 245–255. DOI:10.1016/j.cattod.2011.04.010 |
| [27] | WEI G L, YU Z, FANG N G, et al. Catalytic degradation of tobacco-specific nitrosamines by ferric zeolite[J]. Applied Catalysis B:Environmental, 2013, 129: 301–308. DOI:10.1016/j.apcatb.2012.09.039 |
| [28] | PARK J Y, LEE Y J, KHANNA P, et al. Alumina-supported iron oxide nanoparticles as Fischer-Tropsch catalysts:Effect of particle size of iron oxide[J]. Journal of Molecular Catalysis A:Chemical, 2010, 323: 84–90. DOI:10.1016/j.molcata.2010.03.025 |
| [29] | TIPPINS H H. Charge-transfer spectra of transition-metal ions in corundum[J]. Physical Review B, 1970, 1(1): 126–135. DOI:10.1103/PhysRevB.1.126 |
| [30] | LU L, LI L, WANG X, et al. Understanding of the finite size effects on lattice vibrations and electronic transitions of nano α-Fe2O3[J]. The Journal of Physical Chemistry B, 2005, 109: 17151–17156. DOI:10.1021/jp052780+ |
| [31] | JANAS J, GURGUL J, SOCHA R P, et al. Effect of Cu content on the catalytic activity of CuSiBEA zeolite in the SCR of NO by ethanol:Nature of the copper species[J]. Applied Catalysis B:Environmental, 2009, 91(1/2): 217–224. |
| [32] | ISMAGILOV Z R, YASHNIK S A, ANUFRIENKO V F, et al. Linear nanoscale clusters of CuO in Cu-ZSM-5 catalysts[J]. Applied Surface Science, 2004, 226(1/2/3): 88–93. |
| [33] | WANG L, GAUDET J R, LI W, et al. Migration of Cu species in Cu/SAPO-34 during hydrothermal aging[J]. Journal of Catalysis, 2013, 306: 68–77. DOI:10.1016/j.jcat.2013.06.010 |
| [34] | PESTRYAKOV A N, PETRANOVSKⅡ V P, KRYAZHOV A, et al. Study of copper nanoparticles formation on supports of different nature by UV-Vis diffuse reflectance spectroscopy[J]. Chemical Physics Letters, 2004, 385: 173–176. DOI:10.1016/j.cplett.2003.12.077 |
| [35] | YASHNIK S A, ISMAGILOV Z R, ANUFRIENKO V F. Catalytic properties and electronic structure of copper ions in Cu-ZSM-5[J]. Catalysis Today, 2005, 110(3/4): 310–322. |
| [36] | CAMPOS-MARTIN J M, GUERRERO-RUIZ A, FIERRO J L. Changes of copper location in CuY zeolites induced by preparation methods[J]. Catalysis Letters, 1996, 41: 55–61. DOI:10.1007/BF00811713 |
| [37] | WAHLQVIST M, SHCHUKAREW A. XPS spectra and electronic structure of group IA sulfates[J]. Journal of Electron Spectroscopy and Related Phenomena, 2007, 156/157/158: 310–314. |
| [38] | ARAKAWA K, MATSUDA S, KINOSHITA H. SOx poisoning mechanism of NOx selective reduction catalysts[J]. Applied Surface Science, 1997, 121/122: 382–386. DOI:10.1016/S0169-4332(97)00338-3 |
| [39] | MORENO-TOST R, SANTAMARÍA-GONZÁLEZ J, RODRÍGUEZ-CASTELLÓN E, et al. Selective catalytic reduction of nitric oxide by ammonia over Cu-exchanged Cuban natural zeolites[J]. Applied Catalysis B:Environmental, 2004, 50(4): 279–288. DOI:10.1016/j.apcatb.2004.01.019 |
| [40] | ZHANG L, WANG D, LIU Y, et al. SO2 poisoning impact on the NH3-SCR reaction over a commercial Cu-SAPO-34 SCR catalyst[J]. Applied Catalysis B:Environmental, 2014, 37: 156–157. |



