食管癌是一种高发病率与高死亡率的消化道恶性肿瘤疾病。食管癌患者临床表现以食管狭窄为主[1]。食管狭窄主要由食管癌、手术、腐蚀性物质摄入和药物损伤等引起,会导致患者吞咽困难、恶心呕吐等。目前,内镜扩张是缓解吞咽困难的常用治疗方法,但需要反复进行多次手术,增大了患者的手术风险与经济负担[2]。此外,植入金属或塑料食管支架也是缓解吞咽困难的姑息性治疗方案[3]。这2类食管支架虽能在短期内有效扩张食管,但长期使用会引起一些并发症,如食管狭窄复发、支架滑移等[4-5],这无疑会延长患者的治疗过程。为了克服这一困难,学者们研制出了载药食管支架。载药食管支架不仅能够有效抑制组织增生,还展现出了一定的抗肿瘤能力。这类食管支架能够使患者术后食管再狭窄的发生率降低至5%~10%[6]。
现阶段,制备载药食管支架的常用方法是浸涂法与喷涂法,即通过将食管支架浸入药物/聚合物混合溶液或将溶液喷洒在食管支架表面来形成载药膜,以加载抗癌药物[7]。然而,这种制备工艺无法以水凝胶作为药物载体,且存在覆膜精度不高的问题。覆膜精度不高可能会导致患者不同部位的治疗效果不同,有可能会引起食管再次狭窄。此外,相较于其他材料,水凝胶能够促进细胞生长且可自行降解,生物相容性更高。
随着3D打印技术的快速发展,基于3D打印的食管支架制备工艺得到了广泛关注[8]。Yuan等[9]利用3D打印技术制备了不同形态的含褪黑素的水凝胶食管支架,显著缓解了食管炎症,防止了食管狭窄和纤维化。Lin等[10]基于3D打印技术研发了一种新型的聚合物食管支架,该支架可通过调节聚合物的比例来控制力学性能。Fouladian等[11]采用3D打印技术研制了一种负载5-FU(5-fluorouracil,5-氟尿嘧啶)的食管支架,该支架具有良好的力学性能与药物释放能力。上述研究表明,3D打印技术在制备载药食管支架方面具有显著优势。其中,压电喷墨打印技术具有打印速度快及喷射液滴可控的优点,在3D打印领域的应用尤为广泛。Liu等[12]通过对压电喷墨打印的驱动波形进行优化,确定了最佳脉冲宽度,提高了打印的准确性。Yang等[13]通过优化压电喷墨打印驱动波形的串扰,减少了卫星滴的产生,提高了打印的稳定性。由此可知,通过调控压电喷墨打印的驱动波形可改善喷射液滴的性质,从而提高打印精度。
在食管支架载药层的制备材料方面,PTX(paclitaxel,紫杉醇)和5-FU已被证实具有临床有效性,可用于食管癌的治疗[14-15]。GelMA(gelatin methacryloyl,甲基丙烯酰化明胶)是一种增加了光敏官能团的改性明胶。GelMA水凝胶不仅保留了原始明胶的良好生物相容性与降解性,还能在紫外线和光引发剂的作用下交联固化[16]。GelMA水凝胶中的羟基和氨基还提供了结合DNA链、生长因子和药物分子的活性位点,使得其能够用于制备水凝胶伤口敷料[17]。此外,GelMA水凝胶具有温敏性质,其在高于一定温度时呈液态,而在降低至一定温度后会因形成氢键而凝胶化,有利于后续的固化成形。因此,GelMA水凝胶在生物3D打印领域得到了广泛的研究和应用[18]。
基于此,本文拟利用压电喷墨打印技术制备GelMA水凝胶食管支架载药层。首先,基于有限元仿真法构建压电喷墨打印平台温控箱的仿真模型并优化温控参数,以确保载药层的固化成形精度。随后,开展液滴喷射实验,以分析压电喷头驱动波形参数(电压幅值、斜率参数与脉冲宽度)对液滴直径的影响,通过确定两者的关系来优化驱动波形参数,以改善液滴喷射状况,从而提高载药层的覆膜精度。通过制备高精度的水凝胶载药食管支架,实现在治疗食管狭窄的同时促使细胞附着生长,从而促进患者早日康复。
1 压电喷墨打印平台及其工作原理
1.1 压电喷墨打印平台搭建
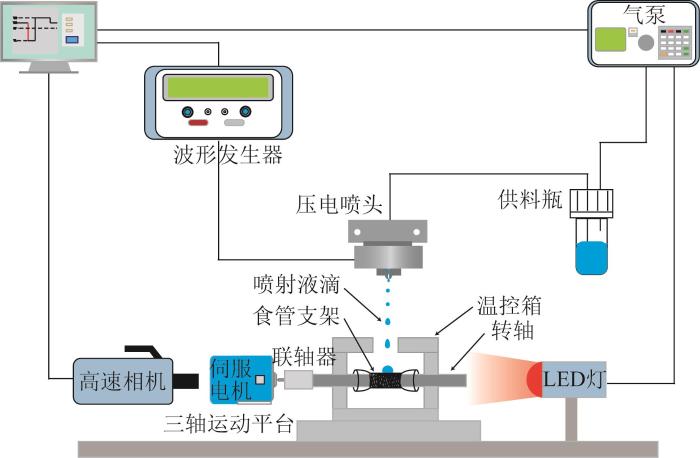
压电喷墨打印平台的结构如图1所示,其由4个模块组成:喷墨打印模块、温控模块、运动控制模块和运动记录模块。喷墨打印模块主要包括波形发生器、气泵、供料瓶和压电喷头(包含储液腔与喷嘴两部分)。其中,压电喷头采用笔者课题组自主研发的高黏度压电式膜片喷头[19]。同时,为了实现单液滴的稳定喷射,笔者团队制造了专用的波形发生器,可调控驱动波形的各项参数。温控模块的核心为温控箱,该温控箱选用导热性较好的铝合金作为箱体材料;在此基础上,添加温控上盖与温控底板,同时对箱体部分进行制冷。制冷技术基于珀尔帖效应,其原理为:当电流流经由不同导体构成的电路时,除了导体中会产生不可逆的焦耳热损耗外,不同导体的连接处还会根据电流方向的不同分别产生吸热、放热现象。据此,选择TEC2-19006半导体制冷片作为制冷源,同时采用水冷散热器作为散热装置,共同组成温控上盖与温控底板。运动控制模块由三轴运动平台、伺服电机、联轴器和转轴组成。其中,三轴运动平台用于保证喷头沿X轴方向的运动;转轴和伺服电机作为承载食管支架的打印平台:将食管支架套在转轴上后,利用伺服电机控制转轴转动,以完成载药层的打印。此外,为了能够更好地优化打印效果,使用由LED(light emitting diode,发光二极管)灯与高速相机组成的运动记录模块来记录整个打印过程,以观察并寻找喷射液滴的变化规律。
图1
图1
压电喷墨打印平台结构示意
Fig.1
Structure diagram of piezoelectric inkjet printing platform
1.2 压电喷头工作原理介绍
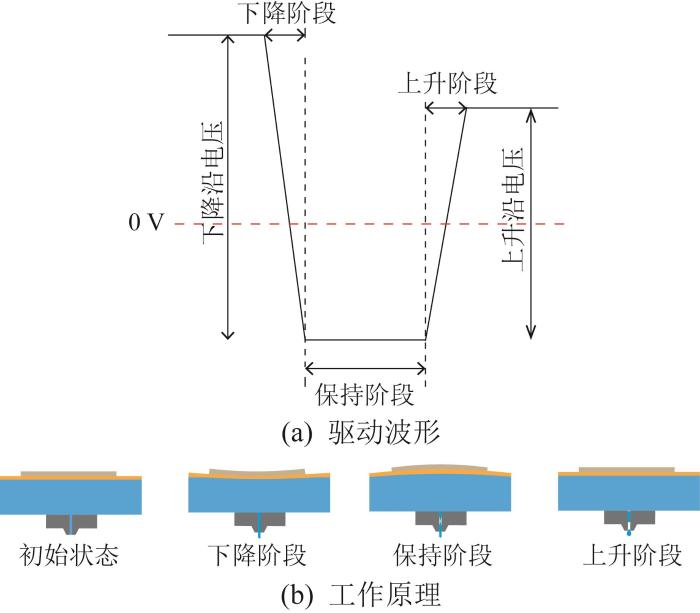
图2(a)所示为一种用于驱动压电喷头的波形。该驱动波形的主要作用是通过电压脉冲信号激励压电陶瓷,使其产生压力波,进而驱动喷头完成液滴喷射。压电喷头的工作原理如图2(b)所示。在驱动波形的作用下,压电陶瓷在电压下降阶段发生向下的轴向形变,导致喷头腔体内压力增大,使得液体被挤出,形成具有一定高度和速度的液柱。随后,当下降沿电压作用结束后,驱动波形进入电压保持阶段。在这一阶段,压电陶瓷逐渐恢复原状,喷头腔体内的压力随之减小,使得部分液体被吸回喷头腔体内,造成液柱收缩现象。接着,驱动波形进入电压上升阶段,此时压电陶瓷在电压作用下产生向上的轴向形变,使得喷头腔体内压力降低。在该状态下,液柱的前半部分在惯性和重力的双重作用下继续向下运动,后半部分因受到压力作用而呈收缩回喷头腔体内的趋势。当收缩达到一定程度时,液柱断裂,前半部分形成液滴。
图2
图2
压电喷头的驱动波形与工作原理
Fig.2
Driving waveform and working principle of piezoelectric inkjet head
2 温控箱的设计与仿真分析
2.1 温控箱设计与仿真建模
由文献[20]可知,质量浓度为5%的GelMA水凝胶在37 ℃的喷头内保持液态,在打印成液滴后需进行降温处理才能从液态转变为凝胶状态。因此,在一定的空间范围内,需要保证空间温度在10 ℃以下。但是,温度过低会使GelMA水凝胶从凝胶状态转变为完全的固态。因此,需将温度控制在合理范围内,以确保材料凝胶化。
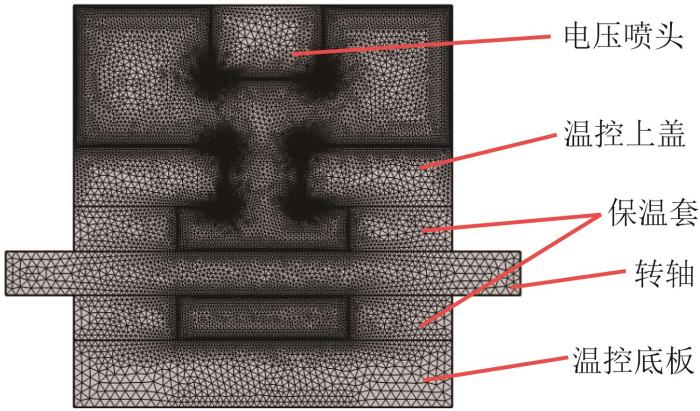
本文利用多物理场仿真软件COMSOL Multiphysics®6.3来模拟温控箱的温控过程。由于仿真涉及固体与流体传热的物理场,且温控箱与压电喷头均可视为轴对称结构,为节约时间成本以及确保仿真准确性,采用二维建模法。温控箱仿真模型简化为五部分:温控上盖、转轴、保温套、温控底板与压电喷头。温控箱仿真模型网格划分结果如图3所示。
图3
图3
温控箱仿真模型网格划分
Fig.3
Grid division of temperature control box simulation model
仿真时采用共轭传热模块,将温控箱设定为静止固体,仅考虑热传导,控制方程如下[21]:
式中:ρ为材料密度,Cp 为材料的比热容,k为热导率,T为温度,Q为材料吸收的热量。
同时,由于存在空气,需要考虑流体传热问题。忽略流体的压缩性与黏性力做功,则静止流体的共轭传热控制方程与固体的相同。
2.2 温控箱仿真分析
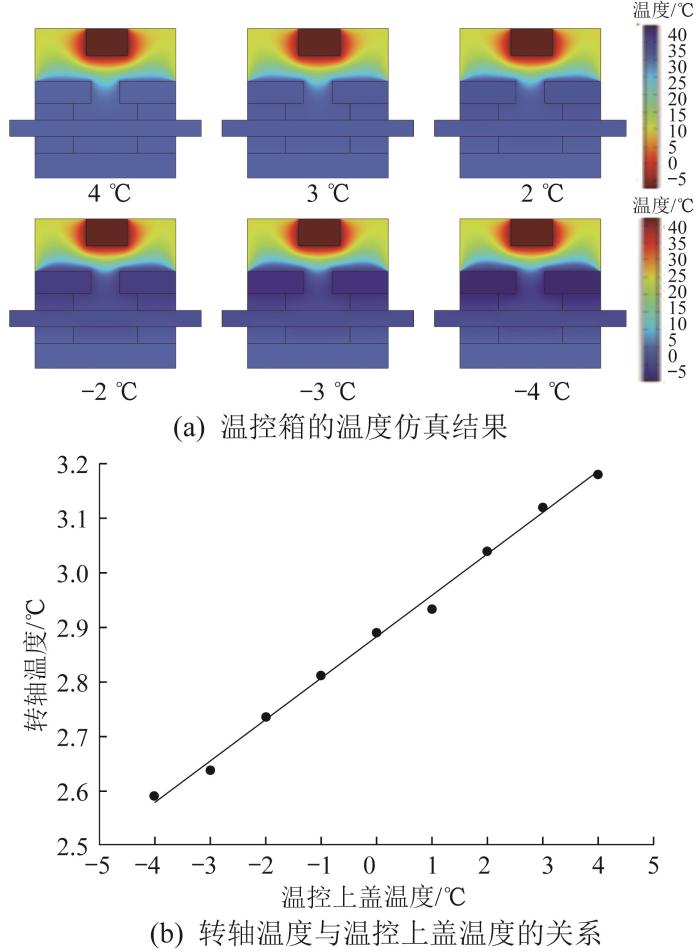
为了确保食管支架载药层的固化成形(即确保转轴温度在10 ℃以下),基于课题组前期所做的温控箱仿真研究[22],对温控参数进行优化。固定温控底板的温度为4 ℃,运用有限元仿真法,探究当温控上盖的温度为-4~4 ℃时搭载食管支架的转轴的温度变化规律。不同温控上盖温度下,温控箱的温度仿真结果如图4(a)所示,转轴温度与温控上盖温度的关系如图4(b)所示。由图4可以看出,随着温控上盖温度的降低,温控箱内部的温度逐渐下降;转轴温度与温控上盖温度呈线性关系:转轴温度随温控上盖温度的升高而升高,且转轴温度稳定在2.5~3.2 ℃范围内。由此可知,当温控底板的温度固定为4 ℃时,温控上盖的温度保持在-4~4 ℃范围内即可保证GelMA水凝胶的固化成形。
图4
图4
不同温控上盖温度下温控箱及转轴的温度变化规律
Fig.4
Temperature variation law of temperature control box and rotating shaft under different temperatures of temperature control cover
3 驱动波形对压电喷墨打印的影响分析
在制造压电喷墨打印机时,压电喷头的尺寸参数和结构等均是固定的,且在喷射过程中无法改变打印材料。因此,驱动波形的各项参数决定了喷射液滴的直径与速度。鉴于本文的研究目的是通过调控驱动波形来控制液滴直径,进而提高食管支架载药层的打印精度,本节只考虑液滴直径的变化。采取控制变量法,通过实验测试不同驱动波形参数(电压幅值、斜率参数及脉冲宽度)对液滴直径的影响。经过预实验的验证,驱动波形的频率固定为2 Hz。利用高速相机记录不同驱动波形参数下的液滴喷射过程(不喷射液滴或存在卫星滴时不记录),每个参数记录4组数据,测量液滴直径并绘制对应的图像。
3.1 电压幅值对液滴直径的影响
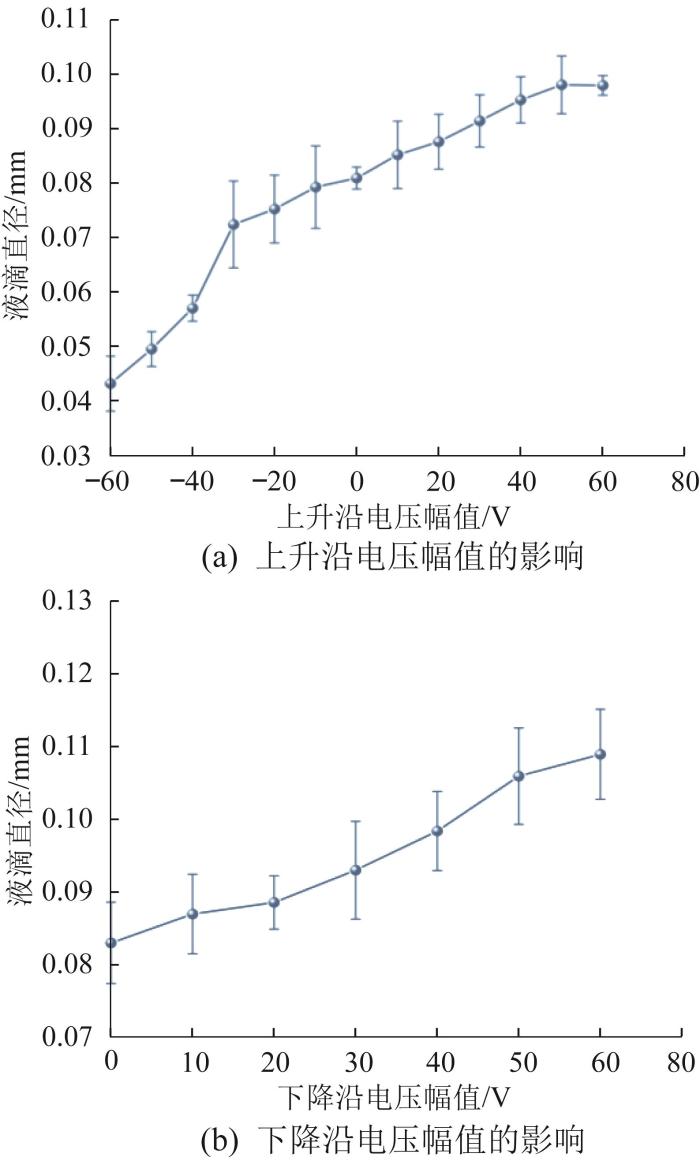
驱动波形的电压幅值直接决定了压电陶瓷在喷墨打印过程中所获得的能量。当电压处于上升阶段时,压电陶瓷发生轴向形变,随着电压幅值的增大,压电陶瓷的形变量与喷头腔体内气压均发生变化,最终影响所喷射的液滴体积。因此,当对压电陶瓷施加的电压下降时,压电陶瓷处于向下弯曲状态,喷嘴处液面形成向外凸出的弯月面;当对压电陶瓷施加的电压上升时,情况相反。这2种情况对应了驱动波形的下降沿和上升沿。由此可知,上升沿电压和下降沿电压对液滴状态的影响不同。为了研究驱动波形的电压幅值对液滴形成过程的影响,分别针对上升沿电压幅值和下降沿电压幅值开展实验研究。设定电压幅值变化范围为-60~60 V,每间隔10 V改变一次电压幅值,观察液滴直径的变化情况。驱动波形电压幅值对液滴直径的影响如图5所示。
图5
图5
驱动波形电压幅值对液滴直径的影响
Fig.5
Influence of driving waveform voltage amplitude on droplet diameter
3.2 斜率参数对液滴直径的影响
驱动波形的斜率参数影响驱动波形电压上升阶段与电压下降阶段的持续时间,因此将其分为上升沿斜率与下降沿斜率两部分。上升沿斜率影响电压上升阶段,在电压升高的过程中,压电陶瓷向上的轴向形变量逐渐增大,喷头腔体内的体积变大,压强降低,使得腔体内压强小于大气压,进而产生负压。液体在负压的影响下被吸回喷头腔体内,此时喷嘴处的液面逐渐呈凹陷的状态。而下降沿斜率的影响则相反,在电压下降的过程中,压电陶瓷产生的形变使喷头腔体内压强增大,导致液体顺着喷嘴向下喷出,喷嘴处液面逐渐呈凸出的状态。为了探究驱动电压的上升沿斜率与下降沿斜率对液滴直径的影响,分别将2个斜率的变化范围设为1~10 V/ms,每间隔1 V/ms改变一次斜率,并观察液滴直径的变化情况。驱动波形斜率参数对液滴直径的影响如图6所示。
图6
图6
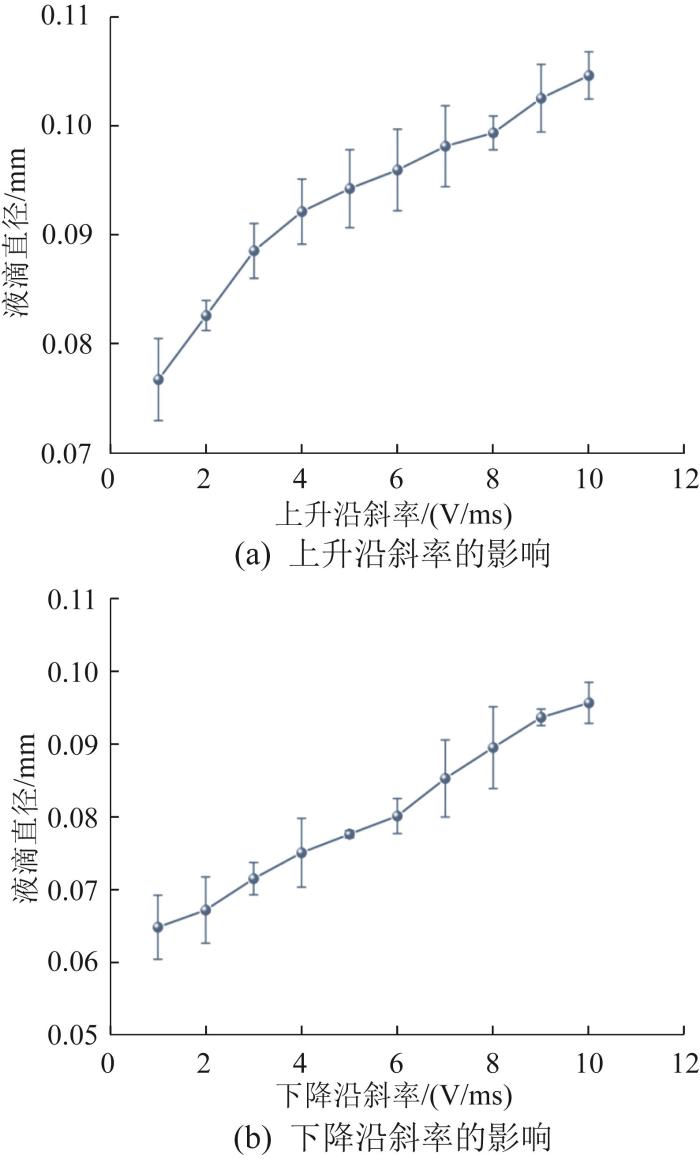
驱动波形斜率参数对液滴直径的影响
Fig.6
Influence of driving waveform slope parameter on droplet diameter
从图6(a)中可以看出,随着驱动波形上升沿斜率的增大,液滴直径增大。这可归因于驱动波形电压上升阶段持续时间的缩短。在电压幅值保持恒定的情况下,压电陶瓷的振幅维持不变,但电压上升阶段持续时间的缩短使得压电陶瓷形变速率加快,从而加速了喷嘴处压力的动态变化。这种压力变化使得喷头在相同时间内能够挤出更多的液体,进而导致所形成液柱的体积增大,则液滴直径随之增大。由图6(b)可知,随着驱动波形下降沿斜率的增大,液滴直径增大。这同样是因为当下降沿斜率增大时,电压下降阶段的持续时间缩短,导致喷头腔体内负压的变化率增大,使得腔体在相同时间内补充的液体增多,则喷射液滴的直径增大。由此可知,不同的上升沿斜率与下降沿斜率下均能实现液滴的正常、稳定喷射。因此,在保证液滴直径不会过大的情况下,调节驱动波形的上升沿、下降沿斜率均能保证稳定喷射。
3.3 脉冲宽度对液滴直径的影响
驱动波形的脉冲宽度是指波形的保持时间,其决定了喷嘴处所形成液柱的长短。由上文分析可知,当驱动波形处于电压下降阶段时,喷嘴处液面呈凸出状态,而在电压保持阶段,喷嘴处液面逐渐形成液柱,故保持时间越长,喷嘴处所形成的液柱就越长。但是,脉冲宽度不能过短,过短的脉冲宽度下喷嘴处所形成的液柱不足以支撑喷嘴形成液滴。而过长的脉冲宽度会导致所形成的液柱过长,当驱动波形处于电压上升阶段时,液柱前半部分的惯性过大,气压差不足以将足够的液体吸回喷头腔体内,进而形成卫星滴,影响打印效果与打印精度。
基于波传导理论的分析,在电压保持阶段,由电压下降阶段产生的正压力波会在封闭的喷头腔体内传播并反射。这些正压力波会与后续电压上升阶段所产生的负压力波相互叠加或抵消,这一相互作用是由脉冲宽度直接决定的。为了确定合理的脉冲宽度,探究其与液滴直径的关系。将脉冲宽度的变化范围设为0.5~3.0 ms,每间隔0.5 ms改变一次脉冲宽度并观察液滴直径的变化情况。脉冲宽度对液滴直径的影响如图7所示。
图7
图7
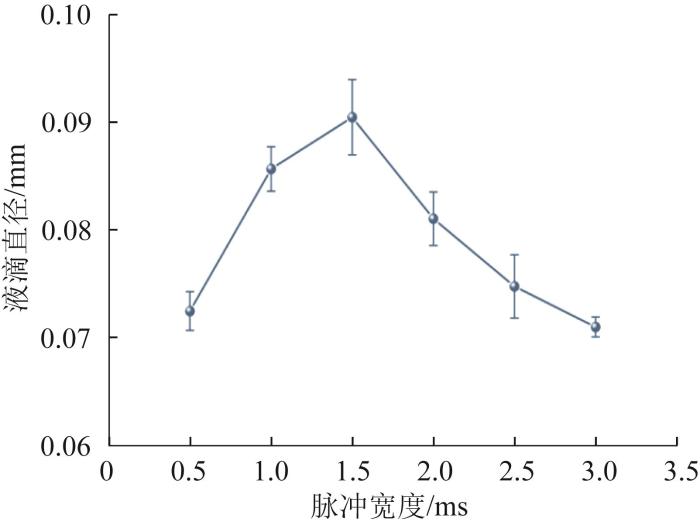
驱动波形脉冲宽度对液滴直径的影响
Fig.7
Influence of driving waveform pulse width on droplet diameter
从图7中可以观察到,液滴直径与驱动波形脉冲宽度之间存在近似抛物线的关系。具体而言,随着脉冲宽度的增大,液滴直径先呈增大趋势,直至脉冲宽度达到1.5 ms,随后液滴直径随脉冲宽度的增大而逐渐减小。出现这一现象的主要原因是:当脉冲宽度过大或过小时,电压上升和下降阶段产生的压力波在喷嘴处会相互抵消,导致传播至喷嘴处的压力波减小,最终影响喷嘴所喷射的液滴大小。当脉冲宽度达到1.5 ms时,所产生的正压力波与后续负压力波所反射的压力波产生了叠加作用,故形成了直径最大的液滴。因此,驱动波形的脉冲宽度可设为1.5 ms。
4 食管支架载药层打印实验
为了验证温控箱仿真设计与驱动波形优化的准确性与有效性,以GelMA水凝胶为打印材料,5-FU为药物,在压电喷墨打印平台上开展食管支架载药层打印实验。温控上盖的温度设为-4 ℃,温控底板的温度设为4 ℃;驱动波形参数设置如下:上升沿电压幅值为30 V,上升沿斜率与下降沿斜率均为7 V/ms,脉冲宽度为1.5 ms。对食管支架载药层3D模型进行切片并导出G代码,初步设定载药层3D模型的切片数为20层。
图8
图8
食管支架载药层打印结果
Fig.8
Printing results of drug-carrying layer of esophageal stent
5 结 论
本文搭建了压电喷墨打印平台并系统地研究了其工作原理。通过添加温控模块优化了打印平台,并运用有限元仿真法优化了温控箱的温控参数,为GelMA水凝胶的固化提供了合适的温度条件。同时,开展了驱动波形电压幅值、斜率参数和脉冲宽度对液滴直径影响的实验研究,发现液滴直径与电压幅值和斜率参数均呈正相关,而当脉冲宽度为1.5 ms时,液滴直径出现最大值;在此基础上,对压电喷头的驱动波形参数进行了优化。最后,开展了食管支架载药层打印实验,验证了温控箱仿真设计与驱动波形优化的准确性与有效性。所提出的方法可为载药食管支架的快速、定制化制备提供新思路,从而促使患者能够尽早康复。
参考文献
食管支架在治疗良性、恶性食管狭窄的研究进展
[J].
Research progress of esophageal stent in the treatment of benign and malignant esophageal stenosis
[J].
How to approach a patient with refractory or recurrent benign esophageal stricture
[J].
Preventing stricture formation by covered esophageal stent placement after endoscopic submucosal dissection for early esophageal cancer
[J].
Risk factors of stent migration in esophageal cancer patients who underwent fully-covered self-expanding metal stents for malignant dysphagia or tracheoesophageal fistula
[J/OL].
TGF-β1 inhibitor P144 protects against benign restenosis after esophageal stenting through TGF-β1/Smads signaling pathway inhibition
[J].
Coronary drug-eluting stents: from design optimization to newer strategies
[J].
A PTX/nitinol stent combination with temperature-responsive phase-change 1-hexadecanol for magnetocaloric drug delivery: magnetocaloric drug release and esophagus tissue penetration
[J].
Futuristic developments and applications in endoluminal stenting
[J].
3D printing of melatonin-loaded esophageal stents for treatment of corrosive esophagitis
[J].
3D-printed flexible polymer stents for potential applications in inoperable esophageal malignancies
[J].
Three-dimensional printed 5-fluorouracil eluting polyurethane stents for the treatment of oesophageal cancers
[J].
Optimization of driven waveform of piezoelectric printhead for 3D sand-printing
[J].
Actuation waveform optimization via multi-pulse crosstalk modulation for stable ultra-high frequency piezoelectric drop-on-demand printing
[J].
The effect of paclitaxel-eluting covered metal stents versus covered metal stents in a rabbit esophageal squamous carcinoma model
[J].
Paclitaxel or 5-fluorouracil/esophageal stent combinations as a novel approach for the treatment of esophageal cancer
[J].
Fiber reinforced GelMA hydrogel to induce the regeneration of corneal stroma
[J].
Engineering the viscoelasticity of gelatin methacryloyl (GelMA) hydrogels via small “dynamic bridges” to regulate BMSC behaviors for osteochondral regeneration
[J].
Recent advances in 3D printing of biomaterials
[J].
高黏度压电式膜片喷头仿真分析与实验研究
[J].
Simulation analysis and experimental study of piezoelectric diaphragm nozzle with high viscosity
[J].DOI:10.13250/j.cnki.wndz.2023.06.017 [本文引用: 1]
Multi-physical field control piezoelectric inkjet bioprinting for 3D tissue-like structure manufacturing
[J].
Modelling analysis of pyrolysis process with thermal effects by using COMSOL Multiphysics
[J].