动态血压(ambulatory blood pressure, ABP)可以用于高血压的识别、诊断和心脑血管并发症风险的评估, 是高血压管理不可或缺的检测指标[1-2].由于动态血压监测仪需要接触人体才能实现血压采集, 在重复测量或者晚间睡眠的情况下会引起患者的不适和抵抗心理, 为动态血压监测带来一定的局限性[3].本文提供一种非接触、非介入式的动态血压获取手段, 对于动态血压监测的普及具有重要的意义.
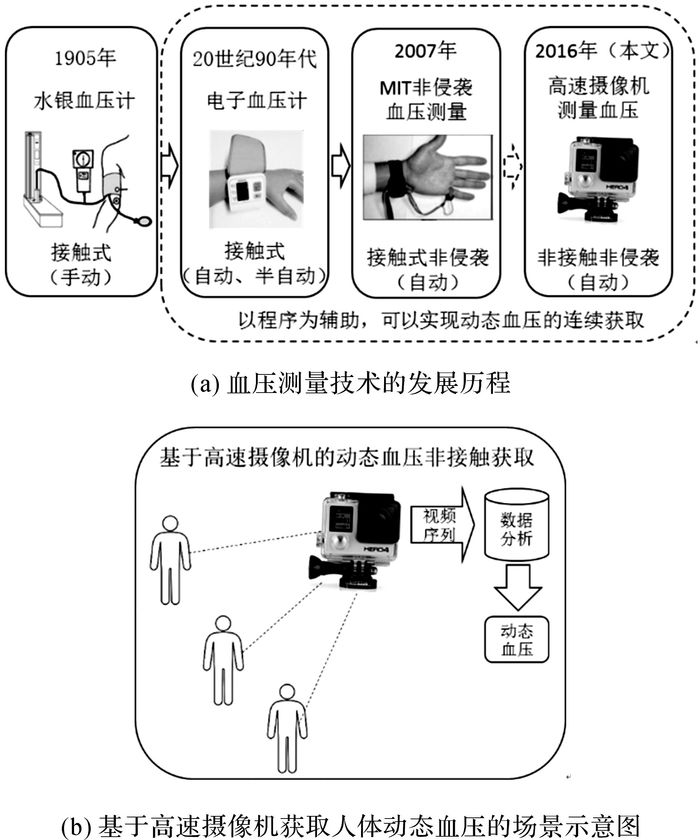
1 血压测量设备的发展历程非接触、非介入式的人体信息测量技术逐渐取代了传统的接触式测量技术.非接触是指无需接触人体, 非介入式(非侵袭)是指在测量过程中不会对人体造成疼痛、痛苦和压迫感等不适[4].血压测量仪器的发展, 经历了从接触式的水银血压计和电子血压计, 到美国麻省理工学院的基于脉搏波速度法的可穿戴式血压计, 如图 1(a)所示.水银血压计和电子血压计在测量过程中, 需要血压计袖带进行充气和放气, 会对人体产生较高强度的压迫感, 造成一定程度的不适[5-6].美国麻省理工学院的可穿戴式血压计与常规血压计袖带不同, 测量过程中无需充放气, 因此不会对人体产生压迫感, 具有非介入式的特点[7].水银血压计在测量血压时, 需要人为地判断血压;电子血压计和可穿戴式血压计可以自动获取血压, 在程序的辅助下, 可以用于血压的连续采集.上述血压计在连续获取血压时, 均要求患者连续佩戴血压计, 会对患者的日常生活产生不便.血压测量仪器在经历了由接触式、侵袭式测量至接触式、非介入式测量的演变过程后, 具有向非接触式、非介入式测量演变的趋势.实现一种非接触、非介入式的血压连续测量方法, 对于动态血压的监测具有重要的意义.
|
图 1 血压测量的发展历程和基于高速摄像机的动态血压获取的场景示意图 Fig. 1 History of blood pressure measurements and illustration of ambulatory blood pressure acquisition scene based on high speed camera |
基于高速摄像机的非接触连续获取人体动态血压的场景示意图, 如图 1(b)所示.基于高速摄像机的动态血压非接触获取技术与现有的血压测量手段相比, 具有非介入式、非接触、非约束、采样周期短和多个人体同步获取的优势.由于基于高速摄像机的动态血压非接触获取技术无需接触人体, 即可实现血压采集, 因此与现有的动态血压获取手段相比, 更适合用于实现对动态人体的血压采集.此外, 基于高速摄像机的动态血压非接触获取技术是通过视频采集实现对动态血压的获取, 因此, 对于同一架高速摄像机, 可以同时对多个人体进行视频采集, 从而实现同一时间获取多个人体的动态血压.
2 2基于高速摄像机非接触获取动态血压的原理和关键技术结合血压与脉搏信号相位差、心率之间的函数关系以及基于成像式光电容积描记技术(imaging photoplethysmographic, IPPG)的脉搏信号相位差和心率的非接触获取技术, 实现了一种非接触、非介入式的动态血压获取手段.该动态血压获取手段只需一台高速摄像机, 即可完成动态血压的获取.由于摄像机不需要接触人体即可获得人体的动态血压信息, 不会因为长期监测或者晚间监测而引起人体不适, 从而为动态血压监测提供了一种非接触、非介入式、实时、非约束的动态血压监测手段.
2.1 血压与脉搏信号相位差、心率的函数关系脉搏信号相位差与血压之间存在正相关性, 可以用于实现血压的无创测量[8].基于文献[8]的实验结果, 从理论方面对脉搏信号相位差和血压之间的相关性进行理论推导.
由于脉搏传导时间(pulse wave transfer time, PWTT)与血压(blood pressure, BP)之间满足关系[9]:
| $\text{BP}=a+b\times \text{PWTT}.$ | (1) |
式中:a和b与人体的血管壁弹性有关, 对于同一个体在短时间内不会发生太大的改变[9].由于脉搏传导时间的计算是将心电图(electrocardiogram, ECG)的R波的峰值作为脉搏传导时间测量的起始点, 光电容积脉搏波(photoplethysmographic, PPG)的峰值点作为测量的终止点[10], 人体上两个固定点P1和P2的脉搏传导时间PWTT1、PWTT2的差值ΔPWTT应满足以下关系:
| $\Delta \text{PWTT}=c\times \text{PWT}{{\text{T}}_{2}}.$ | (2) |
由式(1)、(2) 可得, 人体血压和与两个固定点之间的脉搏传导时间的差值满足关系:
| $\text{BP}=a+b\times \Delta \text{PWTT},$ | (3) |
| $k=b/c.$ | (4) |
由于两点之间的脉搏信号相位差Δφ与脉搏传导时间之差ΔPWTT之间满足:
| $\Delta \text{PWTT}=\frac{1}{\text{HR}}\times \frac{\Delta \varphi }{360}.$ | (5) |
式中:HR为该个体当前时刻的心率, 同一时刻同一个体上的不同部位所获得的心率相同.将式(5) 代入式(3), 得到血压与两固定点的脉搏信号相位差之间满足关系:
| $\text{BP}=a+\frac{k}{\text{HR}}\times \frac{\Delta \varphi }{360}.$ | (6) |
式中:待定系数a和k、HR以及Δφ为未知数.其中, HR和Δφ可以通过高速摄像机进行非接触实时获取.将ΔPWTT视为变量x, 可以将式(6) 转换为一次函数:
| $\text{BP}=a+kx.$ | (7) |
a和k与人体的血管壁弹性有关, 对于同一个体在短时间内相对保持不变.通过智能电子血压仪采集多组血压BP、实时获取的心率HR以及相位差Δφ获得相应的变量x, 对曲线进行拟合可以获得待定系数a和k.
2.2 基于IPPG技术的脉搏信号相位差和心率的非接触获取光电容积描记技术(photoplethysmographic, PPG)是于1930年提出的, 利用光的反射和传播非侵入测量微血管组织中随心脏循环周期振动的脉搏信号的光技术[11-14].由于PPG技术需要PPG传感器直接接触人体的皮肤来获取人体的脉搏信号, 会引起测量结果的变化, 限制了PPG技术的应用范围[12, 15-16].IPPG技术的提出弥补了PPG技术无法采集肌肤存在损伤, 获取动态人体的生理参数的缺陷.目前, IPPG技术已经成功地用于与人体心血管相关的生理参数的获取, 包括人体的心率、呼吸率和血氧饱和度的获取[17-21].
由于高速摄像机可以获取人体动态、多点的视频序列, 采用高速摄像机作为获取人体血压的设备.基于高速摄像机获得的视频序列, 采用IPPG技术对人体不同部位的脉搏信号进行提取, 获得不同部位之间的脉搏信号的相位差和人体当前时刻的心率.
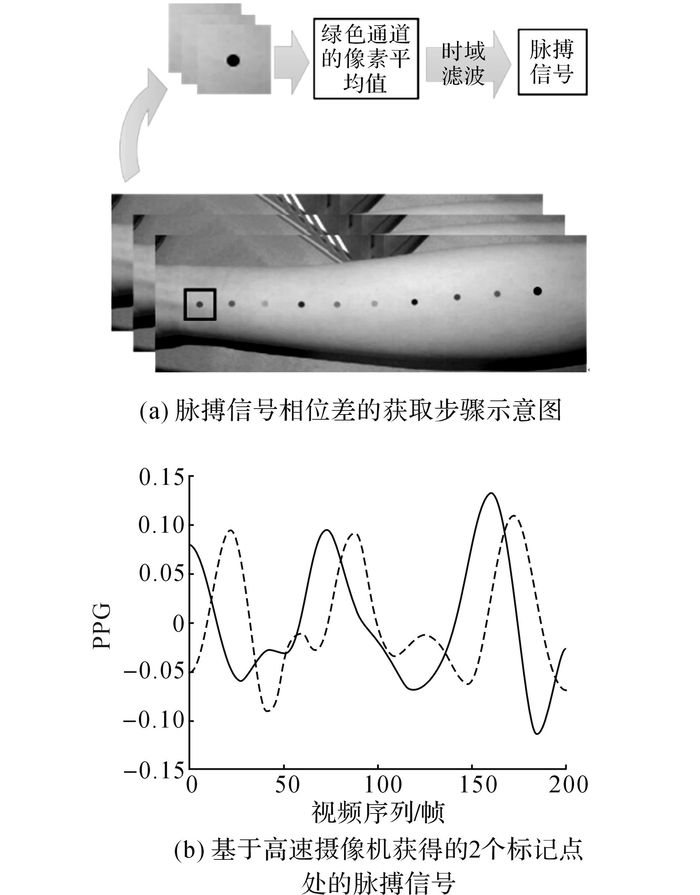
2.2.1 脉搏信号相位差的非接触获取为了获取脉搏信号的相位差, 需要获取人体不同部位的脉搏信号.由于人体胳膊相对易于采集, 选取人体的胳膊作为脉搏信号获取的对象.获取脉搏信号相位差的具体步骤如图 2(a)所示.
|
图 2 基于视频序列的脉搏信号相位差的获取 Fig. 2 Acquisition of phase difference of pulse wave based on videos |
1) 在胳膊上以2 cm为间距, 标记10个点, 采用高速摄像机录制包含人体胳膊的视频序列.对录制所得的视频序列, 以标记点为中心, 分别截取10个标记点处的视频序列.
2) 对每一个标记点的视频序列作以下处理:对视频序列的每一帧图像分离出绿色通道, 对每一帧图像的绿色通道的像素求平均值;采用巴特沃兹滤波器对视频序列的绿色通道的平均值组成的信号进行时域滤波.由于人体的脉搏信号的频率为0.4~6.0 Hz, 将巴特沃兹滤波器的滤波参数设置为0.4~6.0 Hz.经过上述处理, 得到同一段时间的不同标记点处的脉搏信号, 如图 2(b)所示.图中,PPG为脉搏信号幅值.
3) 为了减小误差, 对脉搏信号的相位差进行多点采集、取平均值的处理.以第一个标记点作为起始点, 采用相关性分析, 依次求取间距为10 cm的2个标记点的脉搏信号之间的相位差, 如图 2(b)所示, 2个脉搏信号之间的相位差为73.46°.对于每一段视频序列, 都可以获取5个相位差, 对这5个相位差取平均值, 获得该段视频序列所对应的人体上的间距为10 cm的两点之间的脉搏信号相位差.
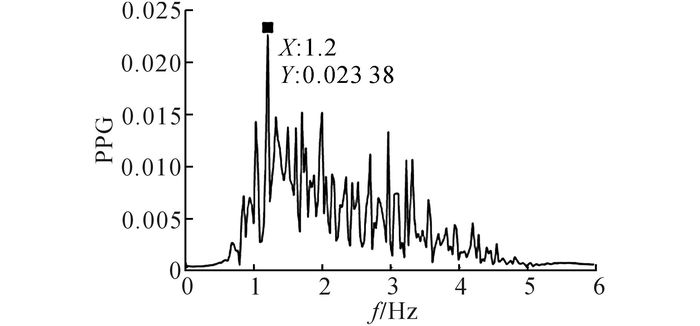
2.2.2 心率的非接触获取对脉搏信号相位差的非接触获取的步骤2) 中获得的标记点处的脉搏信号进行傅里叶变换, 得到脉搏信号的频谱图, 如图 3所示.由于人体的心率为0.7~3.0 Hz, 在经傅里叶变换后所获得的频谱图中的0.7~3.0 Hz下的幅值峰值所对应的频率为当前录制周期所对应的人体的心率.图 3中, 在0.7~3.0 Hz下的幅值峰值所对应的频率为1.2 Hz, 故该标记点处所获得的人体的心率为1.2 Hz.对10个标记点处所获得的心率取平均值, 将所得的平均值作为当前录制周期人体的心率.
|
图 3 脉搏信号的频谱图 Fig. 3 Spectrogram of pulse wave |
血压与脉搏信号相位差、心率之间的函数关系为理论基础, 为了实现基于高速摄像机的动态血压的非接触获取, 首先需要通过曲线拟合获得函数中的未知参数a和k.a和k与人体的血管壁弹性相关, 对于同一个体, a和k在短时间内相对保持不变.为了使a和k相对保持不变, 减少实验过程中的干扰, 针对同一个体进行实验.该实验个体为24岁成年女性, 身体状况健康, 在正常情况下, 该个体的收缩压为128 mmHg, 舒张压为71 mmHg.
通过数据采集和曲线拟合, 获取参数a和k.
数据采集:在人体的右臂以10 cm为间距绘制5组标记点, 每相邻标记点之间的间距为2 cm, 采用GoPro高速摄像机连续录制1 800 s的包含10个标记点的视频序列.在人体的左臂, 采用欧姆龙电子血压仪连续采集人体的舒张压和收缩压, 实测场景示意图如图 4所示.

|
图 4 人体舒张压和收缩压实测场景示意图 Fig. 4 Scene of measurement of systolic and diastolic blood pressure |
曲线拟合:以90 s为周期, 将1 800 s的长视频截取为20段短视频.针对每一段短视频, 提取脉搏信号相位差和心率.依据式(5) 得到当前周期的变量x.对当前周期内的采用欧姆龙电子血压仪测得的舒张压和收缩压, 分别取平均值作为当前周期的变量y.采用一次函数进行曲线拟合得到舒张压pd和收缩压ps, 分别与人体的脉搏信号的相位差和心率之间满足函数关系:
| $\begin{align} &{{p}_{\text{s}}}=408.71x+69.334, \\ &{{p}_{\text{d}}}=89.112x+59.381. \\ \end{align}$ |
采集19段以90 s为周期的包含人体胳膊信息的视频序列, 通过欧姆龙智能电子血压仪获取对应时刻的收缩压p′s和舒张压p′d.对每一段视频序列, 采用基于IPPG技术的脉搏信号相位差和心率的非接触获取技术, 得到当前视频序列的脉搏信号的相位差和心率.将所得的相位差和心率代入拟合所得的函数, 计算人体的收缩压ps和舒张压pd.
将计算所得的ps和pd与欧姆龙智能电子血压仪检测所得的p′s和p′d进行比较, 计算两者的误差.误差的计算公式如下:
| $\begin{align} &{{e}_{{{p}_{\text{s}}}}}=\frac{{{p}_{\text{s}}}-p_{\text{s}}^{'}}{{{p}_{\text{s}}}}\times 100\%, \\ &{{e}_{{{p}_{\text{d}}}}}=\frac{{{p}_{\text{d}}}-p_{\text{d}}^{'}}{{{p}_{\text{d}}}}\times 100\%. \\ \end{align}$ |
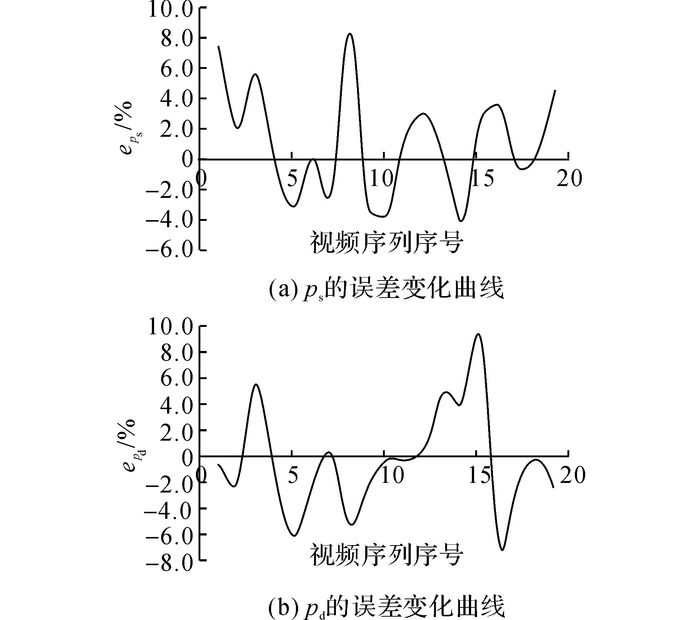
通过计算所得的ps和pd的误差变化曲线分别如图 5(a)、(b)所示.从图 5(a)可以看出, 通过高速摄像机所获得的ps相对于欧姆龙智能电子血压仪所获得的p′s的误差为-4.03%~8.44%.从图 5(b)可以看出, 通过高速摄像机所获得的pd相对于欧姆龙智能电子血压仪所获得的p′d的误差为-6.58%~8.90%.
|
图 5 收缩压和舒张压的误差变化曲线 Fig. 5 Error curves of systolic and diastolic blood pressure |
通过高速摄像机所获得的血压相对于基于欧姆龙智能电子血压仪所获得的血压的误差为±10%.误差的主要来源在于以下2个方面:1) 在通过视频序列获取脉搏信号的过程中, 外界光线干扰会导致所获得的脉搏信号的变化, 从而引起所获得的脉搏信号相位差和心率的变化, 这一因素对与曲线拟合所获得的参数值和血压的获取都会产生影响;2) 通过拟合所得的脉搏信号相位差和心率与血压之间的函数关系的参数值与人体的血管壁弹性相关, 人体的血管壁弹性与人体的生理状态相关, 不同个体在不同生理状态下的拟合所得的参数不同, 这一因素会对与曲线拟合所获得的参数值产生影响, 从而对血压的获取产生影响, 导致误差的产生.
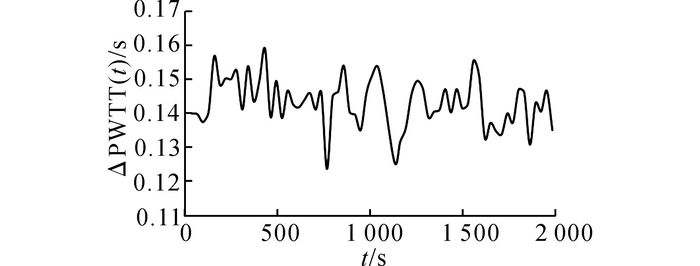
3.3 非接触获取动态血压的实现基于拟合所得的脉搏信号相位差和心率与血压之间的函数关系, 结合基于IPPG技术的脉搏信号相位差和心率的非接触获取, 实现基于高速摄像机的动态血压获取.通过高速摄像机对同一个体的连续录制时长1 950 s的视频序列, 并通过欧姆龙电子血压仪记录了录制过程中人体的血压.基于录制所得的视频序列, 以30 s为周期提取脉搏信号相位差和心率, 通过式(5) 可得脉搏信号传导时间差PWTT(t)随时间的连续变化曲线, 如图 6所示.
|
图 6 脉搏信号传导时间差随时间的连续变化曲线 Fig. 6 Curve of pulse wave transit time difference varies with time |
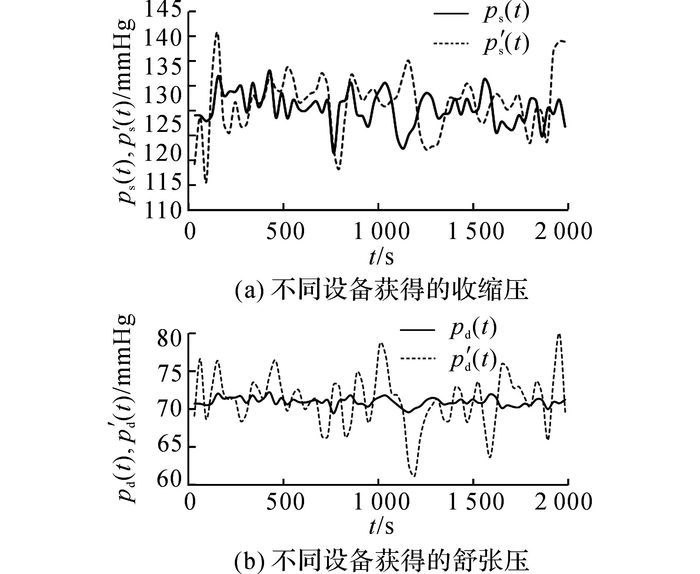
基于上述拟合所得的关系, 通过所获得的脉搏信号相位差和心率得到的ps(t)随时间连续变化的曲线, 分别如图 7(a)的实线所示, pd(t)随时间连续变化的曲线如图 7(b)的实线所示.欧姆龙电子血压仪测量一次血压的周期约为45 s, 通过重采样将周期变为30 s, 得到基于欧姆龙电子血压仪获得的p′s(t)随时间连续变化的曲线如图 7(a)的虚线所示, p′d(t)随时间连续变化的曲线如图 7(b)的虚线所示.
|
图 7 不同设备获得的收缩压和舒张压随时间连续变化的曲线 Fig. 7 Acquired curves of systolic blood pressure and diastolic blood pressure varies with time through different devices |
基于高速摄像机获得的ps(t)和pd(t)以及通过欧姆龙智能电子血压仪获取的p′s(t)和p′d(t)的统计特性如表 1所示.可以看出, 基于高速摄像机所获得的血压的平均值近似等于通过欧姆龙智能电子血压仪获取的血压的平均值, 但标准差和方差低于欧姆龙智能电子血压仪获取的血压的标准差和方差.
| 表 1 不同设备获得的收缩压、舒张压数据的统计特性 Table 1 Statistical properties of acquired systolic blood pressure and diastolic blood pressure through different devices |
对基于高速摄像机获得的ps(t)和基于欧姆龙智能电子血压仪所获得的p′s(t)进行相关性分析发现:当t<1 080 s时, 通过高速摄像机获得的血压与欧姆龙智能电子血压仪获得的血压之间的相关系数为0.35;当t>1 080 s时, 通过高速摄像机获得的收缩压与欧姆龙智能电子血压仪获得的收缩压之间的相关系数为-0.36.相关系数的正负变化由t=1 080 s时引入的相位差引起.相关系数的绝对值大于0.3, 说明基于高速摄像头非接触获得的人体动态血压和基于欧姆龙智能电子血压仪获得的血压实相关.
对基于高速摄像机获得的pd(t)和基于欧姆龙智能电子血压仪获得的p′d(t)进行相关性分析发现:通过高速摄像机获得的舒张压与欧姆龙智能电子血压仪获得的舒张压之间的相关系数仅为0.18.从表 1可以看出, 欧姆龙智能电子血压仪获得的舒张压的方差高于高速摄像机获得的舒张压的方差, 说明前者的波动程度高于后者.影响舒张压波动的因素包括心率和外周阻力[22].欧姆龙智能电子血压仪在测量血压时需要充放气, 会引起外周阻力的变化, 导致舒张压的波动程度较大.高速摄像机在获取血压时无需接触人体, 不会引起外周阻力的变化, 避免了充、放气阶段的压力产生的干扰, 因此波动程度相对较低.
综上, 可以看出, 基于高速摄像机获得的动态血压具有以下特点:1) 与基于欧姆龙智能电子血压仪所获得的动态血压具有明显的相关性;2) 相对于欧姆龙智能电子血压仪, 避免了测量血压时充、放气阶段的压力带来的干扰;3) 相对于欧姆龙智能电子血压仪, 在同一段时间内, 基于高速摄像机所获得的血压数据更丰富, 包含更多的血压变化信息.
4 结语基于高速摄像机的动态血压非接触获取为动态血压监测提供了一种非接触、非介入式的测量手段, 对于动态血压监测的普及具有重要意义.与传统的动态血压监测仪相比, 基于高速摄像机的动态血压非接触获取无需接触人体, 不会对人体造成不适, 避免了传统血压测量手段在充、放气阶段产生的压力所引入的干扰, 具有更广泛的应用范围和更舒适的血压监测体验.由于基于高速摄像机的动态血压获取无需接触人体, 从而可以用于存在肌肤损伤的人体以及夜间的动态血压的连续获取, 也可以结合目标跟踪技术实现对动态人体的动态血压获取.通过高速摄像机非接触获取人体的动态血压是基于随时间同步变化的视频序列, 因此基于高速摄像机的动态血压非接触获取技术可以实现多个人体的动态血压同步获取.此外, 通过合理的设置采样周期可以获得更丰富的血压变化信息, 为心血管疾病的预防、诊疗和预后提供更有效的数据.
| [1] |
王继光. 24 h动态血压监测:适用人群及临床意义[J].
中华高血压杂志, 2014, 22(7): 614–615.
WANG Ji-guang. Twenty-four-hour ambulatory blood pressure monitoring:applicable crowd and its clinical significance[J]. Chinese Journal of Hypertension, 2014, 22(7): 614–615. |
| [2] | O'BRIEN E, PARATI G, STERGIOU G, et al. European society of hypertension position paper on ambulatory blood pressure monitoring[J]. Journal of Hypertension, 2013, 31(9): 1731–1768. DOI:10.1097/HJH.0b013e328363e964 |
| [3] | O'BRIEN E. Twenty-four-hour ambulatory blood pressure measurement in clinical practice and research:a critical review of a technique in need of implementation[J]. Journal of Internal Medicine, 2011, 269(5): 478–495. DOI:10.1111/jim.2011.269.issue-5 |
| [4] | 非接触、非介入式改变医疗保健[DB/OL]. (2013-07-25)[2016-08-28]. http://news.cecb2b.com/info/20130725/920756.shtml. |
| [5] | Non-contact and non-invasive changes medical insurance.[DB/OL]. (2013-07-25)[2016-08-28]. http://news.cecb2b.com/info/20130725/920756.shtml. |
| [6] |
张政波, 吴太虎. 无创血压测量技术与进展[J].
中国医疗器械杂志, 2003, 27(3): 196–199.
ZHANG Zheng-bo, WU Tai-hu. Noninvasive blood pressure measurement technology and its progress[J]. Chinese Journal of Medical Instrumentation, 2003, 27(3): 196–199. |
| [7] |
郑理华, 窦建洪, 何兴华, 等. 无创血压测量技术的改进与进展[J].
中国医学装备, 2013, 10(3): 49–52.
ZHENG Li-hua, DOU Jian-hong, HE Xing-hua, et al. Improvement and progress of noninvasive blood pressure measurement technology[J]. China Medical Equipment, 2013, 10(3): 49–52. |
| [8] | MCCOMBIE D B, SHALTISP A, REISNER A T, et al. Adaptive hydrostatic blood pressure calibration:Development of a wearable, autonomous pulse wave velocity blood pressure monitor[C]//200729th Annual International Conference of the IEEE Engineering in Medicine and Biology Society. Lyon:IEEE, 2007:370-373. https://www.ncbi.nlm.nih.gov/pubmed/18001967# |
| [9] |
李申龙, 李毅彬, 李洪阳, 等. 基于脉搏波相位差的无创连续血压测量方法[J].
传感器与微系统, 2016, 35(1): 62–64.
LI Shen-long, LI Yi-bin, LI Hong-yang, et al. Non-invasive continuous blood pressure measurement based on phase difference of pulse wave[J]. Transducer and Microsystem Technologies, 2016, 35(1): 62–64. |
| [10] |
向海燕, 俞梦孙. 用脉搏波传导时间实现血压连续测量[J].
医疗卫生装备, 2006, 27(2): 19–21.
XIANG Hai-yan, YU Meng-song. Measurement of continuous blood pressure via pulse wave translation time[J]. Medical Equipment, 2006, 27(2): 19–21. |
| [11] | ZAKARIA N A, SHARIFMUDDIN N B, RIDZWAN W M F W M, et al. Pulse wave transit time and its relationship with systolic blood pressure[C]//6th World Congress of Biomechanics (WCB 2010). Singapore:Springer, 2010:1354-1357. https://link.springer.com/chapter/10.1007%2F978-3-642-14515-5_345 |
| [12] | SUN Y, PAPIN C, AZORIN-PERIS V, et al. Use of ambient light in remote photoplethysmographic systems:comparison between a high-performance camera and a low-cost webcam[J]. Journal of Biomedical Optics, 2012, 17(3): 0370051–03700510. |
| [13] | SUN Y, HU S, AZORIN-PERIS V V, et al. Noncontact imaging photoplethysmography to effectively access pulse rate variability[J]. Journal of Biomedical Optics, 2013, 18(6): 061205. |
| [14] |
李章俊, 王成, 朱浩, 等. 基于光电容积脉搏波描记法的无创连续血压测量[J].
中国生物医学工程学报, 2012, 31(4): 607–614.
LI Zhang-jun, WANG Cheng, ZHU Hao, et al. Non-invasive continuous blood pressure measurement based on photoplethysmographic[J]. Chinese Journal of Biomedical Engineering, 2012, 31(4): 607–614. |
| [15] | KAMSHILIN A A, MIRIDONOV S, TEPLOV V, et al. Photoplethysmographic imaging of high spatial resolution[J]. Biomedical Optics Express, 2011, 2(4): 996–1006. DOI:10.1364/BOE.2.000996 |
| [16] | TENG X F, ZHANG Y T. The effect of applied sensor contact force on pulse transit time[J]. Physiological Measurement, 2006, 27(8): 675–684. DOI:10.1088/0967-3334/27/8/002 |
| [17] | TENG X F, ZHANG Y T. The effect of contacting force on photoplethysmographic signals[J]. Physiological Measurement, 2004, 25(5): 1323–1335. DOI:10.1088/0967-3334/25/5/020 |
| [18] | JONATHAN E, LEAHY M J. Cellular phone-based photoplethysmographic imaging[J]. Journal of Biophotonics, 2011, 4(5): 293–296. DOI:10.1002/jbio.v4.5 |
| [19] | JONATHAN E, LEAHY M J. Investigating a smartphone imaging unit for photoplethysmography[J]. Physiological Measurement, 2010, 31(11): N79. DOI:10.1088/0967-3334/31/11/N01 |
| [20] | POH M Z, MCDUFF D J, PICARD R W. Advancements in noncontact, multiparameter physiological measurements using a webcam[J]. IEEE Transactions on Biomedical Engineering, 2011, 58(1): 7–11. DOI:10.1109/TBME.2010.2086456 |
| [21] | HUMPHREYS K, WARD T, MARKHAM C. Noncontact simultaneous dual wavelength photoplethysmography:a further step toward noncontact pulse oximetry[J]. Review of Scientific Instruments, 2007, 78(4): 044304. DOI:10.1063/1.2724789 |
| [22] |
肖晓. 血压为何会升高[J].
药物与人, 2004(1): 14.
XIAO Xiao. Why blood pressure rises[J]. Medicine and People, 2004(1): 14. |



